Отобранный образец измельчается мясорубкой. 5 г измельченной средней пробы взвешивают в химическом стакане с погрешностью + 0,01 г. и добавляют 200 мл дистиллированной воды. Через 40 мин настаивания (при периодическом помешивании стеклянной палочкой) водную вытяжку фильтруют через бумажный фильтр. Для определения хлоридов берут 1 мл водной вытяжки в мерную колбу на 100 мл и доводят до метки дистиллированной водой. Полученный раствор используют для ввода в хроматограф.
Выполнение измерений
Готовят градуировочные растворы объемно-весовым методом. Для приготовления исходного раствора хлорид-иона концентрацией 1 г/л необходимо взять навеску 2,1 г хлористого калия и растворить в дистиллированной воде в отдельной мерной колбе вместимостью 1000 мл.
Установку и включение хроматографа осуществляют в соответствии с инструкциями по эксплуатации хроматографа Цвет-3006М. На насосе задают расход элюента 2,0 см3/мин, шкалу чувствительности устанавливают «32». Устанавливают режимные параметры и вводят градуировочный раствор в дозатор хроматографа. Снимают хроматограммы стандартных растворов. Градуировочный коэффициент К для хлорид ионов рассчитывается по формуле:
 (.4)
(.4)
где hгр – высота пика компонента в градуировочном растворе, мм;
Сгр – концентрация компонента в градуировочном растворе, мг/л.
Проведение анализа
Вводят в хроматограф водную вытяжку для определения хлорид-иона. Снимают хроматограмму. Время выхода пика хлорида 10 мин. Концентрацию хлорид-иона в пробе (Спробы) вычисляют по формуле:
Спробы(мг/кг)= 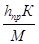 (.5)
(.5)
где hпр – высота пика компонента в пробе, мм;
М – навеска пробы, г.
Аргентометрическое определение хлоридов в воде
Метод основан на титровании хлорид-ионов раствором нитрата серебра в нейтральной или слабощелочной среде (рН=6,5–10) в присутствии индикатора K2CrO4.
Сl- + Ag+ → AgCl ↓
Определению мешает присутствие ионов РО43 – (> 25 мг/л), Fe3+ (> 10 мг/л) и катионов, образующих осадки с Сl –.
Рабочий раствор нитрата серебра готовят следующим образом: AgNO3– 2,4 г AgNO3 помещают в мерную колбу на 1 литр и доводят дистиллированной водой до метки. Точную концентрацию устанавливают по раствору NaCl, приготовленному из фиксанала или по точной навеске.
Раствор AgNO3 для качественного определения хлорид-ионов -10%-й.
Раствор K2CrO4 – 5%-й.
Выполнение определения
К 5 мл исследуемой воды добавляют 3 капли 10%-го раствора AgNO3. Приближенное содержание Сl – определяют в соответствии с таблицей
Таблица 1 – Характер осадка хлорида серебра в зависимости от концентрации хлорид-ионов
| Признаки | Опалесценция, слабая муть | Сильная муть | Хлопья, осаждающиеся не сразу | Белый объемистый осадок |
| Cодержание Сl – (мг/л) | 1–10 | 10–60 | 50–100 | > 100 |
В зависимости от содержания СГ необходимо брать для анализа различный объем воды. Если содержание хлорид-иона – в пределах 100–250 мг/л, для анализа необходимо брать 100 мл воды; если 250–280 мг/л – 50 мл воды; если > 800 мг/л – объем воды берется < 50 мл. Количественное определение Сl –.
К необходимой для анализа аликвоте воды (100 мл или меньше) добавляют 1 мл 5%-го раствора K2CrO4 и титруют раствором AgNO3 до появления оранжево-бурой окраски. Расчет содержания хлоридов ведут по формуле:
 (.6)
(.6) 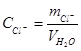 (.7)
(.7)
 (.8)
(.8)
где mCl− – масса хлорид-иона, г; CCl − концентрация хлорид-иона, мг/л; ТAgNO3/ Cl- – титр раствора AgNO3 пo хлорид-иону, г/мл; VAgNO3 – объем раствора AgNO3, израсходованный на титрование, мл; VH2O - объем воды, взятой для анализа, л.