Учреждение образования
«Международный государственный экологический университет
Им. А.Д Сахарова
Кафедра «Возобновляемые источники энергии»
Лабораторная работа
| Расчет количества теплоты для обеспечения температурного режима гальванического процесса | ||
| по дисциплине «Основы технологий производств» | ||
Минск – 2012
Цель работы:
- получить представление об основах технологии гальванических процессов;
- ознакомиться с технологическим процессом хромирования деталей;
- закрепить теоретические знания по составлению тепловых балансов производств;
- рассчитать количество теплоты, требующейся для обеспечения температурного режима процесса хромирования деталей.
Общие положения
Гальванизация – процесс осаждения одного металла на другой в виде электролитов. Покрытия, которые получают с помощью гальванизации, отличаются высокой прочностью, а сам процесс - экономичностью. Электролитами служат водные растворы солей и кислот.
Сущность электролитического процесса сводится к следующему: молекулы солей, растворенные в воде, распадаются на положительные и отрицательные ионы. Положительными являются ионы водорода и металлов, а отрицательными - кислотные и водные остатки. При пропускании через раствор постоянного электрического тока, те ионы, которые заряжены положительно, стремятся к отрицательному электроду, а ионы, заряженные отрицательно, - к положительному. Электрод, служащий положительным полюсом, называется анодом, а отрицательный - катодом. Ионы металлов заряжаются положительно и стремятся к катоду, в качестве которого выступает покрываемое изделие. А анодом служит пластинка из металла, которым покрывают изделие. При всех гальванических процессах используются ванны, изготовленные из кислоупорных материалов.
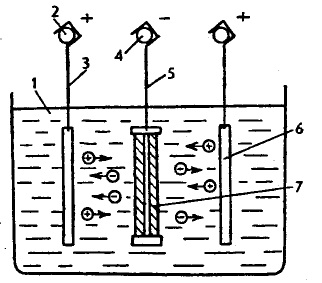
1 — ванна; 2 — анодная штанга; 3 —подвеска для анодных пластин;
4 — катодная штанга; 5 — подвеска для детали; 6 — анод; 7 — деталь (катод).
Рис. 1- Схема электролитического осаждения металла
Хромирование — диффузионное насыщение поверхности стальных изделий хромом, либо процесс осаждения на поверхность детали слоя хрома из электролита, содержащего раствор соли хромового ангидрида, под действием электрического тока. При хромировании деталь является катодом, а в качестве анодов применяются нерастворимые свинцовые пластины (полукольца). Схема электролитического восстановления деталей хромированием показана на рис. 2.
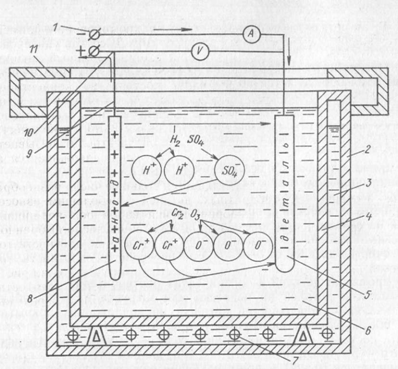
1 -электрическая шина катода; 2 - наружная стенка ванны; 3 -вода для подогрева электролита в ванне; 4- внутренняя стенка ванны; 5 - катод |деталь (—)]; 6 - электролит; 7- электроподогреватель; 8 - анод [свинцовая пластина (+)]; 9 - подвеска; 10 - электрическая шина анода (+); 11- крышка ванны.
Рис. 2 - Схема электролитического восстановления деталей хромированием
Области применения хромовых покрытий. Электролитическое хромирование применяется для внешней отделки изделий, повышения износостойкости, для защиты от коррозии и в ряде других случаев. Декоративные и защитно-декоративные покрытия хромом отличаются долговечностью. Поэтому многие изделия, и в особенности работающие в тяжелых условиях эксплуатации, подвергаются декоративному хромированию: например, детали автомобилей, самолетов, вагонов, приборов, а также инструменты и изделия бытового характера.
Полированные хромовые покрытия обладают хорошей отражательной способностью. Коэффициент отражения света хромом достигает 70%. Наряду с этим, из хромового электролита возможно осаждение черного хрома, применяющегося для уменьшения коэффициента отражения света.
Износостойкие хромовые покрытия применяются для многих инструментов и деталей машин, работающих на трение. К хромированию прибегают при покрытии новых деталей, а также при восстановлении изношенных, потерявших размеры во время работы на трение. Большое значение имеет исправление деталей, забракованных по размерам.
Применение износостойких хромовых покрытий для восстановления изношенных деталей станков и двигателей внутреннего сгорания позволяет во много раз увеличить срок их службы. Примерами подобных деталей могут служить шпиндели станков, шейки коленчатых валов, распределительные валики, толкатели клапанов, поршневые пальцы, шейки валиков различных агрегатов и другие детали. Хромовые покрытия нашли применение также для защиты изделий от коррозии. Хром, осажденный при определенных условиях электролиза, обеспечивающих получение беспористых осадков при толщине слоя 40 – 50 мк, защищает стальные изделия от атмосферной коррозии и коррозии в морской воде.
В промышленности хромирование используется для снижения трения, повышения износостойкости, повышения коррозионной стойкости. Этот процесс обеспечивает повышенную устойчивость стали к газовой коррозии (окалиностойкость) при температуре до 800 °C, высокую коррозионную стойкость в таких средах, как вода, морская вода и азотная кислота. Хромирование сталей содержащих свыше 0,3-0,4 %С, повышает также твёрдость и износостойкость. Твердость хрома составляет от 66 до 70 HRC. Толщина хромового покрытия обычно составляет от 0.075 до 0.25 мм, но встречаются и более толстые, и более тонкие слои. Поверхностные дефекты при хромировании усиливаются и поверхность подлежит последующей обработке, так как хромирование не дает эффекта выравнивания.
Химикаты для хромирования. Электролиты для хромовых ванн приготовляются из двух основных компонентов – хромового ангидрида и серной кислоты. Хромовый ангидрид CrO3. Молекулярный вес 100. Удельный вес 2,7. Выпускаемый отечественною промышленностью хромовый ангидрид представляет собой плавленую кристаллическую массу темно-красного цвета. На воздухе хромовый ангидрид поглощает влагу.
Серная кислота H2SO4. Молекулярный вес 98,08. Удельный вес 1,84. Для приготовления электролита используется чистая серная кислота. В порядке исключения допускается применение технической кислоты.
Составление электролита. Для приготовления электролита рассчитанное количество хромового ангидрида дробится на небольшие куски, загружается в ванну хромирования и заливается для лучшего растворения водой, подогретой до 60-80 оС. При этом можно использовать водопроводную воду, не загрязненную железом, однако, в районах с жесткой водопроводной водой для этих целей необходимо пользоваться конденсатором или даже дистиллированной водой.
После растворения хромового ангидрида раствор перемешивают и определяют в нем содержание CrO3 по удельному весу. Раствор после тщательного перемешивания подвергают анализу и, установив действительное содержание CrO3 и H2SO4, подсчитывают и дополнительно вводят недостающее количество компонентов. Для нормального осаждения хрома рекомендуется содержание в электролите небольшого количества Cr3+, около 2-4 г/л. В готовом электролите производят пробное хромирование.
Корректирование электролита. Для поддержания постоянной концентрации CrO3 и H2SO4 электролит периодически корректируют путем введения в него новых порций хромового ангидрида и серной кислоты. Количество добавляемого в ванну хромового ангидрида определяется на основании удельного веса электролита или результатам анализа. Добавление в ванну CrO3 осуществляется ежедневно. Корректирование электролита серной кислотой производится значительно реже. Один раз в 7-10 дней электролит подвергают анализу на содержание трех- и шестивалентного хрома и серной кислоты. На основании анализа рассчитывают недостающее количество H2SO4 и вводят его в электролит. После этого электролит тщательно перемешивают и дают ему отстояться. Поэтому серную кислоту рекомендуется вводить в ванну во время перерывов в работе.
Работа хромовой ванны. Гальванические ванны предназначены для подготовки поверхностей металлических деталей (конструкций), а также для нанесения на их поверхность различных покрытий.
Залогом успеха при хромировании является правильность выбора режима электролиза, а также соблюдение его при хромировании. Совершенно не допускаются отклонения от установленной величины плотности тока и температуры электролита. Колебание последней допускается в пределах +- 1о. Для получения одинаковой плотности тока, на одновременно загруженных в ванну деталях необходимо руководствоваться следующими правилами. Подвески и контакты (крючки, крючки с прижимами и т.п.) должны изготавливаться из одинаковых материалов. Поперечное сечение токопроводящих частей подвесок должно быть рассчитано на требуемую силу тока без значительного нагревания. Качество контактов при хромировании ввиду применения больших плотностей тока имеет исключительно важное значение. Поэтому поверхность контактов необходимо тщательно очищать от коррозии и всякого налета электролита.
Кроме того, расстояние между изделиями и анодами в ванне для всех подвесок должно быть одинаковым. Несоблюдение этих требований может привести к неоднородности покрытия по толщине слоя хрома, образованию так называемого “пригара” на одних деталях и матовых осадков на других. В процессе хромирования не допускаются перерывы тока, так как при повторном наращивании происходит отслаивание хрома.
Деталь, подвергаемая хромированию, как правило, проходит через следующие шаги:
- очистка для удаления сильных загрязнений;
- тонкая очистка, для удаления следов загрязнений;
- предварительная подготовка (варьируется в зависимости от материала основы);
- помещение в ванну с насыщенным раствором и выравнивание температуры;
- подключение тока и выдержка до получения нужной толщины.
Используемые при хромировании реагенты и отходы процесса чрезвычайно токсичны, в большинстве стран этот процесс находится под строгим регулированием.
Последовательность расчета
Как известно из первого закона термодинамики приходная часть энергетического баланса равна расходной части баланса. Поэтому, чтобы определить количество теплоты, необходимой для проведения процесса, надо предварительно рассчитать расходную часть теплового баланса. Расходная часть состоит из двух составляющих: расход теплоты на разогрев ванны до рабочей температуры и расход теплоты на поддержание температуры электролита на протяжении всего процесса работы ванны.
1. Расход тепловой энергии (Qразогр) на разогрев ванны до рабочей температуры электролита
Qразогр = Qрж + Qрв + Qп.исп + Qп.ст.в (1)
где Qр.ж - расход теплоты на разогрев раствора (ккал/час), рассчитывается по формуле (2);
Qр.в - расход теплоты на нагрев конструкции ванны (ккал/час), рассчитывается по формуле (3);
Qп.исп - расход теплоты на компенсация потерь на испарение жидкости с открытой поверхности, (ккал/час) рассчитывается по формуле (4);
Qп.ст.в - расход теплоты на компенсацию потерь через стенки ванны (ккал/час), рассчитывается по формуле (5).

(2)
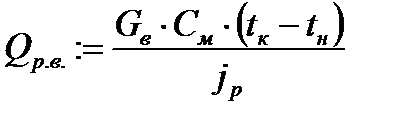
(3)
где Gр.ж. - количество разогреваемого электролита (кг),
Cр.ж. - теплоемкость электролита (ккал/кг*гр),
tк, tн - конечная и начальная температура электролита, оС,
Јр - время разогрева, час;
Gв . – масса ванны (кг),
Cм - теплоемкость материала ванны (ккал/кг*гр),

(4)
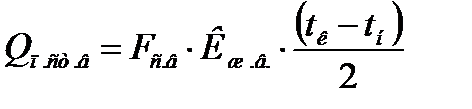
(5)
где Fисп – поверхность зеркала испарения, (м2);
r = скрытая теплота парообразования;
g - вес жидкости, испаряющейся с 1 м2 зеркала испарения, (кг/час*м2), рассчитывается по формуле (7);
Fс.в. – поверхность стенок ванны (м2),
Кж.в. – коэффициент теплопередачи от стенки отдельно стоящего оборудования, (ккал/м2*час*гр) рассчитывается по формуле (6),

(6)
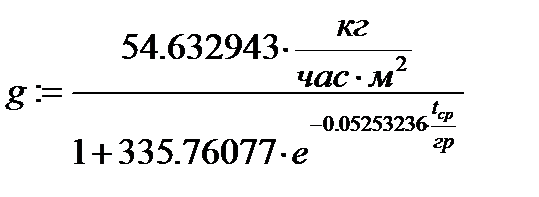
(7)
где tср = (tк – tн)/2.