В главных подгруппах сверху вниз:
• число энергетических уровней в атоме увеличивается;
• число электронов на внешнем уровне одинаково;
• радиус атомов увеличивается;
• прочность связи электронов внешнего уровня с ядром уменьшается;
• энергия ионизации уменьшается;
• сродство к электрону уменьшается;
• ЭО уменьшается;
• металличность элементов увеличивается;
• неметалличность элементов уменьшается.
Периодом называется т акая последовательность элементов, на протяжении которой свойства их изменяются в порядке постепенного усиления от типично металлических дотипично неметаллических (металлоидных). Заканчивается каждый период инертным элементом. По мере ослабления металлических свойств у элементов начинают появляться и постепенно усиливаются неметаллические свойства; в середине периодов находятся обычно элементы, совмещающие в той или иной степени как металлические, так и неметаллические свойства. Эти элементы часто называют амфотерными.
Период – это последовательность элементов (от щелочного металла до инертного газа), атомы которых имеют одинаковое число энергетических уровней, равное номеру периода.
Состав периодов.
Периоды не равномерны по числу входящих в них элементов. Первые три называются малыми, остальные четыре — большими.
В малых периодах от щелочного металла к инертному газу:
• заряд ядер атомов увеличивается;
• число энергетических уровней не изменяется;
• число электронов на внешнем уровне увеличивается от 1 до 8;
• радиус атомов уменьшается;
• прочность связи электронов внешнего слоя с ядром увеличивается;
• энергия ионизации увеличивается;
• сродство к электрону увеличивается;
• ЭО увеличивается;
• металличность элементов уменьшается;
• неметалличность элементов увеличивается.
Все d -элементы данного периода похожи по своим свойствам – все они являются металлами, имеют мало различающиеся радиусы атомов и значения ЭО, поскольку содержат одинаковое число электронов на внешнем уровне (например, в 4-м периоде – кроме Cr и Cu).
Современная формулировка периодического закона. Значение периодического закона и периодической системы химических элементов Д.И. Менделеева для развития науки и понимания химической картины мира.
После работ Г. Мозли атомная масса элемента постепенно начала уступать свою первенствующую роль новой, еще не ясной по своему внутреннему (физическому) смыслу, но более четкой константе — порядковому или, как теперь называют, атомному номеру элемента. Физический смысл этой константы был выявлен в 1920 г. работами английского ученого Д.Чедвика. Д. Чёдвик экспериментально установил, что порядковый номер элемента численно равен величине положительного заряда Z ядра атома этого элемента, т. е. количеству протонов в ядре. Оказалось, что Д. И. Менделеев, сам того не подозревая, расставил элементы в последовательности, точно соответствующей возрастанию заряда ядер их атомов.
К этому же времени было также установлено, что атомы одного и того же элемента могут отличаться друг от друга своей массой; такие атомы получили название изотопов. Примером могут служить атомы:  и
и 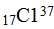 . В периодической системе изотопы одного и того же элемента занимают одну клетку. В связи с открытием изотопов было уточнено понятие химический элемент.
. В периодической системе изотопы одного и того же элемента занимают одну клетку. В связи с открытием изотопов было уточнено понятие химический элемент.
В настоящее время химическим элементом называют вид атомов, имеющих одинаковый заряд ядра - одинаковое количество протонов в ядре. Была уточнена и формулировка периодического закона.