ГОД
Задача 1.
Установите соответствие между формулой вещества и электронной конфигурацией основного состояния входящего в ее состав хрома с учетом его степени окисления:
1) 
2) 
3) 
4)  .
.
Ответ: 1)  –
–  ,
,
2)  –
–  ,
,
3)  –
–  ,
,
4)  –
– 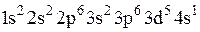 .
.
Задача 2.
Установите соответствие между формулой молекулы или иона и типом гибридизации валентных орбиталей центрального атома.
1. 
2. 
3. 
4.  .
.
Ответ: 1.  – sp3,
– sp3,
2.  – sp2,
– sp2,
3.  – sp,
– sp,
4.  – sp3d2.
– sp3d2.
Задача 3.
Комплексное соединение никеля содержит 33,71 % (мас.) Ni, 13,71 % (мас.) C, 16,00 % (мас.) N и кислород. Комплекс не заряжен, а его молекула имеет тетраэдрическое строение. Установите формулу комплексного соединения, степень окисления и координационное число центрального атома, тип гибридизации его валентных орбиталей. (Величины относительных атомных масс использовать с точностью до целого значения.)
1). Формула комплекса
2). Степень окисления никеля
3). Координационное число
4). Тип гибридизации
Ответ: 1). Формула комплекса –  .
.
2). Степень окисления никеля – 0.
3). Координационное число – 4.
4). Тип гибридизации –  .
.
Задача 4.
К солевому раствору, содержащему хлориды калия и лития, в котором суммарная массовая доля катионов равна суммарной массовой доле анионов, добавили раствор нитрата серебра. В образовавшемся растворе суммарная массовая доля катионов также оказалась равной суммарной массовой доле анионов. Расположите ионы, находящиеся в данном растворе, в порядке увеличения их молярной концентрации.
Ответ:  .
.
Задача 5.
Наименьшее значение суммы коэффициентов в уравнении реакции взаимодействия сульфата алюминия с сульфидом натрия в водном растворе равна …
Ответ: 18.
Задача 6.
При взаимодействии стехиометрических количеств дихромата калия с нитритом натрия в присутствии серной кислоты образуется раствор с массовой долей сульфата калия 5,46 %. Массовая доля нитрата натрия в этом растворе составит _____ %. (Ответ привести c точностью до целого числа, значения относительных атомных масс использовать с точностью до целого.)
Ответ: 8.
Задача 7.
Значение рН, при котором начнется осаждение гидроксида железа (II) из
0,001 М раствора его сульфата, равно ____. (Ответ привести с точностью до сотых, раствор считать идеальным,  .)
.)
Ответ: 7,95.
Задача 8.
Сточные воды металлургического производства содержат растворимые соединения марганца, стронция, алюминия, серебра и никеля (II). Используя систематический анализ кислотно-щелочным методом, расположите реагенты, последовательным действием которых можно разделить данные катионы.
Ответ:  ;
;  ;
;  ;
;  .
.
Задача 9.
Галогенид двухвалентного металла массой 0,1596 г растворили в воде и оттитровали раствором ЭДТА в аммиачном буфере в присутствии эриохромового черного. На титрование было израсходовано 16,8 мл 0,10 М раствора титранта. Формула исходного галогенида имеет вид ___. (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например, CuSO4, Na2CrO4.)
Ответ:  .
.
Задача 10.
Среди перечисленных процессов:  ;
;
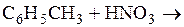 ;
;  ;
;  ;
;  ,
,
реакциями, протекающими по механизму электрофильного замещения, являются …
Ответ:  ;
; 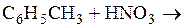 ;
;  .
.
Задача 11.
При сплавлении со щелочью натриевой соли одноосновной карбоновой кислоты образовалось 15,6 г углеводорода X, а при электролизе водного раствора такого же количества этой соли на инертном аноде образовалось 15,4 г углеводорода Y. Если оба процесса протекают количественно, то молярная масса исходной соли составляет _____ г/моль. (Ответ привести с точностью до целого значения.)
Ответ: 144.
Задача 12.
Установите соответствие между формулой исходного соединения и продуктом его взаимодействия с водой.
| Формула исходного соединения | Продукт взаимодействия с водой |
А) 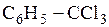
| 1) 
|
Б) 
| 2) 
|
В) 
| 3) 
|
Г) 
| 4) 
|
5) 
| |
6) 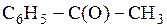
| |
В ответ укажите последовательность цифр без пробелов и запятых, соответствующую формулам продуктов взаимодействия указанных исходных соединений с водой.
Ответ: 2466.
Задача 13.
Синтез вещества Х4, являющегося исходным для получения одного из самых распространенных медицинских препаратов, можно осуществить по схеме:
 .
.
Установите соответствие между веществами X1 – X4 данной схемы превращений и их названиями.
Ответ:
1. Х1 – хлорбензол,
2. Х2 – фенолят натрия,
3. Х3 – 2-гидроксибензоат натрия,
4. Х4 – 2-гидроксибензойная кислота.
5.
Задача 14.
На нейтрализацию водного раствора, образовавшегося при гидролизе 1,000 г ангидрида одноосновной органической кислоты, потребовалось 17,70 мл 0,5М раствора  . Молекулярная формула кислоты имеет вид ___. (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например, C2H4О2, C5H10O2.)
. Молекулярная формула кислоты имеет вид ___. (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например, C2H4О2, C5H10O2.)
Ответ: C7H6O2.
Задача 15.
Синтез-газ (смесь CO и Н2) является исходным сырьем для промышленного производства метанола и многих других продуктов химической промышленности. Одним из способов получения синтез-газа с необходимым соотношением СО и Н2 является реакция  . Синтез проводился в реакторе объемом 1 м3 с использованием эквимолярной смеси оксида углерода (II) и паров воды при температуре 450 єС. Согласно справочным данным, приведенным в таблице,
. Синтез проводился в реакторе объемом 1 м3 с использованием эквимолярной смеси оксида углерода (II) и паров воды при температуре 450 єС. Согласно справочным данным, приведенным в таблице,
| Вещество | 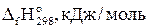
| 
|
| H2(г) | 130,68 | |
| CO2(г) | -393,51 | 213,74 |
| CO(г) | -110,53 | 197,67 |
| H2O(г) | -241,82 | 188,83 |
термодинамический выход водорода в данных условиях составляет _____ %.
(Ответ привести с точностью до целого числа, зависимостью термодинамических функций от температуры пренебречь, газы считать идеальными, R = 8,31 Дж/(моль∙К).)
Ответ: 71.
Задача 16.
Реакция термического разложения оксида азота (IV) 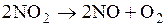 является реакцией второго порядка. Если константы скорости этой реакции при температурах 350 єС и 375 єС равны соответственно 1,57 л/моль-1∙ с-1 и 3,59 л/моль-1∙ с-1 , то при температуре 400 єС константа скорости реакции составит ____ л/моль-1∙ с-1. (Энергию активации в данном интервале температур считать постоянной, R = 8,31 Дж/(моль∙К).)
является реакцией второго порядка. Если константы скорости этой реакции при температурах 350 єС и 375 єС равны соответственно 1,57 л/моль-1∙ с-1 и 3,59 л/моль-1∙ с-1 , то при температуре 400 єС константа скорости реакции составит ____ л/моль-1∙ с-1. (Энергию активации в данном интервале температур считать постоянной, R = 8,31 Дж/(моль∙К).)
Ответ: 7,72.
Задача 17.
В равных количествах воды растворено 8,4 г мочевины и 7,1 г сульфата натрия. Температуры кипения обоих растворов одинаковы.
Значение кажущейся степени диссоциации сульфата натрия составляет ______%. (Ответ привести c точностью до целого числа.)
Ответ: 90.
Задача 18.
Для улучшения прочности и защитно-декоративных свойств серебряного покрытия процесс электролитического серебрения осуществляется после предварительного меднения поверхности изделия. Если толщина слоя осажденной меди равна 5 мкм, время электролиза и сила тока не изменялись, выход по току при меднении составлял 95 %, при серебрении – 98,6 %, то толщина серебряного покрытия будет равна _____ мкм.
(Ответ привести c точностью до целого числа, 
 .)
.)
Ответ: 15.
Задача 19.
При ферментативном гидролизе крахмала получен остаточный декстрин ( ), осмотическое давление 0,08 %-ного раствора которого(
), осмотическое давление 0,08 %-ного раствора которого( = 1 г/см3) при 45оС равно 6,525 Па, а поведение раствора подчиняется уравнению Вант-Гоффа. Число остатков глюкозы, образующих данный декстрин, составляет ____. (Ответ привести c точностью до целого числа.)
= 1 г/см3) при 45оС равно 6,525 Па, а поведение раствора подчиняется уравнению Вант-Гоффа. Число остатков глюкозы, образующих данный декстрин, составляет ____. (Ответ привести c точностью до целого числа.)
Ответ: 2000.
Задача 20.
Для золя, образовавшегося при сливании 100 мл 0,004М раствора йодида магния и 100 мл 0,005 М раствора нитрата серебра, установите:
1) формулу потенциалопределяющего иона
2) электрод, к которому движется коллоидная частица в электрическом поле
3) формулу иона, обладающего наименьшим порогом коагуляции
Ответ:
1) формула потенциалопределяющего иона – 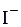 ;
;
2) электрод, к которому движется коллоидная частица в электрическом поле, – анод;
3) формула иона, обладающего наименьшим порогом коагуляции, –  .
.
ГОД
Задание 1
Установите соответствие между формулой вещества и электронной конфигурацией основного состояния входящего в ее состав марганца с учетом его степени окисления.
1) 
2) 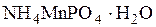
3) 
4) 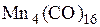
а) 
б) 
в) 
г) 
д) 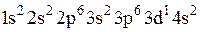
е) 
ж) 
Ответ: 1а, 2б, 3в, 4г
Задание 2
Установите соответствие между формулой молекулы или иона и типом гибридизации валентных орбиталей центрального атома.
1. 
2. 
3. 
4. 
а) sp3
б) sp2
в) sp
г) sp3d2
д) sp2d
е) sp3d
Ответ: 1а, 2б, 3в, 4г
Задание 3
Наименьшее значение суммы коэффициентов в уравнении реакции взаимодействия нитрата алюминия с силикатом натрия в водном растворе равно …
1) 22
2) 19
3) 18
4) 24
Ответ: 1)
Задание 4
Энергия активации реакции разложения антибиотика в водном растворе составляет 125,6 кДж/моль. При введении природного фермента в раствор той же концентрации ее значение понизилось до 106,2 кДж/моль. Для полного разложения 1 ммоль антибиотика в водном растворе при температуре, соответствующей стандартным условиям, в присутствии фермента потребуется в ____ раз(-а) меньше времени, чем в его отсутствие.
(Механизм протекания процесса в присутствии фермента и в его отсутствие считать одинаковым; R = 8,31 Дж/(моль∙К).)
1) 2525
2) 5050
3) 525
4) 1050
Ответ: 1)
Задание 5
Комплексное соединение железа содержит 32,56 % (мас.) Fe, 13,95 % (мас.) C, 16,28 % (мас.) N и кислород. Комплекс не заряжен, а его молекула имеет тетраэдрическое строение. Установите формулу комплексного соединения, степень окисления и координационное число центрального атома, тип гибридизации его валентных орбиталей.
(Величины относительных атомных масс использовать с точностью до целого значения.)
1. Формула комплекса –
2. Степень окисления железа –
3. Координационное число комплексообразователя –
4. Тип гибридизации комплексообразователя –
а) 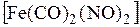
б) 0
в) 4
г) 
д) 
е) 
ж) +2
з) 3
и) 
Ответ: 1а, 2б, 3в, 4г
Задание 6
При взаимодействии стехиометрических количеств гидросульфита калия с перманганатом калия в присутствии серной кислоты образуется раствор с массовой долей сульфата калия 10,1 %. Массовая доля соединения марганца в этом растворе составит ____ %.
(Ответ привести c точностью до целого числа, значения относительных атомных масс использовать с точностью до целого.)
Ответ: 5
Задание 7
Значение рН, при котором начнется осаждение гидроксида кадмия из 0,001 М раствора его нитрата, равно …
(Ответ привести с точностью до десятых, раствор считать идеальным,  .)
.)
Ответ: 8,3
Задание 8
Проба сточных вод металлургического предприятия содержит катионы  Установите соответствие между формулой катиона и формулой реагента, которым можно определить данный катион в указанной смеси.
Установите соответствие между формулой катиона и формулой реагента, которым можно определить данный катион в указанной смеси.
1) 
2) 
3) 
4) 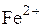
а) 
б) 
в) 
г) 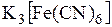
д) 
е) 
ж) 
з) 
Ответ: 1а, 2б, 3в, 4г
Задание 9
Сульфат двухвалентного металла массой 0,1124 г растворили в воде и оттитровали раствором трилона Б в оптимальных условиях в присутствии соответствующего индикатора. На титрование было израсходовано 14,8 мл 0,050 М раствора титранта. Формула исходного нитрата имеет вид ___.
(При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например CuSO4, Na2CrO4.)
Ответ: FeSO4
Задание 10
Схемы реакций, протекающих по механизму нуклеофильного присоединения, имеют вид …
1) 
2) 
3) 
4) 
5) 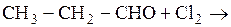
6) 
Ответ: 1, 2, 3
Задание 11
При сплавлении калиевой соли одноосновной карбоновой кислоты со щелочью образовалось 6,72 л (н. у.) газа X, а при электролизе водного раствора такого же количества этой соли на инертном аноде образовалось 17,1 г углеводорода Y. Если оба процесса протекают количественно, то формула кислоты, образующей исходную соль, имеет вид …
(При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например, C2H4O2, C6H12O2.)
Ответ: C5H10O2
Задание 12
Установите соответствие между реагирующими веществами и основным органическим продуктом их взаимодействия.

В ответе укажите последовательность цифр без пробелов и запятых, соответствующую формулам органических продуктов указанных взаимодействий.
Ответ: 4351
Задание 13
Синтез соединения Х4, являющегося исходным веществом для получения синтетических полимерных материалов, можно осуществить по схеме:
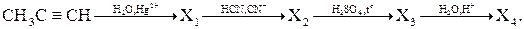
Установите соответствие между веществами X1 – X4 данной схемы превращений и их названиями.
1. 
2. 
3. 
4. 
а) пропанон
б) нитрил 2-гидрокси-2-метилпропановой кислоты
в) нитрил 2-метилпропеновой кислоты
г) 2-метилпропеновая кислота
д) нитрил 2-гидрокси-2-метилуксусной кислоты
е) нитрил 2-метилуксусной кислоты
ж) пропаналь
з) 2-метилпропановая кислота
Ответ: 1а, 2б, 3в, 4г
Задание 14
На нейтрализацию водного раствора, образовавшегося при гидролизе 0,100 г ангидрида двухосновной органической кислоты, потребовалось 20,40 мл 0,1 М раствора  . Молекулярная формула кислоты имеет вид …
. Молекулярная формула кислоты имеет вид …
(При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например C2H4О, C5H10O2.)
Ответ: C4H4O4
Задание 15
Водный раствор нитрата аммония с массовой долей растворенного вещества
1,6 % кристаллизуется при температуре -0,707 ºС. Кажущаяся степень диссоциации нитрата аммония в данном растворе составляет ___%.
(Ответ привести c точностью до целого числа,  град∙кг/моль.)
град∙кг/моль.)
Ответ: 90
Задание 16
При электролизе водного раствора сульфата металла на катоде выделилось 9,21 г металла, а на аноде 3,72 л газа (н. у.). Если выход по току для катодного процесса составляет 80 %, а для анодного – 100 %, то металлом является …
(В качестве ответа введите символ металла, используя латинскую раскладку клавиатуры, например Fe, Zn.)
Ответ: Cr
Задание 17
Одним из полимеров, используемых для получения бензо- и маслостойкой резины, является хлоропреновый каучук – полихлоропрен  Если осмотическое давление 0,05%-го раствора полихлоропрена (
Если осмотическое давление 0,05%-го раствора полихлоропрена ( = 1 г/см3) при 35 ºС равно 3,615 Па, а поведение раствора подчиняется уравнению Вант-Гоффа, то его степень полимеризации составляет …
= 1 г/см3) при 35 ºС равно 3,615 Па, а поведение раствора подчиняется уравнению Вант-Гоффа, то его степень полимеризации составляет …
(Ответ привести c точностью до целого числа, R = 8,31 Дж/моль×К,  .)
.)
Ответ: 4000
Задание 18
Коллоидные частицы (гранулы) золя йодида серебра, образовавшегося при сливании 0,001 М раствора йодида алюминия и 150 мл 0,004 М раствора нитрата серебра, в электрическом поле двигаются к катоду.
Установите:
1) объем раствора йодида алюминия
2) формулу потенциалопределяющего иона
3) формулу иона, обладающего наименьшим порогом коагуляции.
а) меньше 200 мл
б) 
в) 
г) больше 200 мл
д) 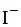
е) 
ж) равен 200 мл
з) 
Ответ: 1а, 2б, 3в
Задание 19
Смешали равные массы растворов нитрата серебра и бромида калия. В результате образовался раствор, в котором суммарная массовая доля катионов оказалась равной суммарной массовой доле анионов. Если масса конечного раствора на 81,2 % больше массы каждого из исходных растворов, то массовые доли нитрата серебра и бромида калия в исходных растворах равны ____ % и ____ % соответственно, а масса осадка образовавшегося при добавлении избытка щелочи к раствору, полученному из 200 г каждого из исходных растворов, составляет ______ г.
1) 11,9
2) 25,5
3) 11,6
4) 18,8
5) 21,2
6) 12,5
Ответ: 1,2,3
Задание 20
Для равновесной системы  термодинамические величины представлены в таблице
термодинамические величины представлены в таблице

Если температуру в системе повысить от 600 oC до 750 оС, то выход продуктов реакции увеличивается на _____ %.
(Ответ привести с точностью до целого числа, зависимостью термодинамических функций от температуры пренебречь, газы считать идеальными, R = 8,31 Дж/(моль∙К).)
Ответ: 19
ГОД
Задание 1
Установите соответствие между формулой вещества и электронной конфигурацией основного состояния входящего в ее состав марганца с учетом его степени окисления.
1) 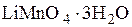
2) 
3) 
4) 
а) 
б) 
в) 
г) 
д) 
е) 
ж) 
Ответ: 1а, 2б, 3в, 4г
Задание 2
Установите соответствие между формулой молекулы или иона и типом гибридизации валентных орбиталей центрального атома.
1. 
2. 
3. 
4. 
а) sp3
б) sp2
в) sp
г) sp3d2
д) sp2d
е) sp3d
Ответ: 1а, 2б, 3в, 4г
Задание 3
Комплексное соединение кобальта содержит 23,79 % (мас.) Co, 3,63 % (мас.) H, 33,87 % (мас.) N и кислород. Комплекс не заряжен, а его молекула имеет октаэдрическое строение. Установите формулу комплексного соединения, степень окисления и координационное число центрального атома, тип гибридизации его валентных орбиталей. (Величины относительных атомных масс использовать с точностью до целого значения.)
1. Формула комплекса –
2. Степень окисления кобальта –
3. Координационное число комплексообразователя –
4. Тип гибридизации комплексообразователя –
а) 
б) +3
в) 6
г) 
д) 
е) 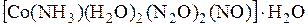
ж) +2
з) 4
и) 
к) 
л) 0
Ответ: 1а, 2б, 3в, 4г
Задание 4
Смешали равные массы растворов нитрата серебра и хлорида аммония. В результате образовался раствор, в котором суммарная массовая доля катионов оказалась равной суммарной массовой доле анионов. Если масса конечного раствора на 85,65 % больше массы каждого из исходных растворов, то массовые доли нитрата серебра и хлорида аммония в исходных растворах равны ____ % и ____ % соответственно, а масса осадка, образовавшегося при добавлении избытка щелочи к отфильтрованному раствору, полученному при сливании по 100 г каждого из исходных растворов, составляет ___ г.
1) 34
2) 5,35
3) 11,6
4) 17
5) 10,7
6) 5,8
7) 4,25
Ответ: 1,2,3
Задание 5
Наименьшее значение суммы коэффициентов в уравнении реакции взаимодействия сульфата хрома (III) с карбонатом калия в водном растворе равна …
1) 15
2) 22
3) 17
4) 12
Ответ: 1)
Задание 6
К раствору медного купороса массой 500 г с массовой долей сульфата (II) 12,8 % постепенно добавляют раствор йодида калия. Максимальная и минимальная масса осадка, который может образоваться в результате взаимодействия, составит ____ г и ____ г соответственно.
1) 127,2
2) 0
3) 76,4
4) 63,6
5) 101,6
Ответ: 1,2
Задание 7
В две колбы поместили по 1 л раствора, содержащего 0,1 моль нитрата диамминсеребра и 1 моль аммиака, и добавили в первую – хлорид, во вторую – бромид калия в количестве 0,001 моль каждой соли. Установите возможность выпадения осадка соответствующего галогенида в каждой колбе, если  ,
,  ,
,  (Растворы считать идеальными, диссоциацией гидрата аммиака пренебречь.)
(Растворы считать идеальными, диссоциацией гидрата аммиака пренебречь.)
1) осадок только с KBr
2) осадок только с KCl
3) осадок с KCl и KBr
4) осадок отсутствует
Ответ: 1)
Задание 8
Проба сточных вод металлургического предприятия содержит катионы  Установите соответствие между формулой катиона и формулой реагента, которым можно определить данный катион в указанной смеси.
Установите соответствие между формулой катиона и формулой реагента, которым можно определить данный катион в указанной смеси.
1)  –
–
2)  –
–
3)  –
–
4) 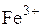 –
–
а) 
б) 
в) 
г) 
д) 
е) 
ж) 
з) 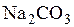
Ответ: 1а, 2б, 3в, 4г
Задание 9
Галогенид двухвалентного металла массой 0,0798 г растворили и объем раствора довели до 100 мл дистиллированной водой. Полученный раствор оттитровали раствором нитрата серебра в присутствии хромата натрия в качестве индикатора. На титрование было израсходовано 16,8 мл 0,10 М раствора  . Формула исходного галогенида имеет вид … (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например CuSO4, CaF2.)
. Формула исходного галогенида имеет вид … (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например CuSO4, CaF2.)
Ответ: MgCl2
Задание 10
Схемы реакций, протекающих по механизму электрофильного замещения, имеют вид …
1) 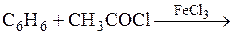
2) 
3) 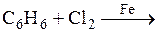
4) 
5) 
6) 
Ответ: 1, 2, 3
Задание 11
При сплавлении со щелочью натриевой соли предельной одноосновной карбоновой кислоты образовалось 24 г углеводорода X, а при электролизе водного раствора такого же количества этой соли на инертном аноде выделилось 23,2 г углеводорода Y. Если оба процесса протекают количественно, то формула кислоты, образующей исходную соль, имеет вид … (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например, C2H4O2, C6H12O2.)
Ответ: C3H6O2
Задание 12
Установите соответствие между реагирующими веществами и основным органическим продуктом их взаимодействия.

В ответе укажите последовательность цифр без пробелов и запятых, соответствующую формулам органических продуктов указанных взаимодействий.
Ответ: 1213
Задание 13
Синтез вещества Х4, являющегося исходным для получения популярного медицинского препарата, можно осуществить по схеме:

Установите соответствие между веществами X1 – X4 данной схемы превращений и их названиями.
1. 
2. 
3. 
4. 
а) 3-хлорпропен
б) пропен-2-ол-1
в) 3-хлорпропандиол-1,2
г) пропантриол-1,2,3
д) 1,2-дихлорпропан
е) нитрил 2-метилуксусной кислоты
ж) пропин
з) 3-хлорпропанол-1
Ответ: 1а, 2б, 3в, 4г
Задание 14
Производные непредельной одноосновной карбоновой кислоты, содержащей одну двойную связь, используются в промышленности при получении прозрачных полимерных материалов. Общее число атомов в образце данной кислоты массой 43 г составляет 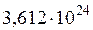 . Молекулярная формула кислоты имеет вид … (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например
. Молекулярная формула кислоты имеет вид … (При записи ответа используйте латинскую раскладку клавиатуры; индекс введите без пробела, как цифру, например  )
)
Ответ: C4H6O2
Задание 15
Для равновесной системы 

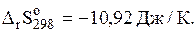 Если температуру в системе понизить от 800 oC до 500 оС, то выход продуктов реакции увеличится на _____ %. (Ответ привести с точностью до целого числа, зависимостью термодинамических функций от температуры пренебречь, газы считать идеальными, R = 8,31 Дж/(моль∙К).)
Если температуру в системе понизить от 800 oC до 500 оС, то выход продуктов реакции увеличится на _____ %. (Ответ привести с точностью до целого числа, зависимостью термодинамических функций от температуры пренебречь, газы считать идеальными, R = 8,31 Дж/(моль∙К).)
Ответ: 15
Задание 16
Для реакции  энергия активации составляет 124,6 кДж/моль. Если температура в системе понизилась от 100 до 60 оС, то для того, чтобы скорость реакции сохранила первоначальное значение, необходимо увеличить давление в ____ раз(-а). (Реакцию считать элементарной, R = 8,31 Дж/моль·К, ответ округлить до целого значения.)
энергия активации составляет 124,6 кДж/моль. Если температура в системе понизилась от 100 до 60 оС, то для того, чтобы скорость реакции сохранила первоначальное значение, необходимо увеличить давление в ____ раз(-а). (Реакцию считать элементарной, R = 8,31 Дж/моль·К, ответ округлить до целого значения.)
Ответ: 5
Задание 17
Водный раствор сульфата натрия с массовой долей растворенного вещества 2,8 % кристаллизуется при температуре - 0,968 ºС. Кажущаяся степень диссоциации нитрата аммония в данном растворе составляет ___%. (Ответ привести c точностью до целого числа,  град∙кг/моль.)
град∙кг/моль.)
Ответ: 80
Задание 18
При электролизе водного раствора сульфата металла на катоде выделилось 19,05 г металла, а на аноде 2,24 л газа (н. у.). Если выход по току для катодного процесса составляет 85 %, а для анодного – 100 %, то металлом является …
(В качестве ответа введите символ металла, используя латинскую раскладку клавиатуры, например Fe, Zn.)
Ответ: Cd
Задание 19
Образец поливинилхлорида, полученный полимеризацией 25 г хлорэтена, содержит 7,525∙1020 макромолекул. Хлорэтен, не вступивший в реакцию полимеризации, может обесцветить 500 г 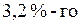 раствора брома в тетрахлорметане. Значение средней молярной массы поливинилхлорида составляет _____ г/моль. (Ответ привести с точностью до целого значения)
раствора брома в тетрахлорметане. Значение средней молярной массы поливинилхлорида составляет _____ г/моль. (Ответ привести с точностью до целого значения)
Ответ: 15000
Задание 20
Коллоидные частицы (гранулы) золя бромида серебра, образовавшегося при сливании 0,001 М раствора бромида магния и 100 мл 0,002 М раствора нитрата серебра, в электрическом поле двигаются к катоду. Установите:
1) объем раствора бромида магния
2) формулу потенциалопределяющего иона
3) формулу иона, обладающего наименьшим порогом коагуляции.
а) меньше 100 мл
б) 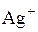
в) 
г) больше 100 мл
д) 
е) 
ж) равен 100 мл
з) 
Ответ: 1а, 2б, 3в
Год
Задание 1
Установите соответствие между формулой вещества и электронной конфигурацией основного состояния входящего в ее состав никеля с учетом его степени окисления.
1) 
2) 
3) 
4) 
а) 
б) 
в) 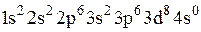
г) 
д) 
е) 
ж) 
Ответ: 1а, 2б, 3в, 4г
Задание 2
Установите соответствие между формулой молекулы или иона и типом гибридизации валентных орбиталей центрального атома.
1. 
2. 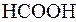
3. 
4. 
а) sp
б) sp2