Получение карбонильных соединений.
Лабораторные способы.
Щелочной гидролиз геминальных (содержат два атома галогена у одного атома углерода) дигалогенпроизводных УВ.
Реакция протекает при действии водных растворов щелочей на дигалогензамещенные углеводороды, содержащие два атома галогена у одного и того же атома углерода.
При щелочном гидролизе дигалогеналканов образуются двухатомные спирты, в которых две группы ОН соединены с одним атомом углерода. Эти вещества неустойчивы и при отщеплении воды, превращаются в карбонильные соединения.
Если два атома галогена связаны с первичным атомом углерода, то образуются альдегиды:
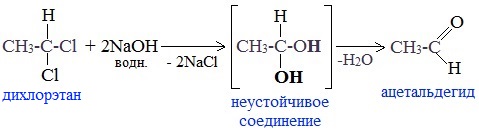
При гидролизе дигалогеналканов, содержащих атомы галогена у вторичного атома углерода, образуются кетоны:
Например,
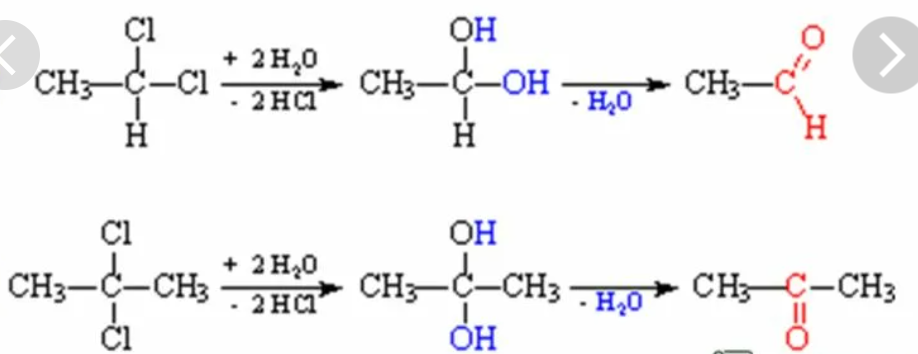
Получение бензальдегида:
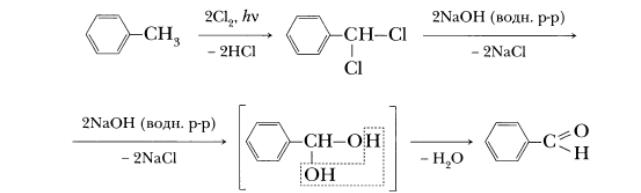
2. Озонолиз — реакция, в которой полностью разрушается двойная углерод-углеродная связь и молекула алкена превращается в две меньшие молекулы. Алкены даже при пониженных температурах легко окисляются озоном.
Озонолиз протекает в две стадии: первая — присоединение озона по двойной связи с образованием озонида, вторая — гидролиз озонида с образованием продуктов расщепления.
Озон пропускают через раствор алкена в инертном растворителе (например, в четыреххлористом углероде), после упаривания растворителя остается озонид в виде вязкого масла.
На примере изомерных бутенов
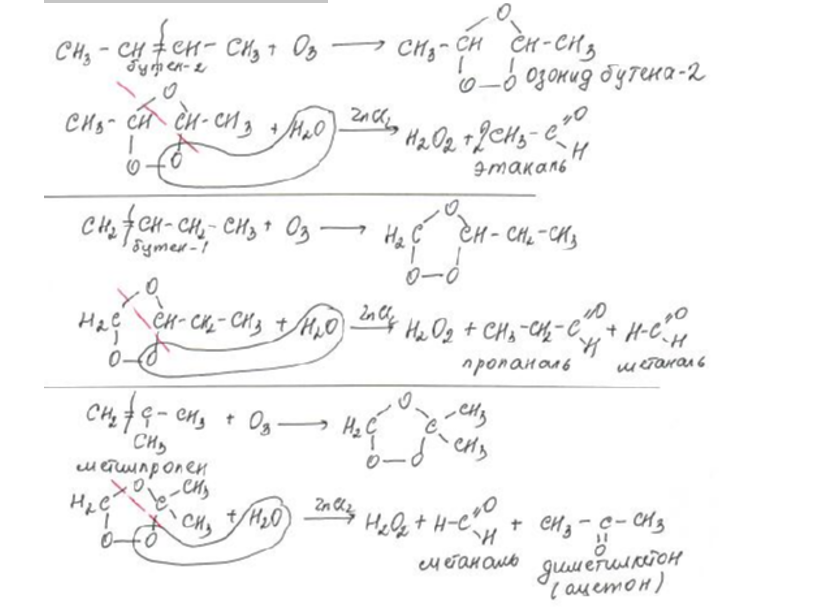
3.Окисление спиртов:
В лаборатории карбонильные соединения получают окислением спиртов в жестких условиях в присутствии сильных окислителей (дихромата калия К2Cr2O7 или перманганата калия КМnО4) в серной кислоте Н2SO4. В качестве окислителя можно использовать оксид меди (II) СuО при нагревании.
При окислении первичных спиртов образуются альдегиды:
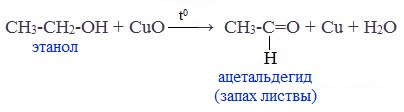
При окислении вторичных спиртов образуются кетоны:
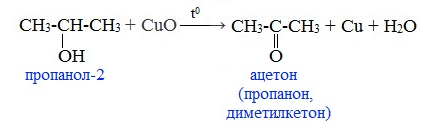
При окислении первичного спирта дихроматом калия в кислой среде при нагревании образуется карбоновая кислота, а на холоду- альдегид:
3С2Н5ОН+ К2Cr2О7 +4Н2SО4→3СН3СНО + Cr2(SО4)3 +К2SО4 +7Н2О
На изменении цвета соединений хрома также основана работа алкотестеров, когда пары спирта, содержащиеся в выдыхаемом водителем воздухе, восстанавливают дихромат в стеклянной трубочке.

Вторичные спирты образуют при окислении в основном кетоны.
3СН3СНОНСН3 + К2Cr2О7 +4Н2SО4→3СН3СОСН3 + Сr2(SО4)3 + К2SО4+7Н2О
Промышленные способы.
Каталитическое окисление алкенов кислородом воздуха
Этим способом в промышленности получают уксусный альдегид — окислением этилена кислородом воздуха (Вакер-процесс).
Эта реакция протекает в присутствии катализатора – смеси PdCl2 и CuCl2 и температуре 1000С:
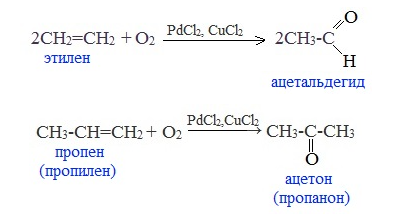
Этим экономичным способом получают низшие альдегиды и кетоны.
Этот промышленный способ более перспективен, чем гидратация алкинов, при которой используются токсичные ртутные катализаторы.
2.Оксосинтез - это присоединение СО и Н2 к олефинам (алкенам) в присутствии кобальтсодержащих катализаторов с образованием альдегидов. Оксосинтез также называют реакцией Релена или гидроформилированием. Данная реакция была открыта в 1938 г. О. Реленом.
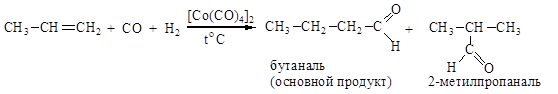
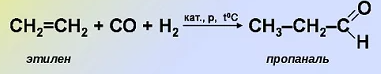
3. Гидратация алкинов (реакция Кучерова)
Присоединение воды к ацетилену происходит в присутствии катализатора соли ртути (II) и идет через образование неустойчивого непредельного спирта (енола), который изомеризуется в уксусный альдегид (в случае ацетилена):
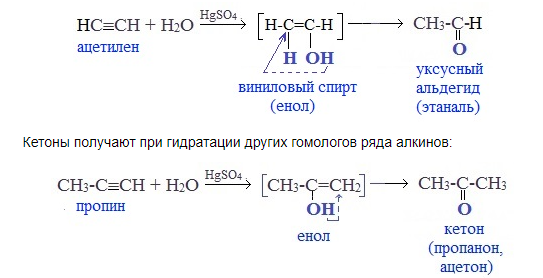
Раньше это был промышленный способ получения карбонильных соединений. В настоящее время этот способ находит ограниченное применение из-за загрязнения получаемых продуктов токсичными солями ртути и относительной дороговизны.
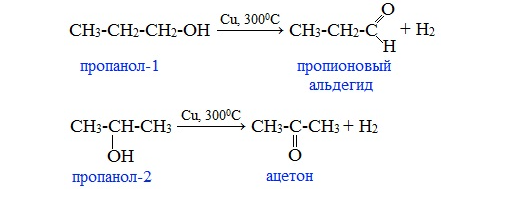
4. В промышленности альдегиды и кетоны получают дегидрированием спиртов, пропуская пары спирта над нагретым катализатором (Cu)
Первичные спирты дегидрируются до альдегидов, а вторичные – до кетонов.
Получение формальдегида
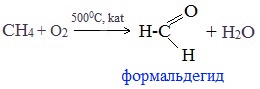
Окисление метана
Формальдегид в промышленности можно получить окислением метана кислородом воздуха при высоких температурах с использованием катализатора (Mn2+или Сu2+)
Окисление метанола
Основной промышленный способ получения формальдегида – окисление метанола с использованием серебряного катализатора при температуре 6500С и атмосферном давлении:
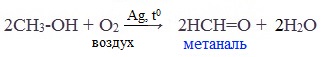
Реакция происходит на раскаленной серебряной сетке, через которую проходят пары ментола, смешанные с воздухом. Реакция настолько экзотермична, что выделяющейся в ходе ее теплоты достаточно для того, чтобы поддерживать сетку в раскаленном состоянии.
В настоящее время разработан перспективный способ высокотемпературного окисления метанола с использованием железомолибденовых катализаторов (Fe-Mo):
