ВВЕДЕНИЕ
Учебная практика по аналитической химии проводится в зале инструментальных методов анализа кафедры неорганической и аналитической химии РГАУ-МСХА им. К.А.Тимирязева с использованием образцов сельскохозяйственной продукции, собранных в ходе учебной практики по другим учебным дисциплинам.
По каждому разделу практики студент готовит письменный отчет, защиту которого проводит в последний день этого раздела практики.
Занятие 1. ПОТЕНЦИОМЕТРИЧЕСКИЙ АНАЛИЗ
Принцип метода. Потенциометрический анализ – раздел аналитической химии, в котором концентрацию определяемого иона находят по величине электродвижущей силы (э.д.с.) гальванического элемента. Любой гальванический элемент состоит из двух полуэлементов – электродов. Э.д.с. гальванического элемента равна разности потенциалов этих электродов.
В потенциометрии один из электродов является индикаторным, а другой – электродом сравнения. Потенциал индикаторного электрода зависит от активности определяемого иона. Потенциал электрода сравнения к изменению активности определяемого иона нечувствителен и имеет постоянное значение. Таким образом, э.д.с. гальванического элемента, составленного из индикаторного электрода и электрода сравнения, задается активностью определяемого иона в растворе.
В потенциометрическом методе анализа существуют два направления: а) потенциометрическое титрование, б) прямая потенциометрия (ионометрия). При потенциометрическом титровании в исследуемый раствор опускают индикаторный электрод и электрод сравнения и регистрируют изменение потенциала этого электрода в зависимости от объема добавляемого титранта. Цель титрования заключается в обнаружении точки эквивалентности. Показателем достижения точки эквивалентности в методе потенциометрического титрования служит резкое изменение потенциала индикаторного электрода (скачок потенциала).
Метод прямой потенциометрии (ионометрии) позволяет определить активность потенциалопределяющего иона в растворе по значению э.д.с. При использовании метода прямой потенциометрии для определения концентрации, а не активности ионов необходимо провести градуирование электрода, т.е. экспериментально определить зависимость потенциала данного электрода от концентрации потенциалопределяющего иона с, используя ряд растворов с известной концентрацией этого иона. При этом вместо величин с для удобства применяют величины p с = - lg с.
Лабораторная работа 1. ИЗУЧЕНИЕ ПРИЕМОВ РАБОТЫС ИОНОМЕРОМ «ЭКОТЕСТ-2000»
Для измерения э.д.с. гальванических элементов используют приборы, которые называют рН-метрами или иономерами. На рис. 1 изображен внешний вид рН-метра – иономера «Экотест-2000». На лицевой панели прибора расположены жидкокристаллический дисплей (1) и клавиатура (2), которая предназначена для оперативной настройки и выбора режима измерения.

Рис. 1. Внешний вид рН-метра – иономера «Экотест-2000»: 1 – жидкокристаллический дисплей; 2 – клавиатура
Клавиатура изображена на рис. 2
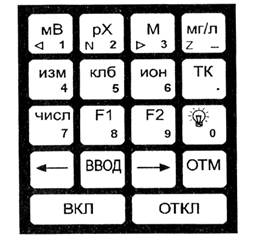
Рис. 2. Клавиатура рН-метра – иономера «Экотест-2000»: назначение клавиш указано в тексте
На задней стенке прибора (рис. 3) расположены разъемы, предназначенные: а) для подсоединения внешнего источника питания, он обозначен надписью ПИТ; б) для подсоединения измерительного электрода (стеклянного или ионоселективного), он обозначен надписью ИЗМ; в) для подсоединения электрода сравнения, он обозначен надписью ВСП; г) для подсоединения термоэлектрического преобразователя, он обозначен надписью Т; д) для подсоединения амперометрического датчика растворенного в воде кислорода с термоэлектрическим преобразователем, он обозначен надписью О2.

Рис. 3. Задняя стенка рН-метра – иономера «Экотест-2000»: обозначения в тексте.
Действие рН-метра – иономера «Экотест-2000» при измерении рН основано на преобразовании электродвижущей силы, возникающей между индикаторным электродом и электродом сравнения, в пропорциональное по величине напряжение, которое преобразуется в цифровой код и аналоговый выходной сигнал, как это показано на структурной схеме прибора (рис. 4).

Рис. 4. Структурная схема рН-метра – иономера «Экотест-2000»: 1 – усилитель входной; 2 – схема измерения температуры; 3 – схема измерения концентрации кислорода; 4 – коммутатор переключения режимов; 5 – аналого-цифровой преобразователь; 6 – микропроцессорная схема; 7 – контур дисплея; 8 – блок управления
Подготовка прибора к работе.
1. Подключить электроды (измерительный и сравнения) к прибору. Электроды поместить в стаканчик с дистиллированной водой.2
2. Включить прибор, нажав кнопку «ВКЛ ».
3. Кнопками «←» и «→» выбрать режим «р Н-метр-иономер»
Измерение рН раствора.
1. Осторожнопогрузить электроды в стаканчик с раствором так, чтобы электроды не касались стенок и дна.
2. Нажать кнопку «ИЗМ».
3. Записать показание прибора, дождавшись стабильного значения в течение 2-3 минут.
4. Нажать кнопку «ОТМ» для выхода из режима измерений.
Помните: в промежутках между измерениями электроды должны быть погружены в дистиллированную воду.
Измерение окислительно – восстановительного потенциала (э.д.с.).
1. Погрузить электроды в стаканчик с исследуемым раствором.
2. Кнопками «←» и «→» выбрать режим «Вольтметр (Eh).
3. Произвести измерение э.д.с.
4. Нажать кнопку «ОТМ» для выхода из режима измерений.
Лабораторная работа 2. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ФОСФОРНОЙ КИСЛОТЫ
Определение фосфорной кислоты основано на ее дифференцированном титровании по двум ступеням:
H3PO4 + NaOH = NaH2PO4 + H2O
NaH2PO4 + NaOH = Na2HPO4 + H2O
Цель работы состоит в определении содержания фосфорной кислоты в контрольном растворе по двум точкам эквивалентности, найденным путем потенциометрического титрования H3PO4 раствором NaOH.
Приборы и оборудование. Потенциометрическое титрование выполняют на магнитной мешалке с вращающимся магнитом, помещенным в стаканчик. Раствор титранта (NaOH) приливают из бюретки при перемешивании титруемого раствора. Измерение рН осуществляют с помощью стеклянного индикаторного электрода, хлорсеребряного электрода сравнения и рН-метра – иономера «Экотест-2000».
Методика определения: 1. В стакан для титрования вместимостью 100 мл внести пипеткой аликвотную часть (10 мл) исследуемого раствора и 20 – 30 мл дистиллированной воды. В полученный раствор погрузить индикаторный стеклянный электрод, хлоридсеребряный электрод сравнения и магнитик для перемешивания. Бюретку заполнить 0,1 н. раствором гидроксида натрия.
2. Провести ориентировочное титрование, приливая раствор титранта порциями по 1 мл и фиксируя рН. Полученные данные внести в табл. 1. Вычитая из каждого последующего значения рН предыдущее, вычислить разности DрН. Самые большие разности DрН укажут на области двух скачков титрования.
Таблица 1. Результаты ориентировочного титрования.
| Объем раствора титранта V (NaOH), мл | pH | ∆pH | Примечание (указать области скачков титрования) |
| 1,00 | |||
| 2,00 | |||
| 3,00 | |||
| 4,00 | |||
| 5,00 | |||
| 6,00 | |||
| 7,00 | |||
| 8,00 | |||
| 9,00 | |||
| 10,00 | |||
| 11,00 | |||
| 12,00 |
3. Провести точное титрование. Для этого после тщательного промывания магнитика и электродов повторить операцию, указанную в пункте 1. Затем прилить из бюретки раствор титранта объемом V 1, который на 1 мл меньше, чем это нужно для достижения области первого скачка титрования, найденной при ориентировочном титровании. Далее прибавлять раствор титранта равными порциями по 4 капли для нахождения точки эквивалентности в области первого скачка титрования (V т.э.1). После достижения резкого изменения рН убедиться в уменьшении и малом изменении DрН, продолжая добавлять титрант порциями по 4 капли. Записать общий объем затраченного титранта V 2 Полученные данные внести в табл. 2. Вычислить разности DрН, объем капли и объемы порций титранта D V, а также отношения ∆рН/∆ V. Для области первого скачка титрования Δ V = 4 V капли1.
Далее прилить раствор титранта объемом V 3, который на 1 мл меньше, чем это нужно для достижения области второго скачка титрования, найденной при ориентировочном титровании и прибавлять раствор титранта равными порциями по 8 капель для нахождения точки эквивалентности в области второго скачка титрования (V т.э.2). После достижения резкого изменения рН убедиться в уменьшении и малом изменении DрН, продолжая добавлять титрант порциями по 8 капель. Записать общий объем затраченного титранта V 4 . Полученные данные также внести в табл. 2. Вычислить разности DрН, объем капли и объемы порций титранта D V, а также отношения ∆рН/∆ V. Для области второго скачка титрования Δ V = 8 V капли2.
Таблица 2. Результаты точного титрования
| Объем раствора титранта V (NaOH), мл | pH | ∆pH | ∆рН/∆ V | Примечание (указать области скачков титрования) |
| В области первого скачка титрования | ||||
| Объем раствора титранта до начала первого скачка V 1, ______ мл | ||||
| 4 капли | ||||
| 8 капель | ||||
| 12 капель | ||||
| 16 капель | ||||
| 20 капель | ||||
| 24 капли | ||||
| 28 капель | ||||
| 32 капли | ||||
| … | ||||
| Объем раствора титранта, V 2,_________ мл | ||||
| В области второго скачка титрования | ||||
| Объем раствора титранта до начала второго скачка V 3, ______ мл | ||||
| 8 капель | ||||
| 16 капель | ||||
| 24 капли | ||||
| 32 капли | ||||
| 40 капель | ||||
| 48 капель | ||||
| … | ||||
| Объем раствора титранта после второго скачка титрования V 4, _______ мл |
4. Построить графики рН – объем титранта и ∆рН/∆ V – объем титранта (рис. 5 и 6 соответственно).

Рис. 5. Интегральная кривая потенциометрического титрования
Рис. 6. Дифференциальная кривая потенциометрического титрования
5. Найти объем раствора титранта, отвечающий первой точке эквивалентности (V т.э.1) и второй точке эквивалентности (V т.э.2 ): а) непосредственно по табличным результатам титрования по каплям; б) из интегральной (график рН – V) и дифференциальной (график ∆рН/∆ V - V) кривых титрования.
6. Рассчитать массу фосфорной кислоты, исходя из первого и второго скачков титрования:
m (H3PO4) = 
где V т.э.– объем раствора титранта, необходимый для достижения точки эквивалентности, мл; с (NaOH) – молярная концентрация эквивалента раствора титранта, моль/л; f экв – фактор эквивалентности фосфорной кислоты; М (Н3РО4) - молярная масса фосфорной кислоты, г/моль; V м.к. – объем мерной колбы с исследуемым раствором (100 мл); V п – объем аликвотной части исследуемого раствора, отмеренный при помощи пипетки (10 мл).
Для первого скачка титрования фактор эквивалентности фосфорной кислоты равен 1, для второго скачка он равен 1/2.