По дисциплине: Физика
Тема: «Исследование теплоемкости металлов»
Выполнил: студент гр. ОНГ-09 _ ____________ / Чебышева А. М./
(подпись) (Ф.И.О.)
Проверил: ассистент _______________ / Быстров Д. С./
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
Цель работы: экспер,0,,,,иментально определить теплоемкость металлов при комнатной температуре и сравнить с теоретическими данными.
Общие сведения:
- Явление, изучаемое в работе:
Теплоемкость тела - это изменение тепловой энергии при изменении температуры тела на один градус.
- Определение основных физических понятий, объектов, величин, процессов и величин:
Удельная теплоёмкость (с) определяется как количество тепловой энергии, необходимой для повышения температуры одного килограмма вещества на один градус. Удельную теплоёмкость можно рассматривать как теплоёмкость единицы массы вещества.

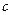 - удельная теплоёмкость,
- удельная теплоёмкость,
 - количество теплоты, полученное веществом при нагреве (или выделившееся при охлаждении),
- количество теплоты, полученное веществом при нагреве (или выделившееся при охлаждении),
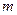 - масса нагреваемого (охлаждающегося) вещества,
- масса нагреваемого (охлаждающегося) вещества,
 - разность конечной и начальной температур вещества.
- разность конечной и начальной температур вещества.
Молярная теплоёмкость (сμ) - это количество теплоты, которую необходимо подвести к 1 молю вещества, чтобы нагреть его на 1 K. Размерность Дж/(К·моль).
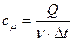
 - количество вещества, моль.
- количество вещества, моль.
Связана с удельной теплоемкостью с того же вещества соотношением:

с - удельная теплоёмкость
М - молярная масса
Объёмная теплоёмкость (сv) - это количество теплоты, которую необходимо подвести к 1 м³ вещества, чтобы нагреть его на 1 K. Размерность Дж/(м³·К).

V – объем вещества, м3
Фонон - квант колебательного движения атомов кристалла. Колебания атомов кристалла благодаря взаимодействию между ними распространяются по кристаллу в виде волн, каждую из которых можно охарактеризовать квазиволновым вектором k и частотой w, зависящей от k:
w = wn( k )
n = 1,2,..., 3 r (r – число атомов в элементарной ячейке кристалла) обозначает тип колебания.
Дебаевская частота (ωD) - максимальная частота фононов, соответствующая колебаниям с длиной волны порядка межатомного расстояния.

υзв –, средней скоростью звуковых волн в кристалле м/с.
а – постоянная кристаллической решетки, м.
Температура Дебая (Θ) — температура, при которой возбуждаются все моды колебаний в данном твёрдом теле. Дальнейшее увеличение температуры не приводит к появлению новых мод колебаний, а лишь ведёт к увеличению амплитуд уже существующих, то есть средняя энергия колебаний с ростом температуры растёт.
Θ = ћωD/k
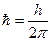
h – постоянная Планка, Дж·с;
ωD - дебаевская частота, Гц;
k – постоянная Больцмана, Дж/К.
Универсальная газовая постоянная численно равна работе расширения одного моля идеального газа в изобарном процессе при увеличении температуры на 1 К. Универсальная газовая постоянная выражается через произведение постоянной Больцмана на число Авогадро:

Na - число Авогадро, моль-1;
k - постоянная Больцмана, Дж/К.
Постоянная Больцмана (k) — физическая постоянная, определяющая связь между температурой и энергией:
1/2 mυ 2 = kT
m - масса молекул газа, кг;
υ - средняя скорость движения молекул газа, м/с;
Т - температура газа (по абсолютной шкале Кельвина), К.
Постоянная Планка (квант действия) — основная константа квантовой теории, коэффициент, связывающий величину энергии кванта электромагнитного излучения с его частотой.
E = hv
E - энергия, переносимая одним квантом, Дж;
v — частота излучения, Гц.
Энергия Ферми (EF) - ферми-уровень, значение энергии, ниже которой все энергетические состояния частиц вырожденного газа, подчиняющихся статистике Ферми – Дирака, при абсолютном нуле температуры заняты. Существование энергии Ферми – следствие Паули принципа, согласно которому в состоянии с определённым импульсом p не может находиться более (2 s + 1) частиц (s – спин частицы). Энергия Ферми совпадает со значениями химического потенциала газа фермионов при Т = 0 К. Положение уровня Ферми зависит от концентрации свободных электронов:
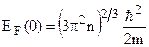
m – масса частицы, кг;
n – концентрация, г/л.
При температурах T>0 К уровень Ферми сдвигается в соответствие с формулой:

k - постоянная Больцмана, Дж/К.
- Законы и соотношения описывающие, описывающие изучаемые процессы, на основании которых получены расчетные формулы:
Закон Дюлонга-Пти
Закон Дюлонга-Пти (Закон постоянства теплоёмкости) — эмпирический закон, согласно которому молярная теплоёмкость твёрдых тел при комнатной температуре близка к 3R:
Cф=3R≈25 Дж/(моль·К)
R – универсальная газовая постоянная, Дж/(моль·К)
Закон Дюлонга и Пти, гласит, что теплоемкость любого твердого тела не зависит от температуры и определяется только числом его атомов в единице объема.
Закон выводится в предположении, что кристаллическая решетка тела состоит из атомов, каждый из которых совершает гармонические колебания в трех направлениях, определяемыми структурой решетки, причем колебания по различным направлениям абсолютно независимы друг от друга. При этом получается, что каждый атом представляет три осциллятора с энергией E, определяемой следующей формулой: E=kT
Формула вытекает из теоремы о равнораспределении энергии по степеням свободы. Так как каждый осциллятор имеет одну степень свободы, то его средняя кинетическая энергия равна K=kT/2, а так как колебания происходят гармонически, то средняя потенциальная энергия равна средней кинетической, а полная энергия - соответственно их сумме. Число осцилляторов в одном моле вещества составляет 3Na, их суммарная энергия численно равна теплоемкости тела - отсюда и вытекает закон Дюлонга-Пти.
Схема установки:

Основные расчетные формулы:
- Теплоемкость металла:

св – удельная теплоемкость воды (Дж/(г·К))
t0кип – температура кипения воды (0С)
ск – теплоемкость калориметра (Дж/К)
t0к1 – температура калориметра до внесения металла (0С)
t0к2 – температура калориметра после внесения металла (0С)
mв – масса воды в калориметре (г)
mМе – масса исследуемого металла (г)
- Масса воды в калориметре:

mст1 – масса металлического стакана из калориметра (г)
mст2 - масса металлического стакана с водой (г)
Формула погрешностей косвенных измерений:
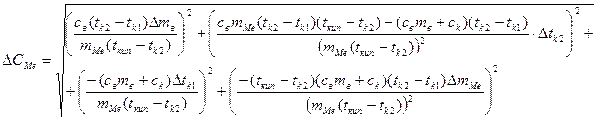
Таблицы с результатами измерений и вычислений:
Таблица 1
| t, мин | tº, ºС | ||
| Al | Fe | ||
| без металла | 23,5 | 23,5 | |
| 23,5 | 23,7 | ||
| 23,5 | |||
| 23,3 | |||
| tºk21 23 | |||
| c металлом | tºk2 27 | ||
| 5,5 | |||
| 6,0 | 29,5 | ||
| 6,5 | 29,4 | ||
| 7,5 | |||
| 28,9 | |||
| 8,5 | 28,5 | ||
| 28,5 | |||
| 9,5 | 30,7 | 28,5 | |
| 30,7 | 28,5 | ||
| 30,5 | |||
Пример вычисления:




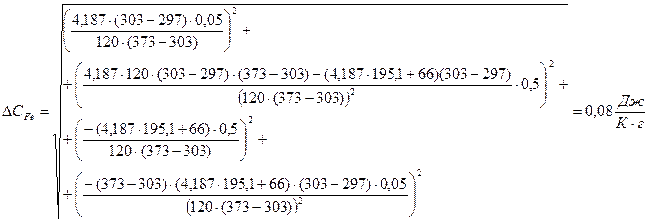


Графики:
1) График зависимости температуры калориметра от времени для Al:

2) График зависимости температуры калориметра от времени для Fe:

Вывод: В данной работе были экспериментально определены теплоемкости металлов при комнатной температуре: 
 . Полученные результаты мы сравнили с теоретическими данными, рассчитанными по закону Дюлонга – Пти:
. Полученные результаты мы сравнили с теоретическими данными, рассчитанными по закону Дюлонга – Пти: 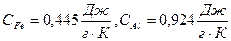 . Наблюдается отклонение экспериментальных величин от теоретических, что связанно с несовершенностью установки и погрешностью измерительных приборов.
. Наблюдается отклонение экспериментальных величин от теоретических, что связанно с несовершенностью установки и погрешностью измерительных приборов.