Практическое занятие
Материльный и конструктивный расчет печи с кипящим слоем для обжига серного колчедана
Серный колчедан(пирит) – один из самых распространенных минералов класса сульфидов, FeS2.
Чистый серный колчедан содержит 53,5% серы и 46,5% железа.
Серный колчедан является основным материалом для получения серной кислоты. Полученную в специальных печах газообразную двуокись серы затем окисляют до SO3, которая абсорбируется водой с образованием серной кислоты. В качестве твердого отхода образуется пиритный огарок.
Пиритные огарки являются ценным сырьем в производстве цемента и в черной металлургии.
Материльный расчет
1. Атомный (мольный) вес химических элементов:
- железо – 55,85 » 56 кг/кмоль;
- сера – 32,07 » 32 кг/кмоль;
- кислород – 16 кг/кмоль.
2. Химическая реакция окисления серного колчедана:
4FeS2 + 11O2= 2Fe2O3 + 8SO2
3. Массовые стехиометрические соотношения по химической реакции:
4*(56+2*32)+11*2*16=2*(2*56+3*16)+8*(32+2*16)
Итого: 480 + 352 = 320 + 512
4. Массы веществ, участвующих в химической реакции:
– серного колчедана M FeS2хим= 480 кг;
– серы в колчедане M Sхим= 256 кг;
– всего кислорода M O2хим= 352 кг;
– кислорода в двуокиси серы M O2газ= 256 кг;
– оксида железа M Fe2Oхим= 320 кг;
– двуокиси серы M SO2хим= 512 кг.
5. Массы веществ, участвующих в химической реакции, с учетом содержания в огарке примеси (X примогар = 0,2) и серы (X Sогар = 0,02):
– огарка M огарфакт= M Fe2Oхим/(1– X примогар– X Sогар)= 320/(1–0,2–0,02)= 410,2 кг;
– примеси M примфакт= M огарфакт* X примогар = 410*0,2= 82 кг;
– серы в огарке M Sогар =M огарфакт* X Sогар =410*0,02= 8,2 кг;
– сухого пирита M пир =M Fe S2хим+ M примогар = 480+82= 562 кг;
– влаги в пирите (u влпир = 0,02): M влпир = M пир * u влпир/(1– u влпир) = 562 * 0,02/(1–0,02) = 11,5 кг;
– двуокиси серы M SO2факт =M SO2хим(M Sхим– M Sогар)/ M Sхим= 512*(256–8,2)/256= 495,6 кг;
– кислорода M O2факт =M O2хим– M O2газ* M Sогар/ M Sхим= 352–256*8,2/256= 343,8 кг.
6. Теоретические массовые расходы на 1 кг сухого пирита:
– огарка g огарфакт = M огарфакт/ M пир= 410,2/562= 0,73 кг/кг пир.;
– кислорода g O2факт = M O2факт/ M пир= 343,8/562=0,61 кг/кг пир.;
– двуокиси серы g SO2факт = M SO2факт/ M пир= 495,6/562= 0,88 кг/кг пир.;
– влаги g влпир= M влпир/ M пир= 11,5/562= 0,02 кг/кг пир.
7. Плотность газообразных соединений при нормальных условиях (T о=273 К):
– кислорода rоO2= M O2мол/ V O2мол= 32/22,4= 1,43 кг/м3 (н.у.);
– диоксида серы rоSO2= M SO2мол/ V SO2мол= 64/22,4= 2,86 кг/м3 (н.у.);
– водяных паров rоH2O= M H2Oмол/ V H2Oмол= 18/22,4= 0,803 кг/м3 (н.у.);
– воздуха rов= 1,293 кг/м3 (н.у.).
8. Теоретические объемы, приходящиеся на 1 кг сухого пирита:
– диоксида серы V оSO2= g SO2факт/rSO2=0,88/2,86= 0,31 м3/кг пир. (н.у.);
– кислорода V оO2= g O2факт/rO2= 0,61/1,43= 0,427 м3/кг пир. (н.у.);
– сухого воздуха V овозд = V оO2/XO2возд = 0,427/0,21= 2,03 м3/кг пир. (н.у.);
– водяных паров V оH2O =(g влпир+0,01 V овозд) /rH2O= (0,02+0,01*2,03)/ /0,803= 0,04 кг/кг пир. (н.у.);
– газообразных продуктов горения V огаз= V оSO2 +V овозд+ V оH2O = =0,31+2,03+0,04= 2,38кг/кг пир. (н.у.).
9. Объемы газообразных компонентов (при избытке воздуха aв=1,05):
– сухого воздуха V возд=aв V овозд= 1,05*2,03= 2,13 м3/кг пир. (н.у.);
– водяных паров V H2O = V оH2O + 0,01 V овозд(aв–1) /rH2O= 0,04+0,01* *2,03 *(1,05–1)/0,803=0,065 м3/кг пир. (н.у.);
– газообразных продуктов горения V газ= V оSO2 +V возд+ V H2O= =0,31+2,13+0,065=2,5 кг/кг пир. (н.у.).
10.Содержание двуокиси серы в газообразных продуктах горения:
X SO2= V оSO2/ V газ = 0,31 / 2,5 = 0,124 м3/ м3 газ. или 12,4 %, что соответствует эксплуатационным данным печей обжига пирита в кипящем слое.
КОНСТРУКТИВНЫЙ РАСЧЕТ
1. Объемный расход воздуха при температуре t в= 20 °С
(сжигается B пир = 14 т/ч = 3,89 кг/с):
V всек= B пир V возд T в/ T =3,89*2,13*(273+20)/273= 8,89 м3/с (н.у.).
2. Кинематический коэффициент вязкости воздуха при температуре t в=20 °С:
nв = 15,2*10–6 м2/с.
3. Плотность воздуха при температуре t в= 20 °С:
rв=rов* T о/ T в =1,293*273/(273+20) = 1,205 кг/м3.
Число подобия Архимеда для частиц огарка в кипящем слое
(при плотности огарка rт=4800 кг/м3, размере частиц d т= 0,4 мм):
Ar=d3rт g/(nв2rв)=(0,4*10–3)3*4800*9,81/((15,2*10–6)2 *1,205)= 10825.
Число подобия Рейнольдса для кипящего слоя
(при порозности e=0,71):
Reо=Ar*e4,75/(18+0,6 (Ar*e4,75)0,5)= 10825*0,714,75/(18+0,6* *(10825*0,714,75)0,5) = 46,582.
6. Фиктивная скорость псевдоожижающего воздуха в кипящем слое:
u o=Re*nв/ d т=46,582*15,2*10–6/0,4*10–3= 1,77 м/с.
7. Расчетный диаметр кипящего слоя в печи обжига пирита:
D сл=(4* V всек/(p u o))0,5=(4*8,89/(p*1,77)) 0,5= 2,23 м.
Расчет паропроизводительности котла-утилизатора по заданным параметрам
Рассчитаем паропроизводительность котла-утилизатора по уравнению теплового баланса: при заданных условиях
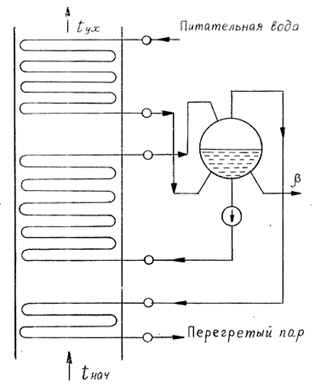
Принципиальная схема котла-утилизатора
Паропроизводительность котла-утилизатора определяется из следующего уравнения теплового баланса:
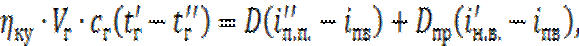
где 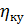 – тепловой кпд котла-утилизатора, по заданию составляет
– тепловой кпд котла-утилизатора, по заданию составляет 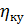 =0,95;
=0,95; 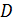 – паропроизводительность котла-утилизатора, т/ч;
– паропроизводительность котла-утилизатора, т/ч; 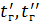 – температуры газов на входе в котел и выходе из котла, по заданию
– температуры газов на входе в котел и выходе из котла, по заданию 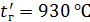 ,
, 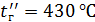 ;
; 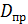 расход воды на продувку котла, принимаем 3% от паропроизводительности котла-утилизатора;
расход воды на продувку котла, принимаем 3% от паропроизводительности котла-утилизатора; 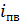 – энтальпия питательной воды, при
– энтальпия питательной воды, при 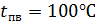 составит
составит 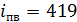
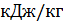 [4, прил. V];
[4, прил. V]; 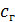 – теплоемкость газов,
– теплоемкость газов,