Нуклеиновые кислоты способны гидролизоваться по трем механизмам: в кислой и щелочной среде, а также в присутствии ферментов. В первом случае гидролиз протекает частично и избирательно. Так, например, при гидролизе ДНК происходит разрыв связей между пуриновыми основаниями и моносахаридом дезоксирибозой и образуется ДНК, в составе которой нет пуриновых оснований.
В щелочной среде нуклеиновые кислоты гидролизуются полностью, но в несколько этапов: нуклеотиды → нуклеозиды → азотистые основания, моносахарид и ортофосфорная кислота.
Ферментативный гидролиз протекает под действием специальных энзимов – нуклеаз. Происходит разрыв конкретных химических связей.
Как известно, большая часть нуклеиновых кислот в клетке связана с белком в форме нуклеопротеинов. Поступающие с пищей нуклеопротеины разрушается панкреатическими ферментами, а нуклеопротеины ткани - лизосомальными ферментами. Вначале происходит диссоциация компонентов нуклеопротеинов на белки и нуклеиновые кислоты. Этому способствует кислая среда желудка. Белки затем включаются в обмен вместе с другими белками пищи, а нуклеиновые кислоты гидролизуются нуклеазами сока железы (РНКазами и ДНКазами), с образованием смеси полинуклеотидов. Далее в процесс включаются полинуклеотидазы и фосфодиэстеразы (эндонуклеазы) кишечника Они довершают гидролиз нуклеиновых кислот до мононуклеотидов. В кишечнике, как правило, образуются 3'-фосфат нуклеотиды, а под влиянием лизосомальных полинуклеотидаз образуются биологически важные 5'- фосфат нуклеотиды. Нуклеотиды гидролизуются нуклеотидазами, с образованием нуклеозидов и Фн. Нуклеозиды, которые обычно рассматриваются как конечный продукт переваривания нуклеиновых кислот в кишечнике, всасываются.
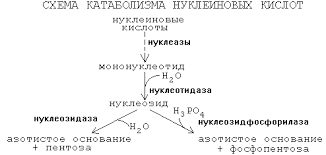
В клетках некоторых тканей, в том числе и клетках кишечника, нуклеозиды подвергаются фосфоролизу нуклеозид фосфорилазами, с образованием оснований и рибозы 1-Ф (или дезоксирибозы 1-P). Рибоза 1-Ф и рибоза 5-Ф в цитозоле находятся в равновесии и могут быть вновь использованы для синтеза нуклеотидов или вступают в неокислительную часть пенозофосфатного пути. Пуриновые и пиримидиновые основания также или распадаются далее до конечных продуктов или используются повторно для синтеза нуклеотидов. В клетке существует интенсивно обмениваемый пул рибонуклеотидов и РНК. Молекулы ДНК и пул дезоксирибонуклеотидов обменивается значительно медленнее. Тканевые пурины и пиримидины, которые не попадают в пути повторного использования, обычно распадаются и продукты их распада выделяются. Используется лишь очень небольшое количество пищевых пуринов, а основная масса поступивших с пищей пуринов распадается. Катаболизм пуринов и пиримидинов не сопровождается значительным высвобождением энергии в сравнении с обменом аминокислот, однако некоторые продукты распада выполняют определенные физиологические функции, например, конечный продукт катаболизма пуринов у человека мочевая кислота, может служить антиоксидантом, продукт катаболизма пиримидина, β– аланин используется в синтезе активных пептидов мозга и мышц. Парэнтеральное введение нуклеотидов и нуклеозидов нашло применение в исследовательской практике. Меченый 3Н –тимидин включается в синтезируемую ДНК без изменений и используется для введения метки в ДНК различных биологических объектов.
Реакции распада мочевой кислоты млекопитающих имеется фермент уратоксидаза которая превращает мочевую кислоту в более растворимый аллантоин. У человека нет такого фермента, и мочевая кислота, кото- рая образуется преимущественно в печени, выделяется почками как конечный продукт обмена пуриновых нуклеотидов. Превращение мочевой кислоты в аллантоин может протекать неферментативно. Эта реакция рассматривается как один из механизмов антиоксидантной защиты клетки у организмов, утративших способность синтезировать аскорбиновую кислоту, а мочевая кислота как важный антиоксидант, заменивший аскорбиновую кислоту. У некоторых животных аллантоин может распадаться далее до мочевины или аммиака. От нуклеотидов к основаниям. Гуаниновые нуклеотиды гидролизуются с образованием гуанозина, который подвергается фосфоролизу до гуанина и рибоза 1-Ф. Гуанин дезаминируется гуанин дезаминазой с образованием ксантина. Аденозин также можно получить по такому пути, однако внутриклеточные нуклеотидазы у человека не очень активны по отношению к AMФ. АМФ чаще дезаминируется ферментом аденилат (AMФ) дезаминазой с образованием ИМФ. Последний далее гидролизуется нуклеотидазой с образованием инозина и после фосфоролиза превращается в гипоксантин. Некоторое количество аденозина образуется из S -аденозилметионина в процессах переметилирования. Аденозин дезаминируется до инозина аденозин дезаминазой. Недостаточность аденозин дезаминазы или пуриновой нуклеозид фосфорилазы ведет к двум различным болезням иммунодефицита механизмами, которые до конца не раскрыты.
При недостаточности аденозин дезаминазы, страдают T и B-лимфоциты, а при недостаточности фосфорилазы нарушается функция T клеток, а B клетки остаются нормальными. В сентябре 1990 г была успешно применена генинженерная технология для лечения 4-летней девочки с недостаточностью аденозин дезаминазы. Катаболизм метилированных (минорных) пуринов зависит от расположения метильной группы. Если метильная группа связана с группой -NH2, она удаляется вместе с -NH2, и оставшаяся часть обменивается в дальнейшем обычным способом. Если метил связан с атомом азота гетероцикла, соединение выделяется в неизменном виде с мочой. От оснований к мочевой кислоте И адениновые и гуаниловые нуклеотиды превращаются в одно общее промежуточное соединение ксантин. Гипоксантин, возникающий из аденина, окисляется в ксантин ксантиноксидазой. Гуанин дезаминируется с образованием аммиака и ксантина. Образующийся аммиак переносится к печени в составе глутамина, где используется для синтеза мочевины. Ксантин, подобно гипоксантину, окисляется кислородом и ксантиноксидазой в мочевую кислоту с образованием перекиси водорода. У человека, мочевая кислота выделяется, а перекись водорода разрушается каталазой. Высокая активность ксантиноксидазы обнаруживается только в клетках печени и кишечника.