1. Процесс растворения представляет собой
а) Химический процесс
б). Физико-химический процесс
в) Механическое смешивание
2.Растворимость газа в жидкости характеризуется:
а. коэффициентом абсорбции
б. коэффициентом адсорбции
в. коэффициентом растворимости
Начало формы
3. Метод исследования разбавленных растворов, основанный на сравнении температуры начала кипения раствора и температуры кипения растворителя при постоянном давлении
калориметрия
криоскопия
осмометрия
тензиметрия
эбуллиоскопия
фотометрия
Конец формы
Начало формы
4. Метод исследования разбавленных растворов, основанный на измерении избыточного давления, прилагаемого к раствору и останавливающего самопроизвольный переход молекул растворителя через полупроницаемую мембрану в раствор
калориметрия
криоскопия
осмометрия
тензиметрия
эбуллиоскопия
фотометрия
Конец формы
Начало формы
5. Повышение температуры начала кипения разбавленного раствора нелетучего растворенного вещества в летучем растворителе по сравнению с температурой кипения растворителя выражается формулой
ΔT = iEm.
Буквой m в этой формуле обозначена
масса растворителя
масса растворенного вещества
масса раствора
молярная концентрация растворенного вещества
моляльная концентрация растворенного вещества
число моль растворенного вещества в растворе
Конец формы
Начало формы
6. Утверждения, справедливые для эбуллиоскопической константы
| зависит только от свойств растворителя; |
| зависит от свойств растворителя и растворенного вещества; |
| зависит от свойств растворителя и концентрации раствора; |
| зависит от температуры и концентрации раствора; |
| увеличивается с ростом соотношения удельной теплоты испарения к квадрату температуры кипения; |
| уменьшается с ростом соотношения удельной теплоты испарения к квадрату температуры кипения |
Конец формы
Начало формы
7. Криоскопические константы для бензола и воды равны соответственно 5,12 и 1,86 К•кг/моль. Молекула вещества в водном растворе полностью диссоциирует на две частицы, а в бензоле не диссоциирует и не ассоциирует. Укажите, во сколько раз будут различаться понижения температуры начала отвердевания разбавленного раствора одного и того же вещества в бензоле и в воде при одинаковых моляльных концентрациях.
(Ответ введите числом, округленным до десятых)
Введите ответ:.............................
Конец формы
Начало формы
8. Изотонический коэффициент Вант-Гоффа это поправка, учитывающая
| увеличение равновесного давления пара над чистым растворителем при нагревании; |
| непостоянство давления при нагревании или охлаждении раствора; |
| различие молярных масс растворителя и растворенного вещества; |
| изменение числа частиц в растворе при диссоциации или ассоциации молекул; |
| изменение плотности раствора при диссоциации или ассоциации молекул; |
| изменение изотопного состава молекул растворенного вещества |
Конец формы
Начало формы
9. Вычислите изотонический коэффициент Вант-Гоффа для разбавленного водного раствора некоторого вещества, если молекула вещества диссоциирует в растворе на две частицы и степень диссоциации составляет 60%.
(Ответ введите числом, округленным до десятых)
Введите ответ:.............................
Конец формы
Начало формы
10. Известно, что практически все молекулы бензойной кислоты, растворенной в бензоле, ассоциированы в димеры. Вычислите изотонический коэффициент Вант-Гоффа для разбавленного раствора бензойной кислоты в бензоле.
(Ответ введите числом, округленным до десятых)
Введите ответ:
 .............................
.............................
Конец формы
Начало формы
11. Выберите выражение, которое может использоваться для определения кажущейся молярной массы растворенного вещества криоскопическим методом
 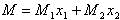
|  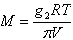
|
 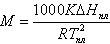
|  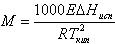
|
 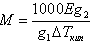
|  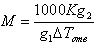
|
Конец формы
Начало формы
12.Выражение, которое может использоваться для определения кажущейся молярной массы растворенного вещества по результатам измерений осмотического давления
 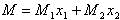
|  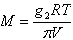
|
 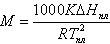
|  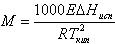
|
 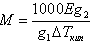
|  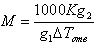
|
Конец формы
13.Масса газа, растворенного в заданном объеме жидкости, с которой газ находится в равновесии при определенной температуре, пропорциональна давлению газа
а. закон Рауля
б. закон Генри
в. закон Ландсберга
14. Понижение температуры замерзания и повышение температуры кипения – это закон:
а. Вант-Гоффа
б. Первый закон термодинамики
в. Второй закон Рауля
15. В уравнении P = iCRT, поправка i для электролитов носит название:
а. Коэффициент изменения
б. Электролитический коэффициент
в. Изотонический коэффициент
в. несмешивающаяся жидкость
16.Осмотическое давление двух растворов при одинаковой температуре относятся между собой как понижение температур их:
а. кипения
б. замерзания
17.Зависимость растворимости газа от давления выражается:
а. законами Генри-Дальтона
б. законами Рауля
в. законами Коновалова
18.Насыщенный раствор одновременно:
а. может быть разбавленным
б.не может быть концентрированным
в. не может быть разбавленным
г. может быть ненасыщенным