Во всех рассуждениях о образовании ковалентных связей и геометрической структуре молекул по методу валентных связей был обойден вопрос: что заставляет атомы образовывать ковалентные связи? Для этого необходимо обратиться к рассмотрению энергии.
В атомах электроны (ē) существуют в разрешенных энергетических состояниях – на А томных О рбиталях.
Аналогично в молекулах ē существуют в разрешенных энергетических состояниях, которые называются М олекулярными О рбиталями и, т.к. молекулы сложнее атомов, то => МО сложнее АО.
Большей предсказательной силой обладает метод молекулярных орбиталей (ММО), где:
-молекула рассматривается как единая система ядер и электронов;
- электроны находятся в общем пользовании всех ядер атомов, образующих молекулу;
Таким образом, метод МО химическую связь рассматривает как многоцентровую и многоэлектронную. В этом случае для приближенного решения уравнения Шредингера волновая функция пси ψ, соответствующая МО, задается как линейная комбинация АО, т. е. как сумма и разность атомных волновых функций с вариационными коэффициентами (с1, с2), определяющими долю участия АО в построении МО или указывающими на долю их вклада в перекрывание электронных облаков.
При сложении АО образование МО: ψ+ = с1 ψ1 + с2 ψ2,
При вычитании АО образуется МО: ψ- = с3 ψ1 – с4 ψ2.
МО также, как и АО характеризуются квантовыми числами:
n главным, l побочным, ml магнитным, определяющими их энергию, число и ориентацию в пространстве: АО - s p d f, МО - σ π δ φ.
Полученный метод получил название Линейной Комбинации Атомных Орбиталей (ЛКАО МО). В методе ЛКАО МО для образования устойчивой молекулярной орбитали необходимо, чтобы
1) энергии атомных орбиталей были близки друг к другу;
2) чтобы их симметрия не сильно отличалась. При выполнении этих 2х требований коэффициенты c1 и c2 должны быть близкими по своим значениям, а это, обеспечивает мак симальное перекрывание АО.
Если образуется МО, энергия которой понижается относительно энергий АО, то такая МО называется связывающей. Волновая функция, соответствующая связывающей МО, получается в результате сложения волновых функций с одинаковым знакомψ+ = с1ψ1 + с2ψ2. Электронная плотность при этом концентрируется между ядрами, и волновая функция принимает положительное значение.
При вычитании волновых функций ψ- = с3ψ1 – с4ψ2 энергия МО повышается. Эта орбиталь называется разрыхляющей. Электронная плотность в этом случае располагается за ядрами, а между ними равна нулю. Волновая функция в двух образовавшихся электронных облаках имеет противоположные знаки, что хорошо видно из схемы образования связывающей и разрыхляющей орбиталей, приведенной на (презентация рис. 24,25):
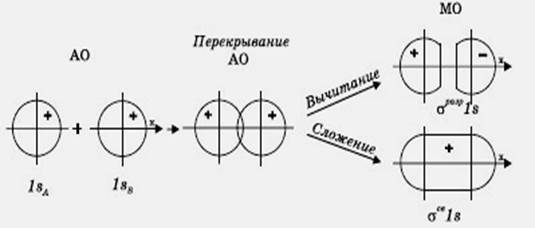
Рис. 24. Схема образования связывающей и разрыхляющей молекулярных орбиталей.
Когда АО (презентация рис.26) одного из атомов вследствие большой разницы в энергии или симметрии не может взаимодействовать с АО другого атома, она переходит в энергетическую схему МО молекулы с энергией, соответствующей ей в атоме. Орбиталь этого типа называется несвязывающей.
Классификация орбиталей на σ или π (презентация рис.27, 28) производится в соответствии с симметрией их электронных облаков аналогично σ - и π -связям в методе валентных связей:
σ-орбиталь имеет такую симметрию электронного облака, при которой поворот ее вокруг оси, соединяющей ядра, на 1800 приводит к орбитали, по форме не отличимой от первоначальной. Знак волновой функции при этом не меняется;
π -орбитали - при повороте ее на 1800 знак волновой функции меняется на противоположный.
Отсюда следует, что
s-электроны атомов при взаимодействии между собой могут образовывать только σ -орбитали,
а три p-орбитали атома – одну σ- и две π -орбитали, причем σ –орбиталь возникает при взаимодействии pХ атомных орбиталей, а π -орбиталь – при взаимодействии pY и pZ. Молекулярные π -орбитали повернуты относительно межъядерной оси на 900. Здесь наблюдается полная аналогия с методом валентных связей (презентация рис.29).

Рис. 29. Схема образования связывающих и разрыхляющих МО
для 2р-атомных орбиталей.
Для того чтобы отличать связ ывающие и разр ыхляющие орбитали друг
от друга, а также их происхождение, принята следующая система обозначений. Связывающая орбиталь обозначается сокращением «св», располагающимся справа вверху после греческой буквы, обозначающей орбиталь, а разрыхляющая – соответственно «разр».
Принято еще одно обозначение: звездочкой * помечаются разрыхляющие орбитали, а без звездочки – связывающие. После обозначения МО пишется обозначение АО, которой молекулярная обязана своим происхождением, например, πразр2pу. Это означает, что молекулярная орбиталь π-типа, разрыхляющая, образовалась при взаимодействии 2 pу -атомных орбиталей (рис. 29):
При рассмотрении электронного строения молекулы с точки зрения метода молекулярных орбиталей (ММО) нужно руководствоваться следующими правилами:
1. Электроны в молекуле, как и в атоме, занимают соответствующие
орбитали, которые характеризуются своим набором квантовых чисел;
2. Число образующихся МО равно числу исходных АО;
3. Энергии связывающих МО ниже энергий АО, а энергии разрыхляющих МО – выше энергий АО, принимающих в образовании связей.
4. Электроны размещаются на МО согласно принципу наименьшей энергии (прав. Клечковского), принципу Паули, правилу Гунда.
5. Химическая связь между атомами образуется, если число электронов на связывающих МО больше числа электронов на разрыхляющих МО.
6. Для молекул, образованных атомами одного химического элемента
(гомоядерных), выигрыш в энергии за счет образования связывающей МО компенсируется повышением энергии разрыхляющей МО.
На энергетической диаграмме обе орбитали располагаются симметрично
относительно атомных орбиталей (презентация рис.32, 33):
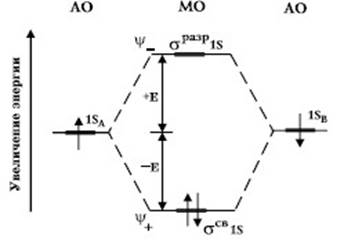
Рис. 33. Энергетическая диаграмма молекулярных орбиталей
для гомоядерных молекул (на примере молекулы водорода)
7. Для молекул, образованных разноэлементными атомами (гетероядерных), связывающие орбитали по энергии ближе к орбиталям более электроотрицательного атома (B), а разрыхляющие – ближе к орбитали менее электроотрицательного атома (A). Разность в энергиях исходных атомных орбиталей (отрезок b) равна ∆ полярности связи, эта разность является мерой ионности связи. Разность в энергиях между связывающей орбиталью и атомной орбиталью (отрезок с) более электроотрицательного атома определяет ковалентность связи. (презентация рис.34):

Рис. 34. Энергетическая диаграмма молекулярных орбиталей
для гетероядерной молекулы.
8. Кратность химической связи равна половине разности числа электронов, расположенных на связывающих орбиталях, и числа электронов на разрыхляющих: n = ½ (Nсвяз. – Nразр).
При описании молекулы по ММО будем придерживаться следующего плана (презентация рис. 35):
• 1. Определить, какие АО перекрываются и образуют МО
• 2. Построить энергетическую диаграмму МО молекулы (иона)
• 3. Распределить электроны по МО в соответствии с принципом наименьшей энергии, принципом Паули и правилом Гунда
• 4. Рассчитать порядок связи и оценить устойчивость молекулы (иона)
• 5. Предположить магнитные свойства молекулы (иона)
• 6. Сравнить энергию ионизации молекулы (иона) и исходных атомов
• 7. Спектральные свойства молекулы (иона)
Для примера разберем энергетические диаграммы и электронное строение гетероядерных и гомоядерных молекул и ионов, образованных двумя атомами элементов первого и второго периодов Периодической системы.
У элементов первого периода (презентация рис.36) валентной орбиталью является 1s- орбиталь. Эти две атомных орбитали образуют две σ-молекулярные орбитали – связывающую и разрыхляющую.
| Молекулярные параметры | Молекулы и молекулярные ионы | |||
| МО | Н+2 | Н2 | Не+2 | Не2 |
| σ* | ― | ― | ↓ | ↓↑ |
| σсв | ↓ | ↓↑ | ↓↑ | ↓↑ |
| E св, кДж∙моль–1 | ||||
| Длина связи, r 0, нм | 0,106 | 0,075 | 0,108 | Молекула не образуется нет выигрыша в энергии |
| Порядок связи n= | 0,5 | 0,5 | ||
| Электронная формула | σсвяз1s1 | σсвяз1s2 | σсвяз1s2 σразр1s1 | σсвяз1s2 σразр1s2 |
| Магнитные свойства | Парамагнит ные | Диамагнит ные | Парамагнит ные | - |
Рассмотрим электронное строение молекулярного иона Н2+. Он имеет один электрон, который будет занимать более энергетически выгодную s-связывающую орбиталь. В соответствии с правилом подсчета кратности связи n= 0,5, а так как в ионе имеется один неспаренный электрон, Н2+ будет обладать парамагнитными свойствами. Электронное строение этого иона запишется по аналогии с электронным строением атома так: σсвяз1s1.
Появление второго электрона на s-связывающей орбитали приведет к энергетической диаграмме, описывающей молекулу водорода Н2, возрастанию кратности связи до единицы и диамагнитным свойствам. Возрастание кратности связи повлечет за собой и увеличение энергии диссоциации молекулы H2 и более короткому межъядерному расстоянию по сравнению с аналогичной величиной у иона водорода. Электронное строение H2 можно записать так: σсвяз1s2.
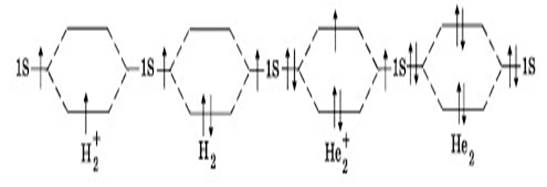
Энергетические диаграммы элементов I периода (презентация рис.34)
Двухатомная молекула He2 существовать не будет, так как имеющиеся у двух атомов гелия четыре электрона расположатся на связывающей и разрыхляющей орбиталях, что приводит к нулевой кратности связи. Но в то же время ион He2+ будет устойчив и кратность связи в нем равна 0,5. Так же, как и ион водорода, этот ион будет обладать парамагнитными свойствами.
У элементов второго периода (презентация рис.37)появляются еще четыре атомных орбитали: 2s, 2pХ, 2pY, 2pZ, которые будут принимать участие в образовании молекулярных орбиталей.
Различие в энергиях 2s- и 2p-орбиталей велико, и они не будут взаимодействовать между собой с образованием молекулярных орбиталей. Эта разница в энергиях при переходе от первого элемента к последнему будет увеличиваться. В связи с этим обстоятельством электронное строение двухатомных гомоядерных молекул элементов второго периода будет описываться двумя энергетическими диаграммами (презентация рис.38), отличающимися порядком расположения на них σсвяз2pх и πсв2py,z электронов.
При относительной энергетической близости 2s- и 2p-орбиталей, наблюдаемой в начале периода, включая атом азота, электроны, находящиеся на σразр2s- и σсвяз2pх-орбиталях, взаимно отталкиваются. Поэтому πсвяз2py и πсвяз2pz -орбитали оказываются энергетически более выгодными, чем σсвяз2pX -орбиталь. На рис. 38 представлены обе диаграммы.
Так как участие 1s-электронов в образовании химической связи незначительно, их можно не учитывать при электронном описании строения молекул, образованных элементами второго периода.
Представленные на рис. 38 энергетические диаграммы, подтвержденные спектроскопическими данными, показывают следующий порядок размещения молекулярных орбиталей с увеличением энергии от Li2 до N2 включительно:
а) а от O2 до F2:
σсвяз1s< σразр1s << σсвяз2s< σразр2s << σсвяз2pX < πсвяз2pУ = πсвяз2pz < πразр2pУ < πразр2pz << σразр2pX.
б) от Li2 до N2 включительно:
σсвяз1s< σразр1s << σсвяз2s < σразр2s < πсвяз2pУ = πсвяз2pz < σсвяз2pX < πразр2pУ < πразр2pz << σразр2pX;
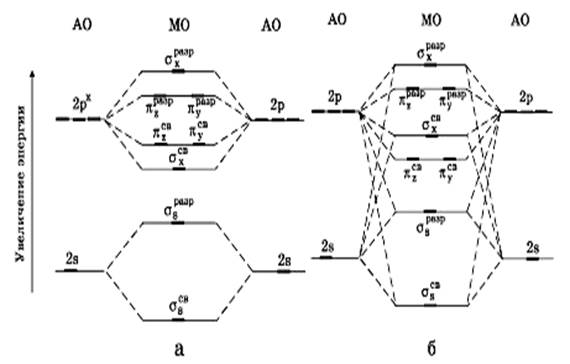
Рис. 38. Энергетические диаграммы уровней двухатомных молекул
при значительном и незначительном энергетическом различии атомных 2s- и 2p-орбиталей.
Второй период системы открывают литий и бериллий, у которых внешний энергетический уровень содержит лишь s-электроны.
Энергетические диаграммы элементов второго периода (презентация рис.39, 41) от Li доF.
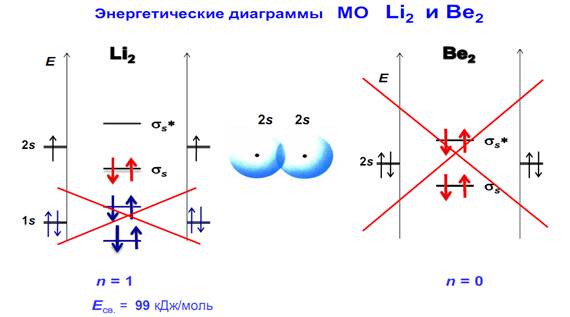
Для этих элементов схема молекулярных орбиталей ничем не будет отличаться от энергетических диаграмм молекул и ионов водорода и гелия, с той лишь разницей, что у последних она построена из 1s-электронов, а у Li2 и Be2 –из 2s-электронов. 1s-электроны лития и бериллия можно рассматривать как несвязывающие, т. е. принадлежащие отдельным атомам. Здесь будут наблюдаться те же закономерности в изменении порядка связи, энергии диссоциации и магнитных свойств. Ион Li2+ имеет один неспаренный электрон, расположенный на σсвяз2s -орбитали – ион парамагнитен. Появление второго электрона на этой орбитали приведет к увеличению энергии диссоциации молекулы Li2 и возрастанию кратности связи с 0,5 до 1. Магнитные свойства приобретут диамагнитный характер. Третий s-электрон расположится на σразр2s -орбитали, что будет способствовать уменьшению кратности связи до 0,5 и, как следствие этого, понижению энергии диссоциации. Такое электронное строение имеет парамагнитный ион Be2+. Молекула Be2, так же как и He2, существовать не может из-за нулевого порядка связи. У этих молекул число связывающих электронов равно числу разрыхляющих!

Дальнейшее заполнение молекулярных энергетических уровней для
двухатомных гомоядерных молекул и некоторых ионов элементов второго
периода показано на (презентация рис. 40,42,43). Как видно из рисунка 40, по мере заполнения связывающих орбиталей энергия диссоциации молекул увеличивается, а с появлением электронов на разрыхляющих орбиталях уменьшается. Ряд заканчивается нестабильной молекулой Ne2. Из рисунка также видно, что удаление электрона с разрыхляющей орбитали приводит к повышению кратности связи и, как следствие этого, увеличению энергии диссоциации и уменьшению межъядерного расстояния. Ионизация молекулы, сопровождаемая удалением связывающего электрона дает прямо противоположный эффект.
Электронные формулы 2х атомных молекул элементов второго периода:
Сравним энергетические диаграммы следующих двух пар молекул и
ионов: О2+, О2, N2+, N2, приведенные на (презентация рис.40):

Рис. 40. Энергетические диаграммы двухатомных молекул и ионов
элементов второго периода Периодической системы.
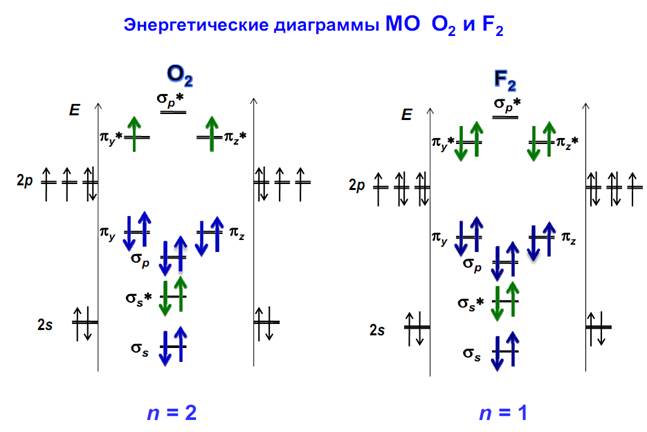
Энергии сконструированных молекулярных орбиталей могут быть определены по данным спектров поглощения веществ в ультрафиолетовой области. Так, среди молекулярных орбиталей молекулы кислорода, образовавшихся в результате перекрывания p -АО, две π связ ывающие вырожденные (с одинаковой энергией) орбитали обладают меньшей энергией, чем σ-связ ывающа я, впрочем, как и π*-разр ыхляющие орбитали обладают меньшей энергией в сравнении с σ*- разр ыхляющей орбиталью

|
| Энергетическая диаграмма, иллюстрирующая с помощью метода МО ЛКАО парамагнитные свойства молекулы O2 |
В молекуле O2 два электрона с параллельными спинами оказались на двух вырожденных (с одинаковой энергией) π*-разрыхляющих молекулярных орбиталях. Именно наличием неспаренных электронов и обусловлены парамагнитные свойства молекулы кислорода, которые станут заметными, если охладить кислород до жидкого состояния (презентация рис. 44)..
Гетероядерные молекулы. При описании энергетических диаграмм МО гетероядерных молекул следующие правила (презентация рис. 45):
1. Исходные АО дают разный вклад в Есвяз. и Еразр. МО.
2.Число МО = числу АО; число связ. МО = число разр. МО = число АО того атома, у которого их меньше.
3. Эффективно перекрываются АО, энергия которых отличается не более, чем на 20эВ.
4. Эффективно перекрываются АО, симметрия которых относительно межъядерной оси одинаковая.
5. АО, не участвующие в эффективном перекрывании, переходят в несвязывающие МО без изменения энергии.
Из двухатомных молекул самой прочной является молекула азота, кратность связи в которой равна трем. Логично предположить, что у гетероядерных молекул и однозарядных ионов, имеющих одинаковое число электронов с N2 – (14=7+7), – кратность связи будет такой же.
Молекулы, имеющие одинаковое число электронов на одинаковых орбиталях, называются изоэлектронными (презентация рис. 46).
Такими молекулами являются CO, BF, BeNe и ионы CN-, NO+, CF+, BO-(презентация рис. 47). По аналогии с молекулой азота они должны обладать высокими значениями энергий диссоциации. Такой вывод нетрудно сделать, распространяя схему МО гомоядерных молекул на гетероядерные.
При этом надо учитывать, что s- и p-орбитали с увеличением заряда ядра понижают свою энергию, а расщепление между ними по энергии растет. Диаграмма (Шрайвер, Эткинс презентация рис. 43).
Вследствие этого появляются существенные отличия в образовании молекулярных орбиталей у некоторых гетероядерных молекул от гомоядерных. Проиллюстрируем это утверждение на примере иона NO+ и
молекулы CO.

Рис. 47. Энергетические диаграммы для иона NO+ (a) и молекулы СО (б).
Поскольку заряды ядер атомов азота(+7) и кислорода(+8) отличаются на единицу, существенного отличия в энергиях их атомных орбиталей не наблюдается и схема МО иона NO+ будет аналогична схеме МО молекулы азота N2 (рис. 47а).
Все р-орбитали атома кислорода (+8) по энергии расположены ниже, чем соответствующие атомные орбитали атома углерода (+6), т. к. заряд ядра кислорода на две единицы больше (Шрайвер, Эткинс презентация рис. 43). Результатом этих энергетических различий будет существенное отличие молекулярных орбиталей СО оксида углерода от молекулярных орбиталей иона NO+ (рис. 47б).
2s-орбиталь (презентация рис. 48). кислорода располагается значительно ниже 2s-орбитали углерода, следствием чего является их слабое взаимодействие, приводящее к образованию слабосвязывающей σсв-орбитали, энергия которой практически не отличается от атомной 2s-орбитали кислорода. В то же время энергии 2p-орбиталей кислорода и 2s-орбитали углерода близки. Эта близость приводит к образованию двух σсв-связывающий и σразр-разрыхляющей орбиталей. Если верхняя занятая σ-орбиталь в ионе NO+ обладает ярко выраженным связывающим характером, то в молекуле CO эта орбиталь является слаборазрыхляющей. Поэтому ион СО+ имеет энергию диссоциации несколько большую, чем молекула СО. Образование других перечисленных выше молекул и ионов сомнительно, т. к. в них энергетические различия еще больше, чем у СО.
На слайдах 49, 50, 51презентации представлены молекулы LiF, HF, проанализируйте их образование.
Метод МО ЛКАО можно использовать не только для двухатомных молекул, но и для многоатомных. Разберем в качестве примера в рамках данного метода строение молекулы NH3 аммиака (презентация рис. 52).
Поскольку три атома водорода имеют только три 1 s -орбитали, то суммарное число образованных молекулярных орбиталей будет равно шести (три связывающих и три разрыхляющих). Два электрона атома азота окажутся на несвязывающей молекулярной орбитали (неподеленная электронная пара НЭП).
Металлическая связь. В отличие от ионных и ковалентных соединений металлы отличаются высокой электропроводностью и теплопроводностью. Высокая электропроводность металлов указывает на то, что электроны свободно могут передвигаться во всем его объеме. Иными словами металл можно рассматривать как кристалл, в узлах решетки которого расположены ионы, связанные электронами, находящимися в общем пользовании, т. е. в металлах имеет место сильно нелокализованная химическая связь. Совокупность электронов, обеспечивающих эту связь, называют электронным газом.
Более общий подход к представлению об ионных, ковалентных и металлических кристаллах можно получить, применяя представления метода молекулярных орбиталей к ним. Предположим, что твердое тело представляет из себя единую молекулу, образованную большим числом атомов. Внешние орбитали этих атомов при взаимодействии образуют связывающие и несвязывающие молекулярные орбитали. Энергетическая зона, образованная связывающими молекулярными орбиталями, называется валентной зоной. Зона, объединяющая несвязывающие орбитали, называется зоной проводимости. Энергетические различия электронов в пределах зоны малы, и изменение их энергии в зоне можно представить как непрерывную полосу энергии. Между зоной проводимости и валентной зоной отсутствуют какие-либо уровни энергий. Поэтому там электроны находиться не могут. Энергетическая зона, разделяющая валентную зону и зону проводимости, носит название запрещенной.

Рис. 23. Энергетические зоны в кристалле, образованные атомными орбиталями.
Электропроводность в твердом теле обеспечивается преодолением электронами запрещенной зоны, т. е. протекание электрического тока обеспечивается переходом электронов из валентной зоны в зону проводимости. В зависимости от ширины запрещенной зоны все твердые тела можно разделить на три класса: диэлектрики, полупроводники и проводники-металлы. Для изоляторов ширина запрещенной зоны составляет более 3 электронвольт, для полупроводников она лежит в пределах от 0,1 до 3 эВ. В металлах вследствие перекрывания валентной зоны и зоны проводимости запрещенная зона практически отсутствует