Занятие 1.1.2.
«Сопряжение как фактор, определяющий устойчивость биологически активных молекул. Природные структуры, содержащие сопряжённые связи (β-каротин, астаксантин, порфирины, флавоноиды, ароматические и гетероциклические соединения). Электронные эффекты, определяющие формирование реакционных центров в молекулах биоорганических соединений »
Задание 1. Приведите примеры сопряженных систем с открытой цепью (бутадиен-1,3, пентадиен-1,3), α-β-ненасыщенных карбонильных соединений и карбоновых кислот (акролеин, акриловая кислота, бутен-2-овая кислота). Укажите тип сопряжения (π-π или π-р) и графическое изображение электронных эффектов для несимметричных алкадиенов. Приведите реакцию гидратации бетен-2-овой кислоты. Обоснуйте направление реакции на основании распределения электронной плотности.
Задание 2. Напишите формулу цитраля (3,7-диметилоктадиен-2,6-аль), входящего в состав лекарственных средств, применяемых для лечения глаз. Проявляется ли эффект сопряжения в данной системе? Покажите электронные эффекты.
Задание 3. Укажите вид и знак электронных эффектов заместителей в молекуле пиридоксаля – витамина группы В (витамин В6).

Задание 4. Приведите формулы гетероциклов: пиррол, имидазол, пиридин, хинолин.
Укажите, какие из гетероатомов играют роль электронодоноров, какие – электроноакцепторов.
Задание 5. Напишите структуру триптофана (3-β-индолил-2-аминопропановая кислоты).
- установите природу гетероатома в структуре аминокислоты, приведите графическое изображение электронных эффектов всех функциональных групп;
- докажите соответствие триптофана критериям ароматичности.
Занятие 1.1.3.
«Кислотно-основные свойства биоорганических соединений: спиртов, тиолов, аминов, карбоновых кислот»
Задание 1. Дайте определение понятия «кислота» по теории Бренстеда Сравните кислотность следующих пар соединений: этантиол и этанол; 4-нитрофенол и пропанол-2. Обоснуйте свой ответ с позиций теории электронного строения соединений.
Задание 2. Для лечения острых и хронических отравлений применяют БАЛ (британский антилюизит) и сукцимер. Приведите названия этих соединений по систематической номенклатуре.
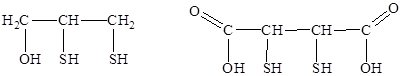
Установите центры кислотности в молекулах этих соединений, какие из них преимущественно определяют кислотность каждого из соединений.
Задание 3.

| В молекуле алкалоида анабазина содержатся два атома азота. Выделите наиболее основный центр в молекуле соединения и приведите строение его соли анабазина с хлороводородной кислотой. |
Задание 4.
 ТИМИН ТИМИН
| Пространственная структура ДНК поддерживается за счет образования водородных связей, которые образуются между комплиментарными парами: аденин-тимин и гуанин-цитозин. Определите основные центры в молекулах тимина и аденина и покажите схему образования водородных связей между ними. |
 АДЕНИН АДЕНИН
|
Задание 5. Дайте определение понятия «основание» по теории Бренстеда. Расположите следующие соединения в ряд по возрастанию основности:
1) пиррол, 2-нитропиррол, пирролидин;
2) анилин, п-аминофенол, п-аминобензойная кислота.
Занятие 1.1.4
«Свойства и биологическая роль карбонильных соединений»
1. Напишите формулу цитраля (3,7-диметилоктадиен-2,6-аль), входящего в состав лекарственных средств, применяемых для лечения глаз. Проявляется ли эффект сопряжения в данной системе? Покажите электронные эффекты.
2. Дайте систематическое название представленным ниже соединениям, в каком из них карбонильная группа обладает большей склонностью к реакциям нуклеофильного присоединения? Объясните свой выбор на основании распределения электронной плотности в молекулах. Напишите схему реакции взаимодействия более реакционноспособного вещества с этиловым спиртом.

3. Какое химическое превращение произойдет с 5-гидроксигексаналем в кислой среде?
4. При заболевании диабетом в организме в результате неполного окисления жиров накапливаются кетокислоты и кетоны. Напишите структуру веществ А и В, а также укажите условия реакций и побочные продукты в следующей цепочке превращений:

5. Написать уравнение реакции альдольной конденсации между N-ацетил-D-маннозамином и пировиноградной кислотой (получение N-ацетил-D-нейраминовой /сиаловой/ кислоты).
Занятие 1.1.5
«Свойства карбоновых кислот и угольной кислоты»
Задание 1. Монокарбоновые кислоты. Важнейшие представители. Электронное строение карбоксильной группы, вид сопряжения. Напишите уравнение реакции уксусной кислоты с метиловым спиртом, аммиаком (при нагревании), гидразином (NH2 - NH2, Н+).
Задание 2. Изобразить формулы биологически активных производных карбоновых кислот: валидола, никотинамида (витамин РР), ацетилхолина, НS-КоА. Напишите реакции изоникотиновой кислоты с этиловым спиртом, аммиаком (при нагревании). Назовите продукты.
Задание 3. Дайте определение кислоты по теории Бренстеда. Качественно сравните кислотность муравьиной, уксусной, трихлоруксусной кислот. Приведите реакции указанных соединений с этанолом (Н+). Назовите полученные продукты.
Задание 4. Сравните между собой электронное строение салициловой и п-аминобензойной кислот. Приведите уравнения реакций указанных кислот со щелочью, уксусным ангидридом.
Задание 5. Напишите синтез ацетилхолина с участием аминоспирта холина и уксусной кислоты. Укажите биологическую роль полученного соединения.
Модульная единица 1.2
Занятие 1.2.1
«Процессы окисления и восстановления биоорганических соединений»
Задание 1. Напишите продукты и механизм гидроксилирования фенилаланина. Какое значение имеют реакции гидроксилирования в организме человека?
Задание 2. Написать продукты в следующей цепочке превращений, назвать их.

( щавелевоуксусная кислота)
Задание 3. Привести реакции окисления - восстановления в системе органических кислот: фумаровая-янтарная; ацетоуксусная – яблочная; пировиноградная - молочная.
Задание 4. Напишите формулу 2-оксобутандиовой (щавелевоуксусной) кислоты, которая является одним из продуктов углеводного обмена. Напишите схему реакции восстановления кислоты и назовите продукт восстановления.
Занятие 1.2.2
«Важнейшие редокс-системы организма»
Задание 1. Приведите схему реакций окисления-восстановления в системе хинон-гидрохинон. Приведите формулы важнейших природных хинонов: убихинона (кофермента Q) и менахинона (витамина К2).
Задание 2. Приведите схему окислительно-восстановительных превращений в системе никотинамидадениндинуклеотид (НАД+ - НАДН). Приведите реакции НАД+- зависимого окисления этилового спирта и молочной кислоты.
Задание3. Привести схему реакции окисления-восстановления в системе изоаллоксазин-дигидроизоаллоксазин, указать фрагмент молекулы, участвующий в передаче протонов и электронов.
Задание 4. Приведите название и структуру основных фрагментов флавинаденинмононуклеотида (ФМН).
Задание 5. Приведите схему реакции НАД+- зависимого окислительного дезаминирования L-глутаминовой кислоты. Назовите продукты реакции.
Занятие 1.2.3
«Роль радикальных процессов. Свободные формы кислорода. Пероксидное окисление липидов биологических мембран.
Ферментативные и неферментативные ингибиторы окисления»
Задание 1. Приведите элементарные реакции инициирования, роста, продолжения и обрыва цепей на примере свободнорадикального окисления олеиновой кислоты. Дайте название радикалам, образующимся в результате этого процесса.
Задание 2. Покажите химизм взаимодействия липидов (RH) с гидроксильными и пероксидными радикалами. Перечислите соединения (антиоксиданты), способные тормозить процесс свободно радикального окисления липидов.
Задание 3. Напишите реакцию уничтожения свободных радикалов с участием важнейшего фенольного биоантиоксиданта (a-токоферола).
Задание 4. Представьте механизм образования активных форм кислорода (О2 ·, ОН·, О2 *, Н2О2). Какие ферменты способны разрушать пероксид водорода и гидропероксиды?
Задание 5. В состав активного центра глутатионпероксидазы входит трипептид глутатион. Изобразите его структуру и приведите химизм реакции глутатиона с пероксидом водорода.
Задание 6. Соотнесите перечисленные ниже соединения к системам ферментативной и неферментативной защиты ПОЛ: супероксиддисмутаза, убихинон, каталаза, глутатионпероксидаза, флавоноиды, липоевая кислота, аскорбиновая кислота.
Занятие 1.2.4
«Электронотранспортные цепи (митохондрий)»
Задание 1. Перечислите последовательно все компоненты дыхательной цепи с указанием стандартных редокс-потенциалов этих биомолекул. Представьте схему тканевого дыхания. Укажите участок цепи, на котором происходит перенос только электронов.
Задание 2. Сколько молекул АТФ синтезируется при переносе пары электронов по клеточной дыхательной цепи.
Задание 3. Назовите цитохром дыхательной цепи, содержащий в своей структуре ионы меди Cu+2/Cu+1.
Задание 4. Сформулируйтехемиосмотическую теорию Митчелла..
Модульная единица 1.3
Занятие 1.3.1.
«Углеводы. Важнейшие полиозы»
Задание 1. Напишите схему образования поли-2-N-ацетилглюкозамина, укажите его значение.
Задание 2. Напишите схему образования амилозы.
Задание 3. Приведите схему образования гиалуроновой кислоты.
Задание 4. Напишите, какие лекарственные препараты и материалы медицинского назначения относятся к углеводам.
Задание 5. Приведите список пищевых продуктов, которые являются источниками углеводов.
Занятие 1.3.2.
«Аминокислоты, пептиды, белки. Классификация и структура белков»
Задание 1. Напишите схему образования глутатиона (γ-Глу-Цис-Гли) и его реакцию с гидропероксидом.
Задание 2. Напишите пептиды, которые могут образоваться при взаимодействии триптофана и α-аланина (in vitro).
Задание 3. Приведите систематическое название пептида с историческим названием везуген (Lis-Glu-Asp). Представьте его структуру в ионизированной форме.
Задание 4. Приведите название ряда структурных белков, укажите их роль.
Задание 5.. Приведите название некоторых транспортных белков. Укажите, какие белки переносят кислород, ионы меди, железа.
Занятие 1.3.3.
«Нуклеиновые кислоты. Циклические нуклеотиды. Модификация структуры нуклеиновых оснований под действием факторов внешней среды.
Антиметаболиты»
Задание 1. Напишите структуру 2-дезоксигуанозин-5/-монофосфата, 2-дезоксицитидин-5/-монофосфата. В структуру ДНК или РНК входят эти соединения.
Задание 2. Напишите взаимодействие аденина и цитозина в структуре ДНК с формальдегидом. Какими могут быть последствия подобной реакции?
Задание 3. Приведите структуру антиметаболитов нуклеиновых кислот (5-фторурацила, 6-меркапторурина). В чем состоит их роль.
Задание 4. Антибиотики 5 поколения содержат антиметаболиты РНК, представляющие собой аналоги аденинозина, у которых вместо рибозы находится арабиноза. Нуклеозид называется арабиноаденозин, который от аденозина отличается тем, что во 2/-положении гидроксигруппа расположена над плоскостью фуранозного цикла. Приведите формулу арабиноаденозина.
Задание 5. Информация о структуре одного из гормонов мозга записана нуклеотидной последовательностью в одной из цепи ДНК, имеющей последовательность: (5/) ATACCGCCTAAATAC (3/). Изобразите последовательность нуклеотидов в другой цепи ДНК с учетом комплементарности нуклеиновых оснований.
Занятие 1.3.4.
«Липиды. Свойства и биологическая роль нейтральных липидов»
Задание 1. Изобразить строение триацилглицерола (триглицерида), включающего пальмитиновую, олеиновую, линоленовую кислоты. Наиболее ненасыщенная кислота находится, как правило, во 2 положении.
Задание 2. Укажите биологическую роль нейтральных липидов.
Задание 3. Покажите на примере олеиновой кислоты различия в строении между природным цис.-изомером и транс-изомером, получаемым, как правило, в результате гидрогенизации (восстановления) жидких масел. Объясните, почему транс-изомеры не проявляют биологического действия и являются для организма балластными соединениями.
Задание 4. Степень ненасыщенности масел и жиров оценивают значением йодного числа, равного количеству г I2, присоединяемого по двойным связям 100 г липидов (г I2/100 г). Значения йодного числа олеиновой (18:1), линолевой (18:2), линоленовой (18:3) кислот равны (89,0 181,0, 274,0) г I2/100 г кислоты, соответственно. Йодное число свиного жира - 42,0, молочного жира – 39,0, у жира муксуна – 123, у жира пеляди (сырка) – 191,0, у жира нельмы 159,0 г I2/100 г. Укажите, какие жиры являются пищевым источником ненасыщенных и полиненасыщенных жирных кислот, расставьте их в ряд по увеличению степени ненасыщенности.
Задание 5. Ряд моющих средств бытовой химии способствуют быстрому омылению жиров, в результате которого образуются водорастворимые продукты, легко смываемые с поверхности посуды.
Напишите реакцию омыления 1,3-О-дистеароил-2-О-линолеил глицерола в слабо щелочной среде КОН, содержащегося в моющем препарате. Назовите продукты.
Занятие 1.3.5.
«Липиды. Фосфолипиды, биологическая роль. Строение биологических мембран»
Задание 1. Изобразить строение фосфатидилхолина, включающего остатки линоленовой и олеиновой кислот с учетом, что наиболее ненасыщенная кислота располагается, преимущественно, во 2 положении.
Задание 2. Приведите химизм гидролиза разбавленным раствором гидроксида натрия приведенных ниже липидов. Назовите продукты.
а) 1-О-пальмитоил-2,3-О-дистеароилоил глицерол
б) 1-О-линолеил-3-О-олеоилглицерол-2-О-эйкозапентаеноил глицерол.
Задание 3. Диолеилфосфатидилхолин относится к ПАВам, широко применяемым в пищевой технологии и косметологии. Приведите формулу этого соединения. Схематично изобразите тип мицелл, образуемых этим соединением в водной среде (например, при производстве йогуртов, кремов) и в масляной среде (например, при производстве майонезов).
Задание 4. Приведите реакцию омыления дистеароилфосфатидилхолина, назовите продукты.
Задание 5. Все природные жирные кислоты представляют собой исключительно цис-изомеры. Транс-изомеры могут накапливаться при длительном хранении продукта, образуются при восстановлении (гидрогенизации) жидких жиров с целью получения более твердых масел (маргарина). Биологической ценности транс-жиры не имеют, необходимо избегать их потребления. Изобразите строение олеиновой и элаидиновой кислот, представляющих собой цис- и транс-изомеры жирной кислоты с индексом 18:1.
Занятие 1.3.6.
«Супрамолекулярные структуры. Липопротеины, липопротеиды. Важнейшие фракции плазмы крови. Биологическая роль. Принципы обеспечения растворимости в воде»
Задание 1. Транспортная функция липидов.Охарактеризуйте, что представляют собой липопротеины крови. Укажите важнейшие липидные компоненты липопротеинов.
Задание 2. Укажите, какими липопротеинами переносятся экзогенные и эндогенные триглицериды.
Задание 3. Какие фракции липопротеинов переносят «плохой» и «хороший» холестерин. Какие фракции липопротеинов обладают наибольшей атерогенностью (образуют атеросклеротические бляшки).
Задание 4. Обоснуйте, почему липопротеины плазмы крови являются водорастворимыми при высоком содержании в них липидов разных классов.
Задание 5. Фосфолипидами, участвующими в формировании липопротеинов, являются фосфатидилхолин (лецитин) и сфингомиелин, образуемые с участием линолевой (18:2) и олеиновой (18:1) кислот. Изобразите структуру указанных фосфолипидов.
Занятие 1.3.7.
«Принципы гормональной и нейромедиаторной регуляции»
Задание 1. Приведите структуру циклопентанопергидрофенантрена (стерана), пронумеруйте цикл. Изобразите производное стерана, содержащее метильные группы в 10 и 13 положениях, а гидрокси-группу – в 17 положении. Все известные гормоны отличаются между собой заместителями, находящимися в этих положениях.
Задание 2. Укажите отличия (3) в структуре женских половых гормонов (эстрадиола) и мужских половых гормонов (тестостерона). Какое из указанных соединений проявляет антиоксидантные свойства.


Эстрадиол Тестостерон
Задание 3. Укажите три отличия в структуре эстрадиола (основного женского гормона) и прогестерона (гормона беременности, гормона желтого тела).

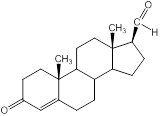
Эстрадиол Прогестерон
Задание 4. Выявите генетическую связь между холестерином, андростероном (одним из мужских половых гормонов) и эстроном (одним из женских половых гормонов).


