Алканы
Общая формула гомологического ряда, гибридизация атомов углерода, химическое строение молекулы метана и его гомологов.Изомерия углеродного скелета. Номенклатура.
Физические свойства алканов.Химические свойства: реакции замещения (галогенирование, нитрование). Механизм реакции радикального замещения, его основные стадии. Понятие о региоселективности реакций. Дегидрирование и дегидроциклизацияалканов. Ароматизация углеводородов (платформинг, риформинг). Изомеризация. Каталитическое окисление и горение алканов. Пиролиз и конверсия метана. Крекинг алканов (термический и каталитический).
Химические методы синтеза алканов. Прямой синтез из углерода и водорода. Синтез метана гидролизом метаноидных карбидов. Синтез Фишера-Тропша. Синтез углеводородов из галогенопроизводных по реакции Вюрца и пиролизом натриевых солей карбоновых кислот (реакция Дюма). Электролиз водных растворов солей карбоновых кислот (реакция Кольбе). Гидрирование ненасыщенных углеводородов и циклоалканов. Крекинг высшихалканов (термический и каталитический).
Алкены
Общая формула гомологического ряда, гибридизация атомов углерода, химическое строение молекулы этилена. Изомерия углеродного скелета, положения двойной связи, пространственная и межклассовая. Номенклатура этиленовых углеводородов.Физические свойства алкенов.
Химические свойства алкенов. Присоединение водорода (гидрирование), галогенов (галогенирование), галогеноводородов (гидрогалогенирование), воды (гидратация). Механизм реакции электрофильного присоединения. Правило Марковникова. Гидробромирование в присутствии органических перекисей (реакция Хараша). Радикальное хлорирование алкенов (реакция Львова). Алкены как алкилирующие реагенты. Реакции гидрокарбонилированияалкенов – современный метод синтеза альдегидов, карбоновых кислот, сложных эфиров и амидов. Алкены как реагенты (диенофилы) в диеновом синтезе (реакция Дильса-Альдера).
Реакции окисления алкенов. Горение. Каталитическое окисление кислородом с образованием альдегидов и эпоксидов. Окисление водным раствором перманганата калия с образованием гликолей (реакция Вагнера). Окисление жесткими окислителями (азотная кислота, подкисленные растворы перманганата и дихромата калия) с разрывом молекулы по двойной связи.Реакции полимеризации алкенов: этилена, пропилена, винилхлорида. Общие понятия химии высокомолекулярных соединений: мономер, полимер, структурное звено, степень полимеризации.Получение алкенов: выделение из продуктов крекинга, дегидродимеризация метана, дегидрирование алканов, гидрирование алкинов. Дегидрогалогенирование галогенопроизводных спиртовым раствором щелочи, дегидратация спиртов в присутствии кислотных катализаторов. Правило Зайцева. Дегалогенированиевицинальныхдигалогенопроизводных активными металлами (цинк, магний).
Циклоалканы
Общая формула гомологического ряда, гибридизация атомов углерода. Угловое напряжение Байера и его проявление: «банановые» связи в циклопропане и неплоские циклы большего размера. Изомерия углеродного скелета с сохранением и без сохранения размера цикла, пространственная и межклассовая изомерии. Номенклатура циклоалканов. Физические свойства циклоалканов.
Химические свойства. Реакции присоединения с разрывом цикла в циклопропане (сходство с алкенами): присоединение галогенов, галогеноводородов. Применение правила Марковникова для замещенных циклопропанов. Реакции галогенирования с сохранением цикла для средних циклов (сходство с алканами). Гидрирование циклопропана, циклобутана и циклопентана. Дегидрирование циклогексана. Окисление циклоалканов сильными окислителями с образованием дикарбоновых кислот. Горение.
Получение циклоалканов: выделение из нефти некоторых месторождений (нафтены), реакция дигалогенопроизводных с активными металлами как общий способ синтеза циклоалканов (внутримолекулярная реакция Вюрца), циклизация пентана, гидрирование бензола и его гомологов.
Алкадиены.
Общая формула гомологического ряда, гибридизация атомов углерода. Изомерия углеродного скелета, положения двойных связей, пространственная и межклассовая изомерии. Номенклатура диеновых углеводородов.
Понятие о сопряжении. π,π–Сопряжение. Сопряженные 1,3-диены. Основные представители сопряженных диенов: дивинил, изопрен и хлоропренОсобенности протекания реакций присоединения в сопряженных диенах (1,2- и 1,4-присоединение). Преимущественное образование продуктов 1,4-присоединения при повышенной температуре. Гидрирование, галогенирование, гидрогалогенирование, циклоприсоединение. Полимеризация и сополимеризация сопряженных диенов с образованием каучуков.Получение сопряженных диенов: дивинила дегидрированием бутан-бутеновой фракции, изопрена – дегидрированием изопентан-изопентеновой фракции нефти, хлоропрена – присоединением хлороводорода к винилацетилену. Синтез бутадиена-1,3 по методу Лебедева из этилового спирта. Возможные методы синтеза сопряженных диенов: дегидратация диолов, дегидрогалогенированиедигалогенопроизводных и дегалогенированиететрагалогенопроизводных соответствующего строения.
Алкины
Общая формула гомологического ряда, гибридизация атомов углерода, строение молекула ацетилена. Изомерия углеродного скелета, положения тройной связи и межклассовая. Номенклатура ацетиленовых углеводородов. Физические свойства алкинов.
Химические свойства алкинов. Присоединение водорода (гидрирование), галогенов (галогенирование), галогеноводородов (гидрогалогенирование), возможность постадийного протекания этих реакций. Присоединение воды (гидратация) к ацетилену и его гомологам (реакция Кучерова). Енолы. Полимеризация ацетилена и его гомологов. Алкины как СН-кислоты, образование ацетиленидов серебра и меди(I), их гидролиз. Реакции винилированияалкинов с концевой тройной связью: присоединение спиртов, фенолов, карбоновых кислот, аминов. Применение правила Марковникова для этих реакций. Реакции гидрокарбонилированияалкинов – удобный метод получения ненасыщенных карбоновых кислот, их сложных эфиров и амидов. Окисление алкинов в различных условиях (с разрывом и без разрыва молекулы по тройной связи). Горение.
Получение алкинов: карбидный синтез и пиролиз метана – способы получения ацетилена. Дегидрогалогенированиедигалогенопроизводных и дегалогенированиететрагалогенопроизводных соответствующего строения. Алкилированиеацетиленидовгалогенопроизводными как метод синтеза гомологов ацетилена.
Арены
Общая формула гомологического ряда, гибридизация атомов углерода, электронное строение молекулы бензола. Правило ароматичности Хюккеля. Номенклатура и изомерия гомологов бензола. Физические свойства аренов.
Химические свойства бензола: реакции галогенирования, нитрования, ацилирования, сульфирования. Реакции алкилирования (алкенами, спиртами, галогенопроизводными) как метод получения гомологов бензола. Механизм реакций электрофильного замещения в аренах. Роль катализатора в каждом из вышеперечисленных процессов. Реакции присоединения (водорода, хлора). Горение и каталитическое окисление бензола до малеинового ангидрида. Окисление боковых цепей в гомологах бензола. Галогенирование гомологов бензола в боковую цепь. Ориентирующее действие заместителей в бензольном кольце в реакциях замещения. Ориентанты первого и второго рода, их активирующее и дезактивирующее влияние на бензольное кольцо. Получение стирола и его реакции по двойной связи: бромирование, гидрирование, окисление, полимеризация.
Получение аренов: тримеризация ацетилена и его гомологов, дегидрирование циклогексана и его производных, дегидроциклизацияалканов, сплавление солей ароматических кислот со щелочами, реакция Вюрца-Фиттига. Примеры природных и искусственно синтезированных ароматических соединений.
Спирты.
Классификация спиртов по характеру углеводородного радикала и по числу гидроксильных групп. Номенклатура спиртов. Спирты первичные, вторичные, третичные. Проба Лукаса. Водородная связь между молекулами, ее влияние на физические свойства спиртов. Гомологический ряд предельных одноатомных спиртов. Изомерия углеродного скелета, положения функциональной группы, межклассовая.
Химические свойства спиртов. Проявление кислотных свойств (ОН-кислотность) при взаимодействии с активными металлами, гидридами и амидами активных металлов. Спирты как нуклеофилы в реакциях нуклеофильного замещения (взаимодействие с галогеноводородами, карбоновыми кислотами) и нуклеофильного присоединения (взаимодействие с альдегидами и кетонами). Дегидрирование и аммонолиз спиртов. Реакции внутри- и межмолекулярной дегидратации. Реакции окисления: окисление до карбонильных соединений и карбоновых кислот, горение. Этиленгликоль и глицерин как представители многоатомных спиртов. Особенности их физических и химических свойств в связи с увеличением числа гидроксильных групп в молекуле. Хелатообразование. Получение спиртов: гидролизом алкилгалогенидов и сложных эфиров, гидратацией алкенов, восстановлением карбонильных соединений и сложных эфиров. Получение спиртов взаимодействием карбонильных соединений с реактивами Гриньяра и по реакции Канниццаро. Получение метанола из водяного газа, этанола – брожением сахаросодержащих веществ, глицерина – гидролизом жиров.
Пример билета (задания 1-20 обязательны, задания 21-25 желательны для выполнения)
1. Из предложенного перечня выберите реакции, в которые может вступать гексан:
1) нитрование 2) ароматизация 3) гидрирование
4) изомеризация 5) окисление
Ответ:_________________(Запишите цифры в порядке возрастания).
2. Циклогексанможнополучить:
1) взаимодействием 1,6-дибромогексана с цинком
2) дегидрированием гексана
3) гидрированием бензола
4) взаимодействием 1-бромопропана с натрием
5) гидрированием гексена-3
Ответ:_________________(Запишите цифры в порядке возрастания).
3. При окислении циклоалканов в зависимости от условий могут образоваться:
1) алканы 2) двухосновные карбоновые кислоты 3) углекислый газ
4) спирты 5) соли двухосновных карбоновых кислот
Ответ:_________________.(Запишите цифры в порядке возрастания.)
4. Продуктом реакции пропена с хлором в различных условиях могут быть:
1) 1,2-дихлоропропен 2) 3-хлоропропен 3) 2-хлоропропан
4) 1,2-дихлоропропан 5) 1,2,3-трихлоропропан
Ответ:_________________.(Запишите цифры в порядке возрастания.)
5. Для каких из приведенных в задании соединений в реакции с HCl правило Марковникова не соблюдается?
1) СН3-СН=СН2 2) CF3-CH=CH2 3) 
4) СН3СН=СНСН3 5) СНСl=CH2
Ответ:_________________.(Запишите цифры в порядке возрастания.)
6. Среди предложенных соединений выберите изомеры изопрена:
1) пентин-1 2) циклопентен 3) бутадиен-1,3
4) метилбутадиен-1,3 5) пентадиен-1,3
Ответ:_________________.(Запишите цифры в порядке возрастания.)
7. Какие из приведенных формул полимеров отражают строение каучуков?
1) (‑CH2‑CH=CH‑CH2‑CH(C6H5)CH2‑)n 2) (‑СН2‑СН2‑)n
3)  4) (—СН2—СН=СН—СН2—)n 5) (‑СН2‑СНCl‑)n
4) (—СН2—СН=СН—СН2—)n 5) (‑СН2‑СНCl‑)n
Ответ:_________________.(Запишите цифры в порядке возрастания.)
8. Ацетилен в промышленности можно получить:
1) перегонкой сырой нефти 2) термическим крекингом метана
3) выделением из природного газа 4) дегидрированием этана
5) прямым синтезом из углерода и водорода
Ответ:_________________.(Запишите цифры в порядке возрастания.)
9. Взаимодействие пропина с избытком бромоводорода протекает:
1) по ионному механизму 2) с разрывом π-связей в молекуле пропина
3) с образованием свободных радикалов
4) с преимущественным образованием 2,2-дибромопропана
5) с преимущественным образованием 1,2-дибромопропана
Ответ:_______________.(Запишите цифры в порядке возрастания.)
10. Среди предложенных реагентов выберите те, которые помогут отличить гексин-1 от гексина-2:
1) бромная вода 2) подкисленный раствор KМnO4
3) аммиачный раствор оксида серебра 4) гидрид натрия
5) аммиачный раствор хлорида меди(I)
Ответ:_________________.(Запишите цифры в порядке возрастания.)
11. Среди предложенных пар соединений выберите пары, состоящие из гомологов:
1) бензол и этилбензол 2) изопропилбензол и кумол
3) этилбензол и пара -ксилол 4) этилбензол и кумол 5) бензол и толуол
Ответ:_________________.(Запишите цифры в порядке возрастания.)
12. В отличие от бензола, стирол взаимодействует:
1) с галогенами 2) с азотной кислотой 3) с перманганатом калия
4) с кислородом 5) с галогеноводородами
Ответ:_________________.(Запишите цифры в порядке возрастания.)
13. Для аренов характерны реакции:
1) гидрирования 2) гидрогалогенирования
3) нитрования 4) окисления 5) гидратации
Ответ:_________________.(Запишите цифры в порядке возрастания.)
14. В цепочкепревращений:
СН4  X1
X1  Х2
Х2  Х3
Х3  Х4
Х4
неизвестными веществами Х являются:
1) бензойная кислота 2) бензол 3) ацетилен
4) толуол 5) 4-хлоробензойная кислота
Запишите в таблицу номера выбранных веществ.
| X1 | X2 | X3 | X4 |
15. Взаимодействие толуола с бромом на свету протекает:
1) по радикальному механизму 2) с разрывом π-связей в молекуле толуола
3) как реакция присоединения 4) как реакция замещения
5) в присутствии катализатора 6) по ионному механизму
Ответ:_______________.(Запишите цифры в порядке возрастания.)
16. Дегидратация спиртов может приводить к образованию:
1) альдегидов 2) кетонов 3) алкенов 4) алкинов 5) простых эфиров
Ответ:_________________.(Запишите цифры в порядке возрастания.)
17. Этандиол-1,2 можетреагировать с:
1) гидроксидом меди(II) 2) оксидом железа(II) 3) хлороводородом
4) азотной кислотой 5) калием 6) фосфором
Ответ:__________________. (Запишите цифры в порядке возрастания.)
18. Дляосуществленияпревращенийпосхеме
С2Н2 → С2Н4 → С2Н5ОН → СН3СНО
необходимо последовательно провести реакции:
1) гидратации 2) гидрирования 3) окисления 4) этерификации 5) дегидрирования
Ответ:________.(Запишите цифры в порядке последовательности процессов.)
19. Среди предложенных соединений выберите соединения, являющиеся структурными изомерами:
1) бутанол-1 2) пропанол-2
3) метилпропиловый эфир 4) бутандиол-1,2
5) пентанол-2 6) гексанол-3
Ответ:_________________.(Запишите цифры в порядке возрастания.)
20. Свежеприготовленный осадок Сu(ОН)2 растворится, если к нему добавить:
1) пропандиол-1,2 2) глицерин 3) пропен
4) пропанол-2 5) этиленгликоль
Ответ:__________________. (Запишите цифры в порядке возрастания.)
21. Предложите 5 уравнений реакций получения этена и 5 уравнений реакций, характеризующих его химические свойства.
22. Напишите реакции, соответствующие предложенным схемам: а)  б)
б)  в)
в)  г)
г) 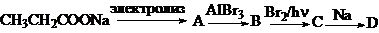
23. Определите молекулярную формулу углеводорода, содержащего 88.2% углерода и 11.8% водорода, если плотность его паров по гелию равна 17.
24. Карбид кальция обработали избытком воды. Выделившийся газ занял объем 4.48 л (н. у.). Рассчитайте, какой объем 20%-ной соляной кислоты плотностью 1.10 г/мл пойдет на полную нейтрализацию образовавшейся щелочи.
25. При бромировании 28.8 г гомолога бензола в присутствии железа получено 35.82 г монобромопроизводного. Выход продукта реакции составил 75%, других нитропроизводных не образовалось.
На основании данных условия задачи:
1) установите молекулярную формулу арена;
2) установите структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в молекуле;
3) напишите уравнение реакции исходного вещества с хлором на свету.