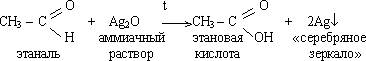Февраля Альдегиды и кетоны.
Карбонильные соединения. Простейшие альдегиды и кетоны
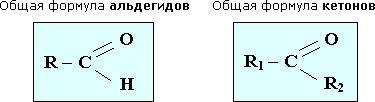
Альдегиды и кетоны называют карбонильными соединениями. Их молекулы содержат карбонильную группу  .
.
 Состав предельных альдегидов и кетонов CnH2nO.
Состав предельных альдегидов и кетонов CnH2nO.
Дополнительная информация
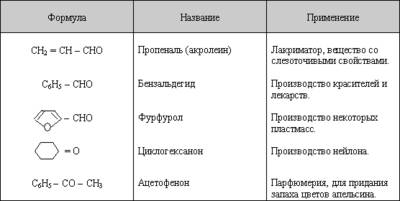
Примеры других карбонильных соединений
Кроме предельных с открытой цепью альдегидов и кетонов, известны и находят применение циклические, непредельные, ароматические, гетероциклические:
Метаналь, этаналь, пропаналь, бутаналь — это гомологи.
Пропанон, бутанон — это гомологи.
Пропаналь и пропанон — это изомеры.
Бутаналь, 2-метилпропаналь, бутанон — это изомеры.
Электронное строение альдегидов и кетонов
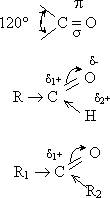
| · Атом углерода в карбониле находится в sp2 -гибридном состоянии. · Двойная связь сильнополярная (в отличие от двойной связи в молекуле CH2= CH2). · В альдегидах полярность связи С ← H больше, чем в углеводородах. · Радикалы уменьшают δ+ на атоме С карбонила. |
Электронная плотность π-связи С = O как наиболее подвижной сильно смещена к более электроотрицательному атому кислорода (полярность связи С = O больше, чем полярность C = O связи в спиртах). В результате на атоме углерода образуется частичный положительный заряд, на величину которого влияют алкильные радикалы. Очевидно, что в альдегидах δ+ на карбонильном атоме углерода больше, чем в кетонах.
Физические свойства альдегидов и кетонов
Метаналь HCHO — бесцветный газ с удушливым запахом, ядовит, его 40%-ый раствор называется формалином.
Этаналь CH3CHO — жидкость с резким запахом, хорошо растворяется в воде, ядовит.
Пропанон (ацетон) CH3COCH3 — бесцветная жидкость с характерным запахом, хорошо растворяется в воде, является органическим растворителем.
Растворимость низших альдегидов и кетонов объясняется образованием водородных связей с молекулами воды.
С увеличением молекулярной массы температуры кипения карбонильных соединений увеличиваются, а растворимость в воде снижается.
Дополнительная информация
К характеристике физических свойств
К характеристике физических свойств
Молекулы альдегидов и кетонов полярны. Но температуры кипения их ниже, чем у соответствующих спиртов, т. к. они не образуют ассоциатов за счет водородных связей. А вот с молекулами воды карбонильные соединения образуют водородные связи, чем и объясняется хорошая растворимость в воде низших альдегидов и кетонов.
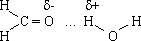
Низшие альдегиды и кетоны имеют резкие, часто неприятные запахи, но с усложнением углеводородного радикала запах становится приятным, такие соединения используются в парфюмерии.
Высшие альдегиды и кетоны — пахучие вещества, применяются в парфюмерии.
Это интересно!
Формальдегид HCHO содержится в древесном дыме и является одним из агентов, обеспечивающих консервирующее действие в ходе копчения продуктов.
Из корицы выделяют коричный альдегид C6H5CH=CHCHO, из горького миндаля — бензальдегид C6H5CHO. Эти альдегиды используют как пищевые добавки для придания запаха продуктам питания.
Это интересно!
Уксусный альдегид CH3CHO является промежуточным продуктом расщепления в организме сахаридов и первичным продуктом метаболизма этилового спирта в печени. Именно он является одной из причин состояния опьянения.
Химические свойства
Карбонильные соединения — реакционно-способные вещества.
Присоединение
Присоединение водорода — общее свойство альдегидов и кетонов, обусловленное карбонильной группой.

Важный вывод
Карбонильные соединения восстанавливаются водородом в спирты!
Из формальдегида — углевод!
Обратите внимание на очень важный в развитии органической химии синтез. В 1861 г. А.М. Бутлеров обнаружил способность формальдегида под влиянием гидроксида кальция образовывать линейные карбоцепные полимеры, близкие по свойствам к сахаристым веществам.
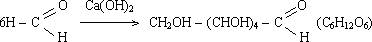
Окисление
Качественные реакции на альдегиды, обусловленные разрывом связи 
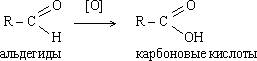
1. Окисление аммиачным раствором оксида серебра (реакция «серебряного зеркала»):