| барбитуратов | барбамил, барбитал, фенобарбитал, этаминал, циклобарбитал, гексабарбитал, бензонал | |
| алкалоидов | морфин, кадеин, дионин, героин, гидрокодон, папаверин, стрихнин, атронин, гиосциамин, скополамин, кокаин, пахикарпин, анабазин, никотин | |
| синтетических азотистых оснований | промедол, аминазин, дипразин, тизерции, мажептил, трифтазин, имизин и его аналоги |
| № п/п | Группа изолируемых веществ | Методы изолирования | Способы очистки от примесей, входящие в состав метода |
| Лекарственные вещества | Водой, подкисленной щавелевой кислотой (метод А.А.Васильевой) | - процеживание - центрифугирование | |
| Лекарственные вещества | Спиртом, подкисленным щавелевой кислотой (метод Стаса-Отто) | - упаривание вытяжек до густоты сиропа, - осаждение белков спиртом, - фильтрование. | |
| Алкалоиды | Водой, подкисленной серной кислотой (метод В.Ф.Крамаренко) | - процеживание, - центрифугирование, - осаждение примесей (NH4)2SO4, - экстракция примесей эфи- ром (рН 2-2,5). | |
| Барбитураты | Водой, подщелоченной гидроксидом натрия (метод П.Валова) | - процеживание, - центрифугирование, - осаждение белков вольфра- матом натрия, - экстракция примесей эфи- ром (рН 2). | |
| Водой, подкисленной серной кислотой (метод В.И.Поповой) | - процеживание, - центрифугирование, - гель-хроматография. | ||
| Производные фенотиазина | Спиртом, подкисленным щавелевой кислотой (модификация метода Стаса-Отто по Е.М.Саломатину) | - упаривание вытяжек до густоты сиропа, - осаждение белков спиртом, - фильтрование, - экстракция примесей эфи- ром (рН 2-3). | |
| Производные 1,4-бенздиазепина | Изолирование метаболитов производ-ных 1,4-бенздиазепина (метод Б.И. Изотова) | - деструкция тканей органов при проведении кислотного гидролиза, - центрифугирование, - фильтрование. |
Результаты выделения барбитуратов из биологического
|
|
материала различными методами
| Барбитурат | Выделено барбитуратов (%) разными методами | ||||
| Стаса-Отто | Васильевой | Крамаренко | Валова | Поповой | |
| Барбамил | |||||
| Барбитал | |||||
| Гексенал | |||||
| Гексабарбитал | |||||
| Фенобарбитал | |||||
| Этаминал | |||||
| Тиобарбитал | - |
Экстрагирование алкалоидов из водных
растворов органическими растворителями в зависимости
от рН и природы растворителя
| Алкалоид | Растворитель | Оптимальные условия экстракции | |
| значение рН | извлечено алкалоида, % | ||
| Атропина сульфат | Дихлорэтан Хлороформ Бензол Эфир | 9,5 – 11,5 9,0 – 11,5 10,5 – 12,0 9,5 – 12,0 | 90 – 93 82 – 85 72 – 75 72 – 75 |
| Кодеина фосфат | Хлороформ Изоамиловый спирт Бензол Эфир | 8,0 – 8,5 8,0 – 8,5 8,0 – 8,5 8,0 – 8,5 | 86 – 88 83 – 85 77 – 80 25 – 29 |
| Морфина гидрохлорид | Хлороформ Изоамиловый спирт Бензол Эфир | 8,6 – 10,2 8,5 – 9,5 8,5 – 9,5 8,0 – 9,0 | 28 – 30 73 – 75 4 – 5 8 – 9 |
| Экстрагирование барбитуратов из водных растворов органическими растворителями в зависимости от рН и природы растворителя | |||
| Барбамил | Эфир Хлороформ Дихлорэтан Бензол | 1,0 – 3,0 1,0 – 3,0 1,0 – 5,0 1,0 – 4,0 | 93 – 97 88 – 93 92 – 94 71 – 74 |
| Фенобарбитал | Эфир Хлороформ Дихлорэтан Бензол | 1,0 – 3,0 1,0 – 4,0 1,0 – 4,0 1,0 – 3,0 | 92 – 94 74 – 76 74 – 78 34 – 36 |
| Барбитал | Эфир Хлороформ Дихлорэтан Бензол | 1,0 – 3,5 1,0 – 2,0 1,0 – 4,0 1,0 – 5,0 | 78 – 81 38 – 40 31 – 34 4 – 6 |
Литература
|
|
1. Калетина Н.И. Токсикологическая химия. – М.: ГЭОТАР-Медиа, 2008.
2. Плетенева Т.В. Токсикологическая химия. – М.: ГЭОТАР-Медиа, 2006.
3. Байзолданов Т. Токсикологическая химия ядовитых веществ, изолиремых методом экстракции. – Алматы,2002.
4. Крамаренко В.Ф. Токсикологическая химия. – Киев: Высшая школа, 1989.
5. Швайкова М.Д. Токсикологическая химия. – М.: Медицина,1975.
6. Контрольные вопросы (обратная связь)
1. Что такое экстракция? Перечислите основные стадии процесса экстракции из биологического материала.
2. Назовите общие методы изолирования лекарственных веществ из биологического объекта.
3. От чего зависит степень извлечения?
4. Назовите частные методы изолирования лекарственных веществ из биологического объекта.
5. В чем заключается сущность метода изолирования подкисленным спиртом (метод Стаса-Отто)?
6. Сущность метода изолирования подкисленной водой (метод А.А.Васильевой)?
7. Для чего получают кислое и щелочное хлороформное извлечение?
8. Перечислите способы очистки вытяжек из биологического материала.
1. Тема 2 – Методы о6наружения и определения лекарственных веществ при проведении судебно-химической экспертизы. Барбитураты в ХТА.
2. Цель: Ознакомить студентов с методами обнаружения и количественного определения барбитуратов при проведении СХА,чтобы студент знал и мог применить их в своей практической деятельности.
Тезисы лекции
Направленный химико-токсикологический анализ
|
|
производных барбитуровой кислоты
Объекты исследования: печень, почки, мозг, селезенка, содержимое желудка, кровь, моча.
Изолирование. При направленном исследовании на барбитураты используются частные методы изолирования – водой, подщелоченной гидроксидом натрия (метод П. Валова) и водой, подкисленной серной кислотой (метод В.И. Поповой).
ТСХ скрининг. При проведении анализа в общей системе растворителей ацетон-хлороформ (1:9) барбитураты находятся во второй зоне со значениями Rf 0,31-0,41. В качестве проявителя барбитуратов используют 5 % раствор сульфата ртути и 0,1 % раствор дифенилкарбазона в хлороформе. При наличии барбитуратов появляются пятна, окрашенные в сине-фиолетовый или красно-фиолетовый цвета. Затем барбитураты элюируют из слоя сорбента ацетоном и элюаты исследуют в частной системе хлороформ-н-бутанол-25% раствор аммиака (70:40:5), сорбент - силикагель КСК, забуференный 0,1 н. раствором борной кислоты. Идентификация индивидуальных барбитуратов проводится в присутствии «свидетелей».
Обнаружение. После очистки кислой хлороформной вытяжки экстракционным методом, возгонкой, хроматографическими методами проводят подтверждение наличия барбитуратов химическими и физико-химическими методами.
Реакции окрашивания: а) с аммиачным раствором нитрата или ацетата кобальта. Наблюдается фиолетовое окрашивание, обусловленное образованием внутрикомплексного соединения:

Реакция не специфична, т.к. её дают пурины, пиримидины, сульфаниламидные препараты. Выполнению этой реакции мешают вода, которая разлагает окрашенные соединения. Реакция является высокочувствительной и носит предварительный характер.
б) мурексидная проба – при наличии барбитуратов наблюдается розовое окрашивание. Реакция обладает низкой чувствительностью и неспецифична, т.к. её дают пурины, пиримидины.
Микрокристаллоскопические реакции: а) выделение кислотной формы барбитуратов – для барбитала характерны бесцветные прозрачные прямоугольные призмы; для фенобарбитала – сфероиды; для барбамила – пластины или призмы, сгруппированные в виде сфероидов; для этамина натрия – призматические кристаллы. Реакции чувствительные и специфичные. Однако необходимо учитывать возможность появления полимофных модификаций, поэтому для подтверждения наличия индивидуальных барбитуратов проводятся б) частные реакции с реактивами:
- с хлорцинкйодом (барбамил, барбитал, этаминал натрия образуют темно-красные прямоугольные пластинки);
- с железйодидным комплексом (барбамил, фенобарбитал, этаминал натрия – оранжево-коричневые или коричневые призмы и их сростки);
- с меднойодидным комплексом (барбами, этаминал натрия – призмы и их сростки);
- со спиртовым раствором йодида калия (барбитал, этаминал натрия – призмы и их сростки);
- с меднопиридиновым реактивом (барбитал – фиолетовые кристаллы в форме звездочек, друз и прямоугольников). Наличие осадка обусловлено образованием внутрикомплексного соединения:

Физико-химические методы идентификации: обнаружение по УФ- и ИК-спектрам; методы ТСХ, ГЖХ, ВЭЖХ.
Количественное определение проводится:
- спектральными (УФ-спектрофотометрия, фотоколориметрия, дифференциальная спектрофотометрия, экстракционная фотометрия);
- хроматографическими (ТСХ, ГЖХ, ВЭЖХ).
Наиболее перспективным среди перечисленных является дифференциальная спектрофотометрия основанная на имино-имидольной таутомерии барбитуратов. После измерения оптической плотности при различных значениях рН возможно нивелировать влияние примесей на полученные результаты:
C = ∆D / E1%1cm · 1,
где: С – концентрация барбитурата в %,
∆D разность оптических плотностей, измеренных:
- при рН 2 (примеси) и рН 10 (барбитураты в имидольной форме и примеси);
- при рН 10 и рН 13 (барбитураты в диимидольной форме),
E1%1cm - удельный показатель поглощения,
1 – толщина поглощающего слоя, в см.
В сочетании с предварительной хроматографической очисткой (методом ТСХ) дифференциальная спектрофотометрия обеспечивает надежные и воспроизводимые результаты количественного анализа барбитуратов.
Иллюстративный материал

Внутрикомплесное соединение с солью кобальта

Внутрикомплесное соединение с меднопиридиновымреактивом
 Кристаллы кислотной формы
барбитала
Кристаллы кислотной формы
барбитала
| 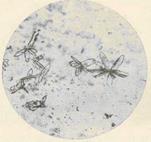 Кристаллы кислотной формы
барбамила
Кристаллы кислотной формы
барбамила
|  Кристаллы кислотной формы
фенобарбитала
Кристаллы кислотной формы
фенобарбитала
|
 Кристаллы кислотной формы
этаминала натрия
Кристаллы кислотной формы
этаминала натрия
|  Кристаллы кислотной формы
бутобарбитала
Кристаллы кислотной формы
бутобарбитала
|  Кристаллы кислотной формы
бензонала
Кристаллы кислотной формы
бензонала
|
 Кристаллы продукта взаимодействия барбитала с раствором хлорцинкйода
Кристаллы продукта взаимодействия барбитала с раствором хлорцинкйода
| 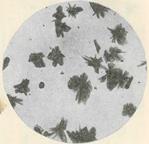 Кристаллы продукта взаимодействия барбамила с раствором хлорцинкйода
Кристаллы продукта взаимодействия барбамила с раствором хлорцинкйода
|  Кристаллы продукта взаимодействия этаминала натрия с раствором хлорцинкйода
Кристаллы продукта взаимодействия этаминала натрия с раствором хлорцинкйода
|
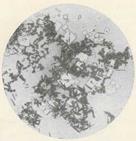 Кристаллы продукта взаимодействия фенобарбитала с железойодидным реактивом
Кристаллы продукта взаимодействия фенобарбитала с железойодидным реактивом
|  Кристаллы продукта взаимодействия этаминала натрия с железойодидным реактивом
Кристаллы продукта взаимодействия этаминала натрия с железойодидным реактивом
|  Кристаллы продукта взаимодействия барбамила с железойодидным реактивом
Кристаллы продукта взаимодействия барбамила с железойодидным реактивом
|
 Кристаллы продукта взаимодействия бутобарбитала с железойодидным реактивом
Кристаллы продукта взаимодействия бутобарбитала с железойодидным реактивом
|  Кристаллы продукта взаимодействия бутобарбитала со спиртовым раствором йодида калия
Кристаллы продукта взаимодействия бутобарбитала со спиртовым раствором йодида калия
|  Кристаллы продукта взаимодействия барбитала с меднопиридиновым реактивом
Кристаллы продукта взаимодействия барбитала с меднопиридиновым реактивом
|
 УФ-спектры поглощения барбитуратов в зависимости от рН раствора
УФ-спектры поглощения барбитуратов в зависимости от рН раствора
|
Литература
1. Калетина Н.И. Токсикологическая химия. – М.: ГЭОТАР-Медиа, 2008.
2. Плетенева Т.В. Токсикологическая химия. – М.: ГЭОТАР-Медиа, 2006.
3. Байзолданов Т. Токсикологическая химия ядовитых веществ, изолиремых методом экстракции. – Алматы,2002.
4. Крамаренко В.Ф. Токсикологическая химия. – Киев: Высшая школа, 1989.
5. Швайкова М.Д. Токсикологическая химия. – М.: Медицина,1975.
6. Белова А.В. Руководство к практическим занятиям по токсикологической химии.- М.:
Медицина, 1976.
6. Контрольные вопросы (обратная связь)
1. Что означает направленный анализ на барбитураты?
2. Какими методами проводят изолирование барбитуратов из биологического материала при
направленном ХТА?
3. Как проводится ТСХ скрининг на барбитураты?
4. Перечислите общие реакции на барбитураты.
5. Объясните, почему на барбитураты после проведения общих реакций, проводятся обязательно частные реакции?
6. Перечислите частные реакции на барбитураты.
7. На чем основан принцип спектрофотометрического определения барбитуратов в ХТА?
1.Тема 3 – Методы о6наружения и определения лекарственных веществ при проведении химическо-токсикологической экспертизы. Алкалоиды в ХТА.
2. Цель: Ознакомить студентов с методами обнаружения и количественного определения алкалоидов при проведении СХА, чтобы студент знал и мог применить их в своей практической деятельности.
Тезисы лекции
Направленный химико-токсикологический анализ алкалоидов
Объекты исследования: мозг, печень, почки, желудок и кишечник с содержимым, промывные воды, легкие, моча.
Изолирование. При направленном исследовании на алкалоиды используется частный метод изолирования водой, подкисленной серной кислотой (метод В.Ф. Крамаренко) с учетом физико-химических свойств алкалоидов.
При направленном анализе алкалоиды сильные основания и алкалоиды средней основности попадают в щелочное хлороформное извлечение, а алкалоиды слабые основания (производные пурина и индола) могут попадать и в кислое извлечение, т.к. они образуют с щавелевой кислотой легко гидролизующиеся в кислой среде соли.
ТСХ скрининг алкалоидов проводится в общей системе растворителей хлороформ-диоксан-ацетон-25% раствор аммиака (45: 47,5: 5: 2,5); сорбент – силикагель КСК; проявитель – реактив Драгендорфа модифицированного по Мунье. Алкалоиды обнаруживаются по наличию пятен оранжевого и оранжево-коричневого цвета в 1-4 зонах. Алкалоид из силикагеля элюируют смесью метанол-диэтиламин (9: 1) с последующим проведением подтверждающего хроматографирования в частных системах растворителей хлоформ-этанол (20: 1); циклогексан-ацетон (5: 1); хлороформ-диэтиламин (9: 1); хлороформ-ацетон (5: 1).
В качестве «свидетелей» используются хлороформные растворы алкалоидов данной группы. Для проведения следующего этапа анализа алкалоиды элюируют смесью растворителей метанол-диэтиламин (9: 1).
Очистка. Этап скрининга методом ТСХ позволяет параллельно проводить качественную очистку от биогенных примесей, которые локализуются на хроматографических пластинках в областях Rf < 0,2 и Rf > 0,8.
Однако, в элюате возможно присутствие остатков примесей, которые удаляются с использованием методов: экстракции, гель-хроматографии, электрофореза, сочетания экстракции и ТСХ.
Подтверждающие исследования элюата включают наиболее чувствительные химические и физико-химические методы анализа алкалоидов.
Идентификация химическим методом. Реакции осаждения с общеалкалоидными осадительными реактивами (пикриновая кислота, соль Рейнеке, реактивы: Драгендорфа, Марме, Майера, Зонненшейна и др.).
Аморфные или кристаллические осадки с нехарактерной формой частиц указывают на наличие гетероциклического атома азота в алкалоидах. Реакции высокочувствительны, не специфичны.
Микрокристаллоскопические реакции. Очищенное хлороформное извлечение выпаривают досуха, остаток растворяют в 0,1 М растворе соляной кислоты. По капле раствора наносят на предметные стекла с углублениями, куда добавляют различные реактивы, результат наблюдают под микроскопом.
Реакции высокочувствительны и специфичны при определенных условиях (дополнительная очистка, температура, влажность и давление в лаборатории).
Реакции окрашивания на алкалоиды. Для проведения этих реакций на алкалоиды хлороформное извлечение или элюат вносят в несколько фарфоровых чашек или тиглей, получают сухие остатки, к которым добавляют по капле различных реактивов и наблюдают окраски.
Можно провести цветные реакции на хроматографических пластинках. Для этого несколько капель извлечения наносят на одну точку пластины с помощью капилляра и после высыхания пятна на него наносят различные реагенты.
Реакции чувствительны, неспецифичны.
Идентификация физико-химическими методами: по УФ- и ИК-спектрам, методами ТСХ, ГЖХ, ВЭЖХ.
Идентификация по УФ-спектрам возможна только после тщательной очистки экстракцией и ТСХ-методом, или при их сочетании.
Количественное определение проводится спектральными (УФ-спектрофотометрия, фотоэлектроколориметрия, экстракционная фотометрия) и хроматографическими методами (ТСХ – планиметрический и денситометрический методы, ГЖХ и ВЭЖХ).
Иллюстративный материал