АЗОТНЫЙ ЦИКЛ В АКВАРИУМЕ БРОШЮРА ДЛЯ НАЧИНАЮЩИХ

Представляем вашему вниманию брошюру, которую мы специально подготовили для начинающих аквариумистов. В ней красочно и кратко рассказано о такой важной составляющей биологического равновесия аквариума, как азотный цикл.
В брошюре описан сам цикл, указаны причины появления высоких концентраций ядов, приведена симптоматика рыб и инструкции по выведению продуктов аммиака из аквариума. Дополнительно представлены ссылки для самостоятельного изучения данного вопроса.
Для просмотра/скачивания брошюры нажмите на картинку ниже:

Для тех, кто хочет более углубленно изучить данный вопрос, рекомендуем материал ниже:
Биологическая очистка воды
Биологическая очистка воды включает важнейшие процессы, происходящие в замкнутых аквариумных системах Под биологической очисткой будем понимать минерализацию, нитрификацию и диссимиляцию соединений, содержащих азот, бактериями, обитающими в толще воды, гравий и детрите фильтра. Организмы, выполняющие эти функции, всегда присутствуют в толще фильтра. В процессе минерализации и нитрификации азотосодержащие вещества переходят из одной формы в другую, однако азот остается в воде. Удаление азота из раствора происходит только в процессе денитрификации (см. раздел 1.3).
Биологическая фильтрация является одним из четырех способов очистки воды в аквариумах. Три других способа – механическая фильтрация, физическая адсорбция и дезинфекция воды – рассматриваются ниже.
Схема очистки воды показана на рис. 1.1., а круговорот азота в аквариуме, включающий процессы минерализации, нитрификации и денитрификации, - на рис. 1.2.
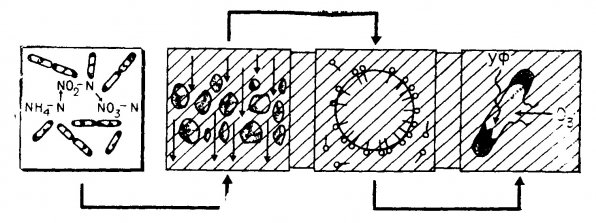
Рис. 1.1. Место биологической очистки в процессе очистки воды. Слева направо – биологическая очитка, механическая фильтрация, физическое осаждение, дезинфекция.
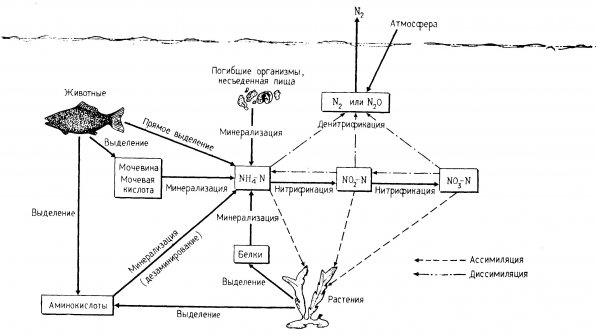
Рис. 1.2. Круговорот азота в аквариумных замкнутых системах.
Минерализация.
Гетеротрофные и автотрофные бактерии – основные группы микроорганизмов, обитающие в аквариумах.
Примечание не из книги автора.
Гетеротрофы (др.греч.— «иной», «различный» и «пища») — организмы, которые не способны синтезировать органические вещества из неорганических путём фотосинтеза или хемосинтеза. Для синтеза необходимых для своей жизнедеятельности органических веществ им требуются экзогенные органические вещества, то есть произведённые другими организмами. В процессе пищеварения пищеварительные ферменты расщепляют полимеры органических веществ на мономеры. В сообществах гетеротрофы — это консументы различных порядков и редуценты. Гетеротрофами являются почти все животные и некоторые растения. По способу получения пищи делятся на две противопоставляемые группы: голозойных (животные) и голофитных или осмотрофных (бактерии, многие протисты, грибы, растения).
Автотрофы (др.греч. - сам + пища) - организмы, синтезирующие органические вещества из неорганических. Автотрофы составляют первый ярус в пищевой пирамиде (первые звенья пищевых цепей). Именно они являются первичными продуцентами органического вещества в биосфере, обеспечивая пищей гетеротрофов. Следует отметить, что иногда резкой границы между автотрофами и гетеротрофами провести не удаётся. Например, одноклеточная водоросль эвглена зелёная на свету является автотрофом, а в темноте — гетеротрофом.
Иногда понятия «автотрофы» и «продуценты», а также «гетеротрофы» и «консументы» ошибочно отождествляют, однако они не всегда совпадают. Например, синезеленые (Cyanea) способны и сами производить органическое вещество с использованием фотосинтеза, и потреблять его в готовом виде, причём разлагая до неорганических веществ. Следовательно, они являются продуцентами и редуцентами одновременно.
Автотрофные организмы для построения своего тела используют неорганические вещества почвы, воды и воздуха. При этом почти всегда источником углерода является углекислый газ. При этом одни из них (фототрофы) получают необходимую энергию от Солнца, другие (хемотрофы) — от химических реакций неорганических соединений.
Гетеротрофные виды утилизируют органические азотосодержащие компоненты выделений водных животных в качестве источника энергии и превращают их в простые соединения, например аммоний (термин «аммоний» относится к сумме ионов аммония (NH4+) и свободного аммиака (NH3), определяемых аналитическим путем, как NH4-N). Минерализация этих органических веществ – первый этап биологической очистки.
Минерализация азотсодержащих органических соединений может начинаться с расщепления белков и нуклеиновых кислот и образования аминокислот и органических азотистых оснований. Дезаминирование – это процесс минерализации, в ходе которого отщепляется аминогруппа с образованием аммония. Предметом дезаминации может служить расщепление мочевины с образованием свободного аммиака (NH3).
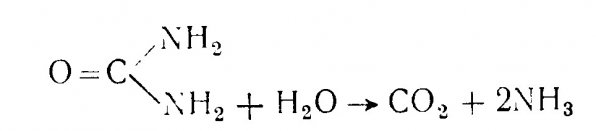
Подобная реакция может идти чисто химическим путем, однако дезаминирование аминокислот и сопутствующих им соединений требует участия бактерий.
Нитрификация воды.
После того как органические соединения переведены гетеротрофными бактериями в неорганическую форму, биологическая отчистка вступает в следующую стадию, получившую название «нитрификация». Под этим процессом понимают биологическое окисление аммония до нитритов (NO2-, определяемых как NO2-N) и нитратов (NO3, определяемых в виде NO3-N). Нитрификация осуществляется главным образом автотрофными бактериями. Автотрофные организмы в отличие от гетеротрофных способны усваивать неорганический углерод (главным образом СО2) для построения клеток своего организма.
Автотрофные нитрифицирующие бактерии в пресноводных, солоноватоводных и морских аквариумах представлены в основном родами Nitrosomonas и Nitrobacter. Nitrosomonas окисляет аммоний до нитритов, а Nitrobacter – нитриты до нитратов.
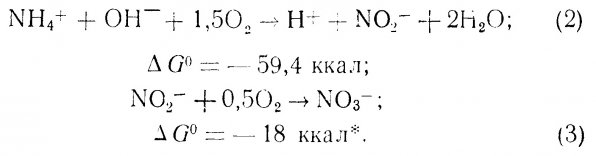
Обе реакции идут с поглощением энергии. Смысл уравнений (2) и (3) заключается в превращении токсичного аммония в нитраты, которые гораздо менее ядовиты. Эффективность процесса нитрификации зависит от следующих факторов: наличия токсикантов в воде, температуры, содержания растворенного в воде кислорода, солености и площади поверхности фильтра.
Токсичные вещества. При определенных условиях многие химические вещества подавляют нитрификацию. При добавление в воду эти вещества либо подавляют рост и размножение бактерий, либо нарушают внутриклеточный обмен бактерий, лишая их способности к окислению.
Коллинз с соавторами (Collins et al., 1975, 1976), а также Левайн и Мид (Levine and Meade, 1976) сообщали, что многие антибиотики и другие средства, применяемые для лечения рыб, не влияли на процессы нитрификации в пресноводных аквариумах, в то время как другие оказывались в разной степени токсичными. Параллельные исследования в морской воде не проводились, а приведенные результаты не следует распространять на морские системы.
Приведенные в трех указанных работах данные представлены в табл. 1.1. Результаты исследований не вполне сопоставимы из-за различий в применявшихся методиках.
Таблица 1.1. Влияние терапевтических норм растворенных антибиотиков и лечебных препаратов на нитрификацию в пресноводных аквариумах (Collins et al., 1975, 1976, Levine and Meade, 1976).
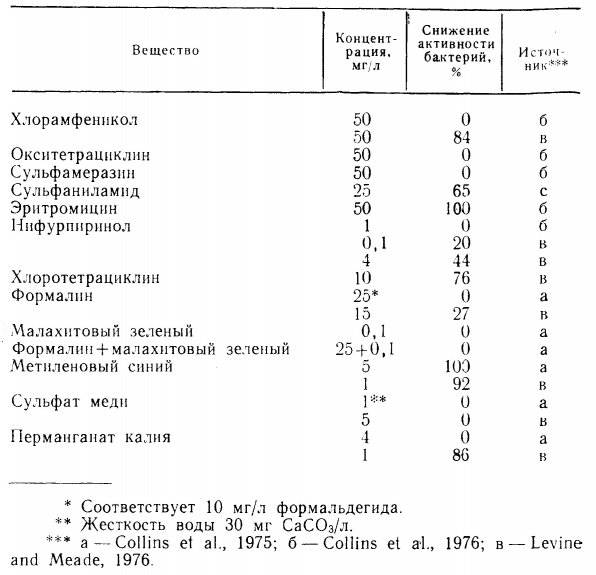
Коллинз с соавторами изучал влияние лекарственных препаратов в пробах воды, взятых непосредственно из работающих бассейнов с биофильтрами, где содержалась рыба. Левайн и Мид использовали для опытов чистые бактериальные культуры. Примененные ими методы, по-видимому, отличались более высокой чувствительностью по сравнению с обычными. Так, в их опытах формалин, малахитовый зеленый и нифурпиринол обладали средней токсичностью для нитрифицирующих бактерий, в то время как Коллинз с соавторами показал безвредность тех же препаратов.
Левайн и Мид полагали, что расхождения связаны с более высоким содержанием автотрофных бактерий в чистых культурах и порог инактивации был бы выше в присутствии гетеротрофных бактерий и при более высокой концентрации растворенных органических веществ.
Из данных табл. 1.1. видно, что эритромицин, хлоротетрациклин, метиленовый синий и сульфаниламид обладают четко выраженной токсичностью в пресной воде. Наиболее токсичным среди изучавшихся веществ оказался метиленовый синий. Результаты полученные при испытании хлорамфеникола и перманганата калия, противоречивы.
И Коллинз с соавторами и Левайн и Мид сходятся в том, что сульфат меди существенно не подавляет нитрификацию. Возможно, это результат связывания свободных ионов меди с растворенными органическими соединениями. Томлинсон и другие (Tomlinson et al., 1966) обнаружили, что ионы тяжелых металлов (Cr, Cu, Hg) гораздо сильнее воздействуют на Nitrosomonas в чистой культуре, чем в активном иле. Они предположили, что это объясняется образованием химических комплексов между ионами металлов и органическими веществами. Длительное воздействие тяжелых металлов более эффективным, чем кратковременное, по-видимому, из-за того, что адсорбционные связи органических молекул были полностью использованы.
Температура. Многие виды бактерий могут переносить значительные колебания температуры, хотя их активность временно уменьшается. Период адаптации, называемый временной температурной инактивацией (ВТИ), часто проявляется при резких изменениях температуры. Обычно ВТИ заметна при резком охлаждении воды; повышении температуры, как правило, ускоряет биохимические процессы и поэтому период адаптации может остаться незамеченным. Срна и Баггали (Srna and Baggaley, 1975) изучали кинетику нитрификационных процессов в морских аквариумах. Повышение температуры всего на 4 градуса Цельсия приводило к ускорению окисления аммония и нитритов на 50 и 12% соответственно по сравнению с исходным уровнем. При снижении температуры на 1 градус Цельсия скорость окисления аммония уменьшалась на 30%, а при понижении температуры на 1,5 градуса Цельсия скорость окисления нитритов уменьшалась на 8% по сравнению с исходными условиями.
pH воды. Каваи др. (Kawai et al., 1965) обнаружили, что при pH менее 9 нитрификация в морской воде подавляется сильнее, чем в пресной. Они объяснили это пониженным природным pH в пресной воде. По данным Секи (Saeki, 1958), окисление аммония в пресноводных аквариумах при снижении pH подавляется. Оптимальное значение pH для окисления аммония 7,8 для окисления нитритов 7,1. Оптимальным диапазоном pH для процесса нитрификации Секи считал 7,1-7,8. Срна и Баггали показали, что морские бактерии-нитрификаторы были наиболее активны при pH 7,45 (диапазон 7-8,2).
Растворенный в воде кислород. Биологический фильтр можно сравнить с огромным дышащим организмом. При правильной работе он потребляет значительное количество кислорода. Потребности водных организмов в кислороде измеряются в единицах БПК (биологическое потребление кислорода). БПК биологического фильтра частично зависит от нитрификаторов, но в основном оно обусловлено активностью гетеротрофных бактерий. Хараяма (Hirayama, 1965) показал, что при высоком биологическом потреблении кислорода активно действовала многочисленная популяция нитрификаторов. Он пропускал морскую воду через слой песка действующего биологического фильтра. Перед фильтрованием содержание кислорода в воде составляло 6,48мг/л, после прохождения слоя песка толщиной 48см. оно снизилось до 5,26мг/л. В тоже время, содержание аммония снизилось с 238 до 140 мг.экв./л., а нитритов – с 183 до 112 мг.экв./л.
В фильтровальном слое присутствуют как аэробные (для жизни необходим О2), так и анаэробные бактерии (не используют О2), однако в хорошо аэрируемых аквариумах преобладают аэробные формы. В присутствии кислорода рост и активность анаэробных бактерий подавляются, поэтому нормальная циркуляция воды через фильтр сдерживает их развитее. Если содержание кислорода в аквариуме снижается, происходит либо увеличение численности анаэробных бактерий, либо переход от аэробного дыхания к анаэробному. Многие продукты анаэробного обмена токсичны. Минерализация может происходить и при пониженном содержании кислорода, но механизм и конечные продукты в этом случае другие. В анаэробных условиях этот процесс идет скорее как ферментативный, чем как окислительный, с образованием вместо азотистых оснований органических кислот, двуокиси углерода и аммония. Эти вещества наряду с сероводородом, метаном и некоторыми другими соединениями придают задыхающемуся фильтру гнилостный запах.
Соленость. Многие виды бактерий способны обитать в водах, ионный состав которых значительно колеблется, при условии, что изменения солености будут происходить постепенно. ЗоБелл и Миченер (ZoBell and Michener, 1938) обнаружили, что большинство бактерий, выделенных из морской воды в их лаборатории, можно выращивать и в пресноводной воде. Многие бактерии перенесли даже прямую пересадку. Все 12 видов бактерий, считавшихся исключительно «морскими», были успешно переведены в пресноводную воду путем постепенного разбавления морской водой (каждый раз добавляли по 5% пресной воды).
Бактерии биологического фильтра очень устойчивы к колебаниям солености, хотя, если эти изменения значительны и внезапны, активность бактерий подавляется. Срна и Баггали (Srna and Baggaley, 1975) показали, что снижение солености на 8% и повышение на 5% не оказали влияния на скорость нитрификации в морских аквариумах. При нормальной солености воды в морских аквариумных системах нитрифицирующая активность бактерий была максимальной (Kawai et al., 1965). Интенсивность нитрификации уменьшалась как при разбавлении, так и при увеличении концентрации раствора, хотя некоторая активность сохранялась даже после повышения солености воды вдвое. В пресноводных аквариумах активность бактерий была максимальной перед добавлением хлористого натрия. Сразу после того, как соленость сравнялась с соленостью морской воды, нитрификация прекратилась.
Есть данные о том, что соленость влияет на скорость нитрификации и даже на количество конечных продуктов. Кул Манн (Kuhl and Mann, 1962) показали, что нитрификация протекала быстрее в пресноводных аквариумных системах, чем в морских, хотя нитритов и нитратов больше образовалось в последних. Каваи и др. (Kawai et al., 1964) получили сходные результаты, которые представлены на рис. 1.3.

Рис. 1.3. Численность бактерий фильтрационного слоя в малых пресноводных и морских аквариумных системах через 134 дня (Kawai etal., 1964).
Площадь поверхности фильтра. Каваи и др. обнаружили, что концентрация бактерий нитрификаторов в фильтре в 100 раз выше, чем в протекающей через него воде. Это доказывает важность величины контактной поверхности фильтра для процессов нитрификации, поскольку она обеспечивает возможность прикрепления бактерий. Наибольшую площадь поверхности фильтрующего слоя в аквариумах обеспечивают частицы гравия (грунта), причем процесс нитрификации происходит в основном в верхней части гравийного фильтра, как показано на рис. 1.4. Каваи и др. (1965) определили, что 1 грамме песка из верхнего слоя фильтра в морских аквариумах содержится 10 в 5-й степени бактерий – окислителей аммония 10 в 6-й степени – окислителей нитратов. На глубине всего 5 см. число микроорганизмов обоих типов снижалось на 90%.
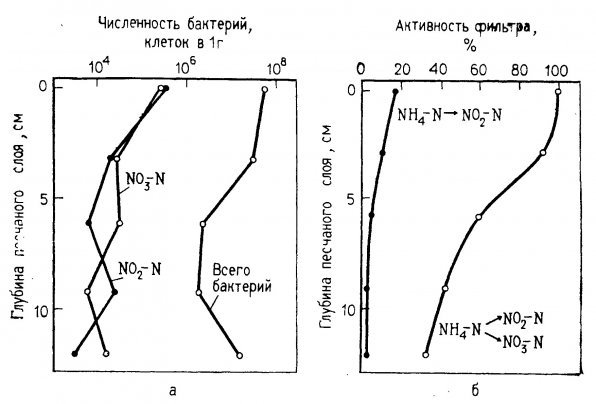
Рис. 1.4. Концентрация (а) и активность (б) нитрифицирующих бактерий на разной глубине фильтра в морском аквариуме (Yoshida, 1967).
Форма и размер частиц гравия также важны: мелкие зерна имеют большую поверхность для прикрепления бактерий, чем такое же количество по массе крупного гравия, хотя очень мелкий гравий нежелателен, так как он затрудняет фильтрацию воды. Зависимость между размерами и площадью их поверхности легко продемонстрировать на примерах. Шесть кубиков массой по 1 гр. Имеют в общей сложности 36 единиц поверхности, в то время как один кубик массой 6 гр. Имеет только 6 поверхностей, каждая из которых больше отдельной поверхности малого кубика. Общая площадь шести однограммовых кубиков в 3,3 раза больше площади поверхности одного 6-граммового кубика. По данным Секи (Saeki, 1958), оптимальный размер частиц гравия (грунта) для фильтров это 2-5 мм.
Угловатые частицы имеют большую поверхность, чем округлые. Шар имеет минимальную площадь поверхности на единицу объема по сравнению со всеми остальными геометрическим формами.
Накопление детрита (Термин «детрит» (от лат. detritus — истёртый) имеет несколько значений: 1. Мёртвое органическое вещество, временно исключенное из биологического круговорота элементов питания, которое состоит из останков беспозвоночных животных, выделений и костей позвоночных животных и др.; 2. совокупность мелких неразложенных частиц растительных и животных организмов или их выделений, взвешенных в воде или осевших на дно водоёма) в фильтре обеспечивает дополнительную поверхность и улучшает нитрификацию. Согласно данным Секи 25% нитрификации в аквариумных системах приходится на долю бактерий, населяющих детрит.
Диссимиляция
Процесс нитрификации приводит к высокой степени окисления неорганического азота. Диссимиляция, «азотное дыхание», или процесс восстановления, развивается в противоположном направлении, возвращая конечные продукты нитрификации к низкой степени окисления. В перерасчете на общую активность окисление неорганического азота значительно превосходит его восстановление, и нитраты накапливаются. Помимо диссимиляции, которая обеспечивает выделение части свободного азота в атмосферу, неорганический азот может быть удален из раствора путем регулярной замены части воды в системе, за счет усвоения высшими растениями или при помощи ионообменных смол. Последний способ удаления свободного азота из раствора применим только в пресноводной воде (см. раздел 3.3).
Диссимиляция – преимущественно анаэробный процесс, который идет в слоях фильтра, испытывающих дефицит кислорода. Бактерии – денитрификаторы, обладающие восстановительной способностью, обычно либо полные (облигатные) анаэробы, либо аэробы, способные переходить на анаэробное дыхание в бескислородной среде. Как правило, это организмы-гетеротрофы, например некоторые виды Pseudomonas, могут восстанавливать ионы нитратов (NO3-) в условиях дефицита кислорода (Painter, 1970).
При анаэробном дыхании бактерии-диссимиляторы усваиваю окись азота (NO3-) вместо кислорода, восстанавливая азот до соединения с низким окислительным числом: нитритов, аммония, двуокиси азота (N20) или свободного азота. Состав конечных продуктов определяется видом бактерий, участвующих в восстановительном процессе. Если неорганический азот восстанавливается полностью, то есть до N2O или N2, процесс диссимиляции называют денитрификацией. В полностью восстановленном виде азот может быть удален из воды и выделен в атмосферу, если его парциальное давление в растворе превышает его парциальное давление в атмосфере. Таким образом, денитрификация в отличие от минерализации и нитрификации снижает уровень неорганического азота в воде.