Для проточных реакторов идеального смешения, соединенных в каскад (К-РИС-Н), используют графический и аналитический методы расчета
Графический метод расчета. Этот метод прост и позволяет рассчитать каскад реакторов идеального смешения непрерывного действия для реакции любого порядка.
В основе расчета лежит уравнение (5)
 , (19)
, (19)
где сi, m-1 - концентрация реагентана входе в m-ый реактор;
сi, m- концентрация реагента на выходе из m-го реактора.
Из уравнения (19) находим, что
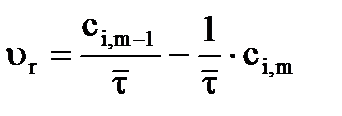 (20)
(20)
Как видно из уравнения (20), для m-го реактора зависимость скорости реакции от концентрации изображается в виде прямой с углом наклона, для которого  (рис. 3). С другой стороны, скорость реакции описывается уравнением
(рис. 3). С другой стороны, скорость реакции описывается уравнением
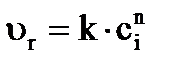 , (21)
, (21)
которое на графике в координатах  от
от  представляет собой при n>1 экспоненту, а при n = 1 прямую линию. Точка пересечения линии уравнений (19) и (20) характеризует концентрациюреагента в m-ом реакторе.
представляет собой при n>1 экспоненту, а при n = 1 прямую линию. Точка пересечения линии уравнений (19) и (20) характеризует концентрациюреагента в m-ом реакторе.
Для расчета К-РИС-Н графическим методом необходимо:
1. Вначале построить график по уравнению (19) зависимости ur от Сi.
2. Затем из точки, лежащей на оси абсцисс, для которой  провести прямую с тангенсом угла наклона, равным
провести прямую с тангенсом угла наклона, равным 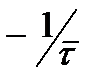 до пересечения с кривой (прямой) в точке М:
до пересечения с кривой (прямой) в точке М: 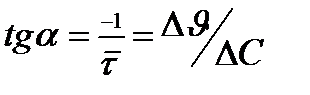 .
.
3. Опустив перпендикуляр из точки пересечения М на ось абсцисс, получают значение концентрации реагента на выходе из первого реактора. Эта же концентрация является исходной для второго реактора.
4.
| υr |
 , и т. д. до тех пор, пока в последнем реакторе не будет достигнута заданная концентрация
, и т. д. до тех пор, пока в последнем реакторе не будет достигнута заданная концентрация  . При этом число ступеней и будет числом реакторов в каскаде, необходимым для достижения заданной степени превращения.
. При этом число ступеней и будет числом реакторов в каскаде, необходимым для достижения заданной степени превращения.
| М |
| Е |
| Д |
| при n>1 |
| υr=k·Cin |
| α |
| сi,2 |
| сi,3 |
| сi |


Рис. 3. Графический метод расчета каскада реакторов идеального смешения
Аналитический метод расчета. Аналитический метод расчета используется только для химических реакций первого порядка.
Предположим, что в каскаде реакторов протекает изотермическая реакция первого порядка при постоянной массовой плотности. Объемы реакторов в каскаде одинаковы. Тогда концентрация реагента А на выходе из первого реактора выражается формулой
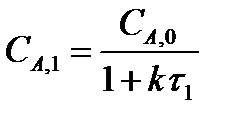 (22).
(22).
Концентрация на выходе из второго реактора представлена следующей формулой
 (23).
(23).
Таким образом, для концентрации на выходе из последнего реактора каскада СAm будет иметь следующее рекуррентное выражение:
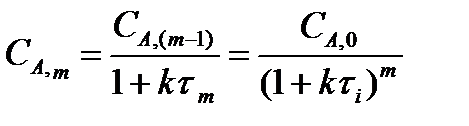 (24).
(24).
Когда реакционные объемы равны, уравнение принимает следующий вид:
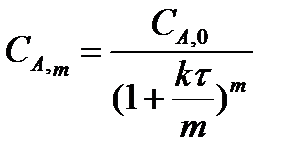 (25).
(25).
Здесь величина τ определяется по полному объему всех реакторов.
Если в каскаде реакторов одинакового объема протекает изотермическая реакция второго порядка, то воспользовавшись теми же соотношениями, что и для реакции первого порядка, можно получить следующее выражение:
 (26).
(26).
Уравнения (24) - (26) позволяют определить объемы каскада реакторов или их число, если известны остальные параметры процесса.
Отметим, что в случае расчета реакторов соединенных параллельно, необходимо учитывать расход исходного сырья на каждой из ветвей соединения. Расчетные параметры определяют суммированием уравнений, составленных для каждой ветви. Рассмотрим некоторые примеры расчета различных типов реакторов, соединенных последовательно, параллельно и смешанно.
Пример 9.
Процесс описывается реакцией типа А → 2R и осуществляется в установке из трех реакторов смешения (рис.4) Время пребывания в обоих ветвях установки одинаковое. Определить производительность по продукту R.
Дано:
объемный расход исходного вещества G0 =18 м3/ч;
начальная концентрация исходного вещества СА0= 2,6 кмоль/ м3;
константа скорости реакции k= 0.02 с -1;
Объемы реакторов Vp1=0,2 м3, Vp1=0,2м3, Vp1=0,6 м3
G01
Vp1 Vp2
G0
Vp3
G02
Рис.4. Смешанная схема соединения реакторов
Решение.
Производительность установки по продукту R складывается из производительностей верхней и нижней ветвей:
ПR = ПR1+ ПR2 = 2G01 СА,0 хА1 + 2G02 СА,0 хА2.
По условию задачи время пребывания в обеих ветвях установки одинаково, тогда:
τв= τ1 + τ2 или  , но τв= τ2; и можно записать:
, но τв= τ2; и можно записать:
 или
или 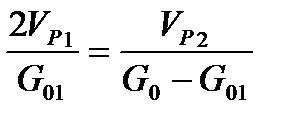 , или
, или  .
.
Решая это уравнение относительно V01, получаем:
G01 = 2 л/с =7,2м3/ч, G02 = 3 л/с = 10,8м3/ч.
Определяем время τ1 = τ2 =200/2=100 с; τн =600/3=200с.
Находим концентрацию вещества А и степень превращения на выходе из верхних и нижних ветвей установки:
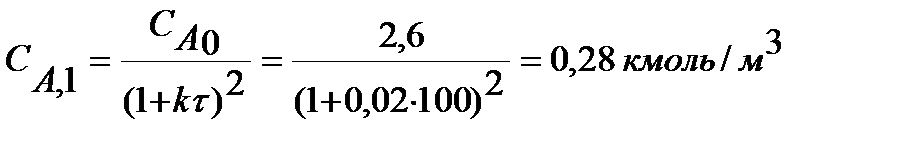
Определяем степени превращения и концентрации на выходе:
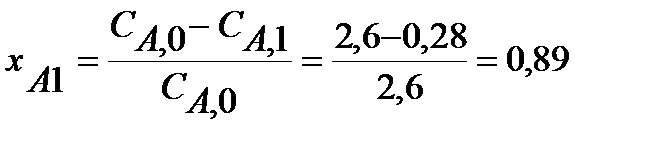 ;
;
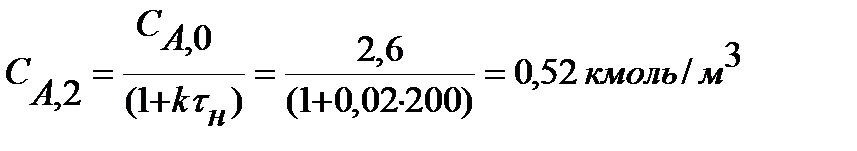 ;
;
 .
.
Определяем производительность по продукту R:
ПR = 2G01 СА0 хА1 + 2G02 СА0 хА2 = 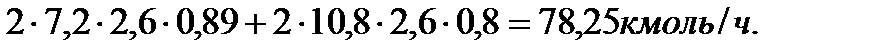
Пример 10.
Реакция проводится в параллельной схеме соединения реакторов РИС-Н и РИВ (рис.5.). Исходный поток по реакторам разделяется поровну. Определить объемные расходы, подаваемые в каждый реактор, и производительность по продукту R.
Дано:
Схема реакции А → R
объемный расход исходного вещества G0 =720 л/мин;
начальная концентрация исходного вещества СА0= 3 моль/л;
константа скорости реакции k= 0,25 с -1;
объемы реакторов Vp1=0,08 м3, Vp2=0,05м3.1
G01
Vp1
G0
G02 Vp2
Рис.5. Схема параллельного соединения реакторов
Решение.
По условию задачи G01 = G0 = 720/2 = 360 л/мин = 6 л/с.
Определяем время пребывания в реакторе смешения и реакторе вытеснения:
 ;
; 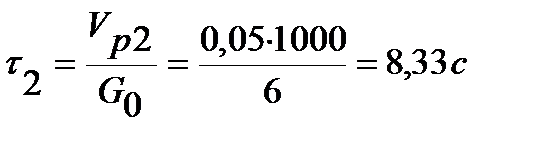 .
.
Находим степень превращения вещества А в реакторах:
 ;
;  .
.
Рассчитаем производительность по продукту R:
ПR = G01 СА0 хА1 + G02 СА0 хА2 = 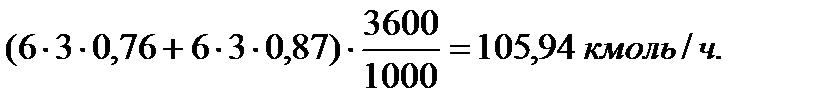
Пример 11.
Реакция проводится в параллельной схеме соединения реакторов РИС-Н и РИВ (рис.5.). Определить распределение объемного потока по реакторам и производительность по продукту R при условии, что степени превращения в реакторах равны.
Дано:
реакция А → 2R;
объемный расход исходного вещества G0 =100 л/мин;
начальная концентрация исходного вещества СА0= 2,6 моль/л;
константа скорости реакции k= 0,0205 с -1;
Объем реактора вытеснения Vp2= 50 л.
Решение.
Приравниваем уравнения для расчета степеней превращения в реакторе смешения и вытеснения:
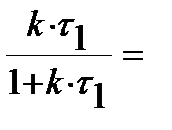

Выражаем 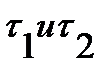 через объемы соответствующих реакторов и объемные расходы, поступающие в них, и получаем:
через объемы соответствующих реакторов и объемные расходы, поступающие в них, и получаем:
 .
.
Подставляем в полученное выражения значения и получаем:
 ,
,
где 1,66- объемный расход смеси, л/с.
Получили нелинейное уравнение, как функцию G01, которое можно решить только графически. Зависимость левой (а) и правой (в) частей уравнения от G01 приведены на рис 6.
Рис.6. Зависимость степени превращения от объемного расхода
В точках пересечения получаем значение G01 и степени превращения вещества xA в реакторах:
хА1=0,57; G01=45,3 л/ми; G02 = G0 - G01 = 54,7 л/мин.
Рассчитываем производительность установки по продукту R:
ПR=(2G01 СА0 хА1 + 2G02 СА0 хА2)=
= 
Пример 12.
Определить объем реакторов смешения (рис. 7), если входящий поток делится поровну, а степень превращения в реакторе вытеснения равна степени превращения в каскаде реакторов смешения. Объемы реакторов смешения равны.
Дано:
реакция А → R;
объемный расход исходного вещества G0 =100 л/мин;
константа скорости реакции k= 0,0205 с -1;
порядок реакции n=1;
объем реактора вытеснения Vp2= 50 л.
G01
Vp1 Vp2
G0
Vp3
G02
Рис. 7. Cмешанный тип и схема соединения реакторов
Решение.
Определяем степень превращения в реакторе идеального вытеснения:

где 
Для каскада реакторов воспользуемся формулой 25 для расчета конечной концентрации в каскаде:
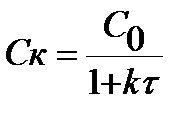 или
или  откуда находим время пребывания в одном реакторе смешения каскада:
откуда находим время пребывания в одном реакторе смешения каскада:
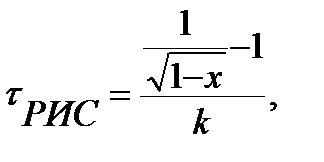 а
а  следовательно,
следовательно,
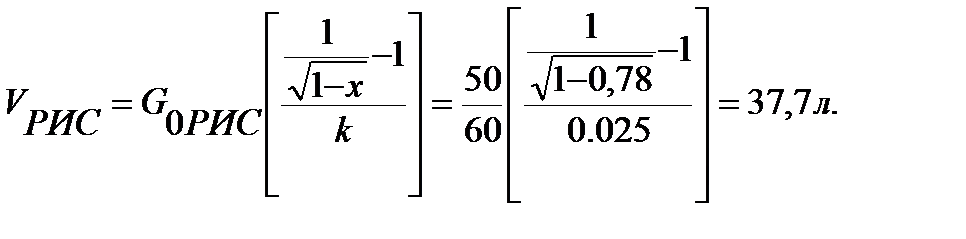
Пример 13.
Рассчитать объемы РИС-Н и РИВ до достижения заданной степени превращения хА и сравнить их объемы.
Дано:
реакция А+ В = R + S;
| концентрация реагента А в потоке, сА, пот - 0,16 моль/л; |
| Концентрация реагента В в потоке, сВ, пот - 0,12 моль/л; Объемный поток реагентов, GV,0 = GV,А + GV,В = 6 м3/ч; Соотношение потоков GV,А / GV,В = 1:3; Константа скорости, К- 5,0 л/моль × мин; Степень превращения, хA - 0,7. |
Реагенты А и В загружаются отдельными потоками, смешиваясь в определенном соотношении перед входом в реактор.
Решение.
1. Расчет РИС – Н
Объем реактора рассчитывается по уравнению (6), преобразовав в виде:
 ,
,
уравнение скорости реакции
ur,A = к · с А,0 (1 – хA) · сB,0 (1– хB).
Определим сА,0 и сB,0:
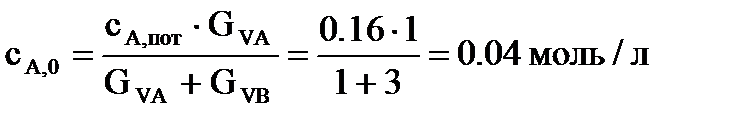 ;
;
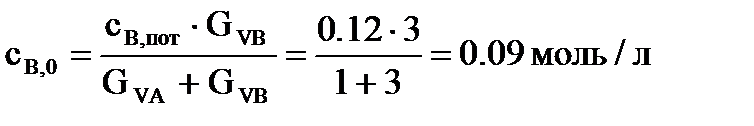 .
.
Для удобства расчета скорости выразим хB через хA:
 .
.
Так как, исходя из стехиометрии, количество А, вступившего в реакцию, равно В, то сB,0 – сB = сА,0 – сА,
следовательно,
 .
.
Выразим сB,0 через сА,0:
 , откуда сB,0 = 2,25 · с А,0, тогда;
, откуда сB,0 = 2,25 · с А,0, тогда;
 .
.
Следовательно:
ur,А = 2,25 · к · сА,02 (1- хA) (1- 0,44хА);
ur,А = 2,25 · 5 · 0,042 (1-0,7) (1-0,44·0,7) = 37,4·10-4 моль/л·мин;
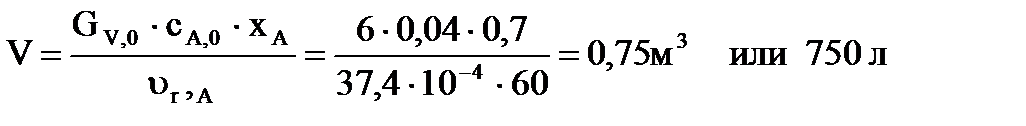 .
.
2. Расчет РИВ
 ,
,
ur,А = 2,25 · к · сА,02 (1 – хA) (1– 0,44хА)
Найдем значение интеграла графическим методом. Для этого построим зависимость  от (хA). Принимая значения хA с шагом 0,1, рассчитаем скорость реакции υr (уравнение 6) и обратное значение скорости
от (хA). Принимая значения хA с шагом 0,1, рассчитаем скорость реакции υr (уравнение 6) и обратное значение скорости  . Результаты расчета сведем в таблицу 3.
. Результаты расчета сведем в таблицу 3.
Таблица 3. Зависимость скорости реакции от степени превращения
| Расчетные величины | Число точек | |||||
| хA | 0,2 | 0,4 | 0,5 | 0,6 | 0,7 | |
| ur*103 моль / л *мин | 13,1 | 8,97 | 7,02 | 5,3 | 3,74 | |
| 1/ ur л* мин/ моль | 56,6 | 76,3 |
Построим график зависимости обратной скорости от степени превращения и рассчитаем площадь под кривой.

|
Рис. 8. График зависимости обратной скорости реакции от степени превращения
Примечание: для нахождения площади под кривой необходимо:
1) выбрать единицу измерения площади (квадрат, прямоугольник) и определить ее площадь путем умножения значений сторон с учетом размерности. Например, масштаб выбранного прямоугольника (рис.8) будет равен произведению хА на 1/ υ r, т.е. 0,1·50=5 л·мин/моль·см2;
2) определить число целых и дробных единиц измерения площади (квадрат, прямоугольник) путем их суммирования;
3) найти площадь умножением полученной суммы на масштаб;
S= 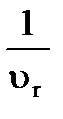 = Σs · 50.
= Σs · 50.
Площадь под кривой равна 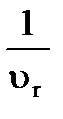 = 41,4 л·мин/моль.
= 41,4 л·мин/моль.
Так как Gv,0= 6 м3/час или 0,1 м3/мин,
то Vрив= Gv,0 · cА,0· 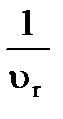 = 0,1· 0,04· 41,4 = 0,166 м3 или 166 л.
= 0,1· 0,04· 41,4 = 0,166 м3 или 166 л.
Сравнивая объемы Vрис-н и Vрив, можно сделать вывод, что РИВ является более эффективным реактором, чем РИС-Н.
Пример 14.
Определить объем одного реактора и время пребывания реагента в каскаде реакторов.
Дано:
реакция А+ В = R + S;
начальная концентрация реагента А сА,0 = 0,3 моль/л;
степень превращения хА= 0.7;
объемный расход Gv,o = 20 л/мин;
константа скорости k = 0,38 мин-1;
число реакторов в каскаде равно 4.
Решение.
1. Объём реактора полного смешения, необходимый для достижения заданного степени превращения, определяем по уравнению:
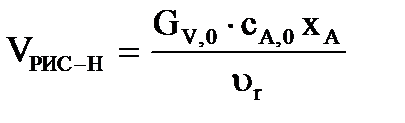 , где
, где 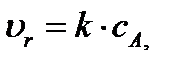
 - конечная концентрация реагента А.
- конечная концентрация реагента А.
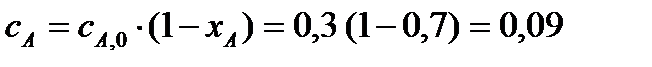 моль/л;
моль/л;
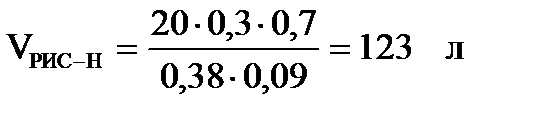 .
.
2. Среднее время пребывания реагентов в РИС-Н определяем из уравнения (11):
 .
.
Время пребывания в каждом реакторе каскада будет равно:
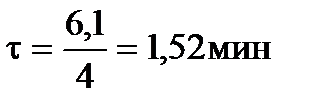 .
.
Тогда объем реактора в каскаде будет равным:
 .
.
Пример 15.
Определить объем одного реактора в каскаде, полагая, что V1=V2=V3.
Дано:
реакция 2А= R + S;
начальная концентрация реагента А,0 = 1,5 кмоль/м3;
необходимая степень превращения хА= 0.8 от равновесной;
объемный расход Gv,o = 10 м3/ч;
константа скорости k1 = 10 м3/(кмоль∙ч);
число реакторов в каскаде равно 3;
константа равновесия Кр =16,0
Решение.
Равновесную концентрацию реагента А определяем из выражения
константы равновесия:
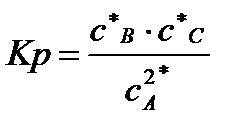
Обозначим равновесные концентрации через y.
Тогда с*А = 1,5-2у, с*В = с*С = y.
Подставляя в уравнение для константы равновесия, получим:
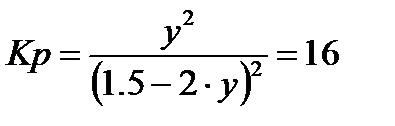 .
.
Решая уравнение, находим значение у =0,66 кмоль/м3. Полученное значение представляет собой равновесную степень превращения. По условию реагент А прореагирует на 80% от равновесной степени превращения:
хА= 0,8×0,66 = 0,53 кмоль/м3
Тогда конечная концентрация реагента А составит:
сА = 1,5- 2×0,533 = 0,43 кмоль/м3
Уравнение скорости реакции в соответствии со стехиометрическим уравнением записываем в виде

или 
Зависимость  рассчитана при значениях сА от 1,5 до 0,3 кмоль/м3 с шагом 0,2.
рассчитана при значениях сА от 1,5 до 0,3 кмоль/м3 с шагом 0,2.
Таблица 4. Расчетные значение скорости реакции и концентрации вещества
| сА, кмоль/м3 | 1,5 | 1,3 | 1,1 | 0,9 | 0,7 | 0,5 | 0,3 |
 ,м3/(кмоль×ч) ,м3/(кмоль×ч)
| 22,.5 | 16,9 | 12,1 | 8,1 | 4,9 | 2,5 | 0,67 |
Построим график зависимости  от сА
от сА

Рис.9. Графическая зависимость скорости реакции от концентрации вещества
Если из точки на оси абсцисс сА,0 провести прямую, то получим точку пересечения с кривой в точке а. При проведении процесса в одну ступень получаем (рис 7.3):
 ,
,
t = 0,63 ч.
Объем единичного реактора:
V РИС-Н = GV,0 × t = 10×0,63 = 6,3 м3.
Примечание: так как по условию объемы трех реакторов одинаковы, то угол наклона проведения прямых к точкам пересечения с кривой будет одинаков. Если уменьшим объем реактора, то для достижения заданной степени превращения необходимо увеличить количество реакторов в каскаде. При этом угол наклона поменяется и будет постоянным для всего количества реакторов в каскаде. Соответственно изменится и время пребывания реагентов в реакторе.