ЛАБОРАТОРНАЯ РАБОТА № 18
Разработка технологического процесса восстановления деталей гальваническими покрытиями
Цель работы: ознакомиться с технологией нанесения гальванических покрытий, научиться рассчитывать режимы и нормы времени.
Выполнил: ст. Прохоров К., гр.18СХТ-1
Общие положения
Сущность процесса нанесения гальванических покрытий. В авторемонтном производстве при восстановлении деталей нашли широкое применение гальванические и химические процессы. Они применяются для компенсации износа рабочих поверхностей деталей, а также при нанесении на детали противокоррозионных и защитно-декоративных покрытий. Гальванические и химические способы обработки предназначены для восстановления изношенных поверхностей деталей (хромирование, железнение, никелирование); для защиты деталей от коррозии (цинкование, бронзирование, оксидирование): для защитно-декоративных целей (хромирование, никелирование, цинкование, оксидировацие); для придания поверхностям деталей специальных свойств, обеспечиваюших хорошую прирабатываемость (меднение, лужение, свинцование, фосфатирование), защиту от науглероживания при цементации (меднение), повышение электрической проводимости (меднение, серебрение), повышение отражательной способности (хромирование, никелирование), подслоя под другое покрытие (медь, никель) или грунта под окраску.
В основе восстановления деталей гальваническими покрытиями лежит процесс электролиза, т.е. прохождения постоянного тока через электролит, связанное с передвижением электрически заряженных частиц – ионов.
Электролиз — электрохимический процесс (электролиз металлов), протекающий между анодом и катодом (деталью) в электролите (водном растворе соли, кислоты или щелочи) и сопровождающийся выделением на катоде металла (рисунки 1 и 2).
|
|
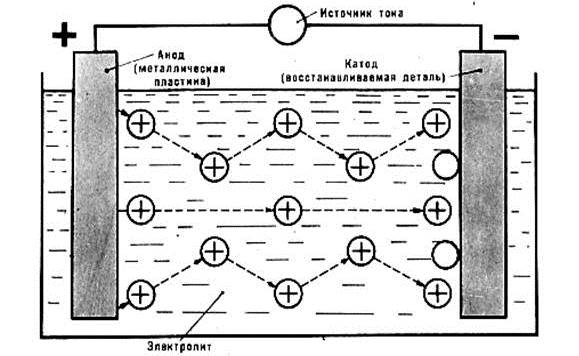
Рисунок 1 - Принципиальная схема процесса электролитического наращивания.
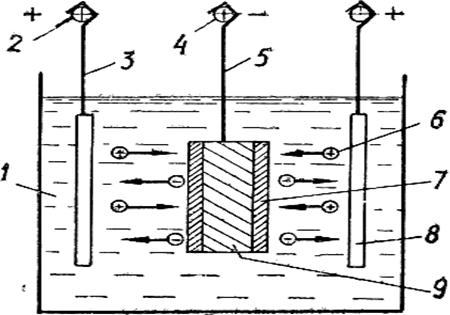
Рисунок 2 - Схема электрохимического осаждения металла
1 - ванна; 2 - Анодная штанга; 3 - Крюк (подвеска) для завешивания анода; 4 - катодная штанга; 5 - крюк подвеска для завешивания детали (катода); 6 - ионы металла (катионы); 7 - покрытие; 8 - Анод; 9 - деталь (катод).
При прохождении постоянного тока через электролит на аноде 3 происходит растворение металла (переход его в электролит) и выделение кислорода, а на катоде 9 (деталь) — отложение металла и выделение водорода.
Из гальванических процессов наиболее широко применяются хромирование и железнение, а также никелирование, цинкование и меднение. Применяются также химические процессы; химическое никелирование, оксидирование и фосфатирование
Электролитические покрытия предпочтительнее наплавки, так как:
- процессы гальванического осаждения металла не вызывают структурных изменений в деталях,
- позволяют устранять незначительные износы,
- легче поддаются механизации и автоматизации,
- можно получать равномерные по толщине покрытия с широким диапазоном твердости (от 1000 до 12000 МПа), что позволяет восстанавливать большую номенклатуру деталей, значительно отличающихся конструктивно-технологическими характеристиками и условиями эксплуатации,
- одновременно можно восстанавливать значительное количество деталей,
- применяемые электролиты можно использовать многократно,
|
|
- технологический процесс легко поддается механизации и автоматизации.
Недостатки электролитического наращивания:
- сравнительно низкая производительность процесса,
- большой цикл подготовительных операций,
- значительное выделение вредных веществ (хлор, кислотные испарения и т.п.).
Наибольшее распространение получили осталивание (железнение), хромирование, никелирование, меднение, нанесение электролитических сплавов.
Железнение:
- высокая производительность наращивания (скорость осаждения металла 0,2…0,5 мм/ч),
- толстые осадки (до 2 мм и более),
- высокие физико-механические свойства,
- недорогие и недефицитные материалы,
- себестоимость восстановления – 30…50% от стоимости новой детали при одинаковой износостойкости.
Хромирование:
- высокая твердость, жаростойкость, износостойкость покрытий, низкий коэффициент трения;
- осадки хрома обладают повышенной хрупкостью и плохой прирабатываемостью;
- низкий к.п.д.;
- процесс чувствителен к изменениям температуры электролита и плотности тока,
- электролит нестабилен по составу и требует корректировки в процессе электролиза.
Увеличивает износо - и коррозионную стойкость деталей, улучшает внешний вид.
Никелирование:
- высокая твердость, жаростойкость, износостойкость покрытий, низкий коэффициент трения;
- низкая производительность,
- дефицитные материалы,
- электролит нестабилен по составу и требует корректировки в процессе электролиза,
- высокая себестоимость восстановления.
|
|
Применятся для защитно-декоративных целей, как подстилающий слой при декоративном хромировании, а иногда для повышения изностойкости и восстановления деталей – поршневых колец, пальцев, плунжеров и т. п.
Безванные способы применяют для восстановления крупногабаритных деталей: коленчатых валов, отверстий корпусных деталей, цилиндров двигателей и др. К безванному осаждению металла относятся три способа: струйный, проточный, натиранием.
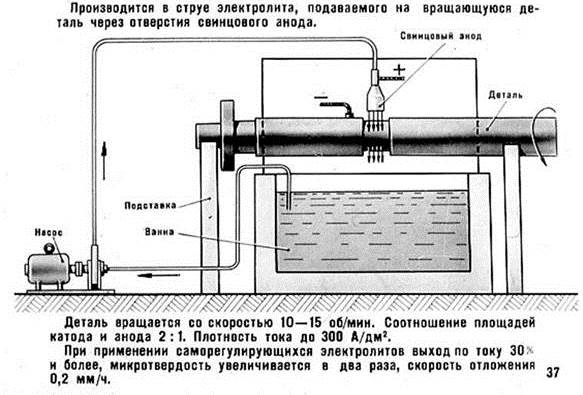
Рисунок 3 - Струйное хромирование.
В проточном электролите восстанавливают внутренние поверхности цилиндров двигателей (рисунок 4) и гидроцилиндров, которые образуют местную ванну для циркулирования электролита. Он нагнетается в полость детали насосом. Расстояние между зеркалом цилиндра (катодом) и стержнем (анодом) должно быть не менее 5...10 мм. При струйном и проточном способах восстановления деталей применяют плотность тока 180...220 А/дм2.
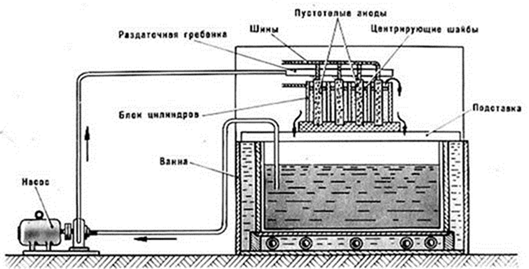
Рисунок 4 - Установка для безванного хромирования в проточном электролите
Принципиальная схема наращивания металла э лектролитическим натиранием приведена на рисунке 5
Восстанавливаемую деталь закрепляют в патроне станка и подключают к катоду источника постоянного тока 9. Электролит из сосуда 1 с помощью капельницы с краном подается к войлочному тампону 4, Закрепленному в тампонодержателе (анод). В межэлектродном пространстве между деталью и стержнем (это собственно местная ванна) протекает электрохимическая реакция, в результате которой на детали наращивается металл.
Этим способом можно восстанавливать и внутренние поверхности (например, отверстия корпусных деталей), при этом применяют подвижный (вращающийся) анод.
Относительное перемещение анода (катода) препятствует росту зерен, структура осадка получается мелкозернистая и ненапряженная, а поверхность очень гладкая, что в отдельных случаях позволяет исключить механическую обработку покрытия. Рабочая плотность тока при электронатирании — 150...180 А/дм2. Производительность этого способа в 3...4 раза выше, чем ванных.
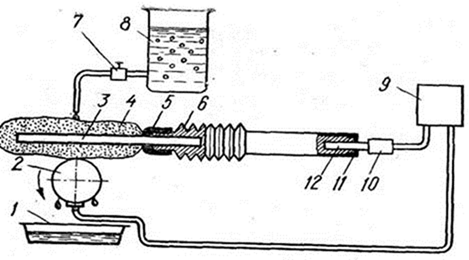
Рисунок 5 - Электролитическое осаждение металла натиранием
1 — емкость для сбора электролита; 2 — деталь (катод); 3 — графитовый стержень (анод); 4 — тампон; 5 — пластмассовый колпачок; 6 — алюминиевый корпус; 7 — кран; 8 — резервуар с электролитом; 9 — источник тока; 10 — клемма; 11 — пластмассовая гайка; 12 — штеккер для подвода тока к аноду
Хромирование. Технологический процесс хромирования включает следующие операции:
1) механическая обработка поверхности;
2) промывка органическими растворителями;
3) изоляция участков, не подлежащих покрытию;
4) монтаж на подвесные приспособления;
5) обезжиривание;
6) промывка в горячей и холодной воде;
7) декапирование;
8) электроосаждение покрытия.
При хромировании в качестве электролита используют водный раствор хромового ангидрида (CrО3) и серной кислоты (Н2SO4). При хромировании используют нерастворимые аноды, изготовленные из сплава свинца с сурьмой. Изменяя режим электролиза (плотность тока, температуру электролита) можно получить различные хромовые покрытия:
- матовые (серые) отличаются высокой твердостью, хрупкостью и пониженной износостойкостью (некачественные);
- блестящие отличаются высокой твердостью, хрупкостью и износостойкостью. Имеется сетка пересекающихся трещин. Применяется для деталей, работающих на износ;
- молочные отличатся высокой износостойкостью, большой вязкостью и пониженной твердостью. Сетка трещин отсутствует. Для деталей, воспринимающих большие удельные давления и знакопеременные нагрузки.
Железнение. Технологический процесс включает следующие операции:
1) механическая обработка поверхности;
2) защита поверхностей, не подлежащих покрытию;
3) обезжиривание в бензине или щелочном растворе;
4) промывка в горячей и холодной воде;
5) монтаж на подвесные приспособления;
6) анодная обработка (травление);
7) промывка в холодной воде;
8) железнение;
9) промывка в горячей воде;
10) нейтрализация;
11) механическая обработка.
В качестве электролита применяют водный раствор хлористого железа (FeCl2×4H2O) и соляную кислоту (НСl) и некоторые другие компоненты. Железнение производят с применением растворимых анодов из малоуглеродистой стали 08 или 10, помещенных в чехлы из стеклоткани для сбора шлама.
Технологические приемы получения износостойких покрытий.
Применение ассиметричного периодического тока позволяет путем изменения параметров обратного импульса управлять свойствами покрытий (износостойкость, микротвердость, усталостная прочность), а также увеличить производительность процесса.
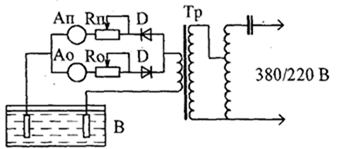
Рисунок 6 – Принципиальная схема установки для получения ассиметричного периодического тока
Режим процессов электролитического наращивания определяется следующими основными показателями:
- состав электролита (г/л);
- кислотность электролита: рН < 7 – кислый, рН = 7 – нейтральный, рН > 7 - щелочной;
- температура, оС;
- плотность тока, А/дм2;
- выход по току (к.п.д.), %.
Таблица 1. Примеры режимов электролитического наращивания
| Показатель режима | Вид электролитического наращивания | ||
| Железнение | Хромирование | Никелирование | |
| Состав электролита, г/л | Хлористое железо- 400…600, Аскорбиновая кислота - 0,5…2. | Хромовый ангидрид - 120…150, Серная кислота – 1,2…1,5. | Щавелевокислый алюминий – 300, Сернокислый никель – 140, Хлористый натрий – 10. |
| Кислотность, рН | 0,8…1,3 | - | - |
| Температура, оС | 20…40 | 50…65 | 7,5…8,5 |
| Плотность тока, А/дм2 | 20…40 | 30…100 | 75…82 |
| Выход по току, % | 85…92 | 15…16 | 90…95 |
В соответствии с законом Фарадея толщина h, мм, осаждаемого металлического покрытия
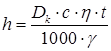
где Dк - рекомендованная для данного электролита и его температуры катодная плотность тока, А/дм2;
c - электрохимический эквивалент, г/ А*ч; (железнение c =1,042; хромирование c =0,323; никелирование c =1,095)
η — выход по току, %, (железнение – 90%; хромирование – 15%; никелирование – 50%)
t — продолжительность электролиза, ч;
γ — плотность металла, г/см3; (железнение γ =7,8; хромирование γ =6,9; никелирование γ =8,9).
Силу тока при нанесении покрытий определяют по формуле:
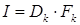
где 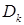 - катодная плотность тока, А/дм2;
- катодная плотность тока, А/дм2;
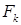 - площадь покрываемой поверхности, дм2.
- площадь покрываемой поверхности, дм2.
Катодная плотность тока определяется условиями работы детали, видом покрытия и т.д. Для учебных целей катодную плотность можно принять из таблицы 1.
Площадь анода определяется по формуле:
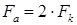
Норма времени на выполнение наращивания слоя металла на изношенной поверхности определяется по формуле:
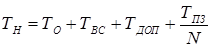
Основное время рассчитаем по формуле:
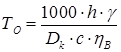
Аналитические зависимости получены из условия равномерности распределения осадка по наращиваемой поверхности. В действительности толщина осадка на различных участках детали не одинакова — на выпуклых поверхностях толщина слоя больше.
Норма времени определяется по формуле:
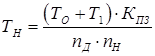
где Т1 - время на загрузку и выгрузку деталей (Т1 =0,2 ч);
КПЗ - коэффициент подготовительно-заключительного времени (КПЗ =1,2);
пД - число деталей, одновременно наращиваемых в ванне (пД =1);
пн - коэффициент использования ванны (пн =0,8).
Ответы на контрольные вопросы
1.Какое назначение гальванических покрытий?
Они применяются для восстановления деталей, компенсации износа рабочих поверхностей деталей, а так же при нанесении на детали противокоррозионных и защитно-декоративных покрытий.
2. В чем заключается сущность электрохимического (гальванического) способа нанесения покрытий?
В электролизе, т.е. в прохождении постоянного тока через электролит, связанного с передвижением электрически заряженных частиц – ионов. Который в свою очередь представляет электрохимический процесс (электролиз металлов), протекающий между анодом и катодом (деталью) в электролите (водном растворе соли, кислоты или щелочи) и сопровождающийся наращиванием на катоде дополнительного металла.
3. Что представляют собой катоды и аноды в гальваническом производстве?
Катод- это деталь, на которое наносится покрытие. Анод- металлические (медь, никель, хром, серебро, цинк, железо и др.) пластины.
4. Перечислите и охарактеризуйте основные операции технологии нанесения гальванических покрытий
Подготовка детали (зачистка, промывка, обезжиривание, защита необрабатываемых поверхностей); определение: материалов и техпроцесса, толщины покрытия, параметров тока, выбор электролита и анода, подвеска деталей, доработка деталей после покрытия(механическая, химическая),контроль
5. Какое оборудование и устройства применяются для нанесения гальванических и химических покрытий?
Ванны для погружения, слива электролитов, промывки;