ХИМИЯ
Инструкция: Вам предлагается ознакомиться с двумя контекстами и выполнить к ним тестовые задания с выбором одного правильного ответа.
Степень окисления
Степенью окисления элемента называют условный заряд его атома в соединении, который он приобретает, отдавая или принимая электроны от других элементов. Если элемент отдаёт свой электрон, он приобретает положительную степень окисления, если принимает - отрицательную.
Степень окисления обозначается арабскими цифрами со знаком «+» или «-». Каждому атому в любом сложном соединении соответствует определенная степень окисления. Например, для фтора во фтороводороде HF степень окисления равна -1, для водорода +1. В простом веществе степень окисления любого элемента равна 0.
Степень окисления многих химических элементов – величина переменная. Например, для серы известны следующие степени окисления: +2 в 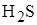 , +4 в
, +4 в 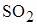 , +6 в
, +6 в 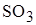 . В простом веществе степень окисления серы равна нулю. Атомы металлов проявляют только положительную степень окисления. Атомы неметаллов (кроме фтора) могут проявлять как положительную, так и отрицательную степень окисления.
. В простом веществе степень окисления серы равна нулю. Атомы металлов проявляют только положительную степень окисления. Атомы неметаллов (кроме фтора) могут проявлять как положительную, так и отрицательную степень окисления.
В соединениях неметаллов одного и того же периода отрицательную степень окисления будет иметь элемент с большим порядковым номером, например, в хлориде фосфора (V) 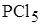 :
: 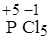
В химических соединениях сумма абсолютных значений степеней окисления равна нулю.
1. Количество электронов перешедших к более электроотрицательному элементу в соединении 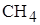
A) 5
B) 2
C) 4
D) 3
E) 6
2. Степень окисления хлора в соединении 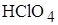
A) +1
B) +2
C) +3
D) +5
E) +7
3. Одинаковое значение степени окисления кремний проявляет в веществах
A) 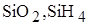
B) 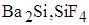
C) 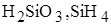
D) 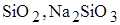
E) 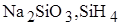
4. Степени окисления частиц 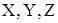
|
|
| Частица | Заряд ядра | Распределение электронов по слоям | |||
| I | II | III | IV | ||
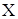
| +8 | - | |||
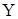
| +13 | ||||
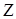
| +19 |
A) +3, 0, +1
B) 0, +3, +1
C) +1, 0, +3
D) +1, +3, 0
E) +3, +1, 0
5. В ряду 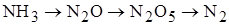 степень окисления азота
степень окисления азота
A) понижается, затем растет
B) растет, затем снижается
C) увеличивается
D) уменьшается
E) не изменяется
Движение электрона в атоме
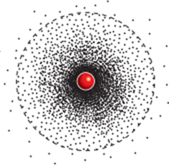
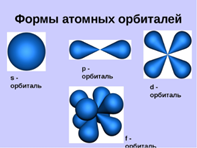
Рис 1 Рис 2
Согласно современным представлениям, электрон в атоме находится в постоянном движении вокруг ядра, не имеющий определенной траектории. В каждый момент времени электрон находится в определенной точке около ядерного пространства (рис 1). Модель движения электрона вокруг ядра называют электронными облаками, или орбиталями.
Электроны в атомах при движении образуют электронные облака различной формы (рис 2). Электроны, образующие при движении орбитали шарообразной формы, называют s -электонами. Электроны, образующие орбитали гантелеобразной формы, называют р-электронами, которые распологаются перпендикулярно по осям x, y, z. Существуют также d- и f- электронные облака, имеющие более сложное строение.
Электронное строение атома удобнее изображать в виде электронных формул, которые составляют следующим образом: сначала пишут номер энергетического уровня, затем буквой обозначают форму электронного облака и цифрой (справа над буквой) указывают число электронов с данной формой облаков.
Например, порядковый номер кислорода – 8, значит у него имеется 8 электронов, которые распределяются на двух энергетических уровнях следующим образом: 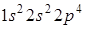 .
.
|
|
6. Сера на внешнем энергетическом уровне имеет_____электронов
A) 2
B) 3
C) 4
D) 5
E) 6
7. Количество орбиталей у атома хлора
A) 5
B) 6
C) 2
D) 3
E) 4
8. Диаграмма атома химического элемента
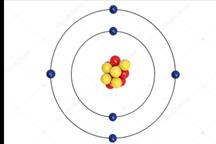
A) кислорода
B) азота
C) углерода
D) фтора
E) бора
9. Электронная формула металла
A) 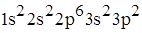
B) 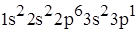
C) 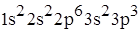
D) 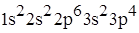
E) 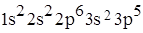
10. Электронная формула иона 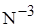 одинакова с
одинакова с
A) 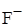
B) 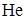
C) 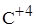
D) 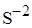
E) 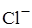
Инструкция: Вам предлагаются тестовые задания с выбором одного или нескольких правильных ответов.
11. Соединение кальция в костях организма человека, молярная масса которого (г/моль)
A) карбонаты, 106
B) фосфаты, 185
C) силикаты, 135
D) сульфаты, 400
E) нитраты, 85
F) фосфаты, 310
G) сульфаты, 342
H) сульфаты, 142
12. Массовые доли элементов в соединении, входящего в состав костей (%)
A) 40,00
B) 34,48
C) 29,41
D) 24,39
E) 38,71
F) 20,00
G) 41,29
H) 58,71
13. Типы кристаллических решеток соединений, такой, как у соединения, представленного на рисунке

A) 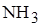
B) 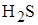
C) 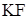
D) 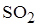
E) 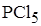
F) 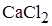
G) 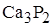
H) 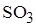

14. Металлическая связь – это связь между
A) катионами и анионами
B) свободными электронами
C) молекулами
D) протонами
E) нейтронами
F) катионами металлов
G) анионами
H) протонами и электронами
15. Группа щелочных металлов
A) 
B) 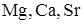
C) 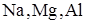
D) 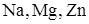
E) 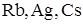
F) 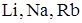
G) 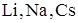
H)