Исследование термодинамических процессов
(2 часа)
Цель работы
Исследование влияния показателя политропы на характеристики состояния рабочего тела и энергетические результаты процессов.
Задачи работы
1 Изучить экспериментальный метод исследования политропных процессов.
2 Усвоить порядок расчета термодинамических процессов.
Обеспечивающие средства
Экспериментальная установка, порядок проведения измерений и обработки результатов опыта.
Краткие теоретические сведения
Термодинамический процесс – последовательность изменения термодинамических состояний системы (переход газа из начального состояния в конечное). Политропный процесс - термодинамический процесс, во время которого теплоёмкость газа остаётся неизменной.
Частные случаи политропного процесса: при Т = const (закон Бойля-Мариотта); при р = const (закон Гей-Люссака); при V = const (закон Шарля); при S=const.
Порядок выполнения работы
Проведение процессов в экспериментальной установке предполагает изменение состояния воздуха в трубе (1). При заполнении трубы водой из водопроводной сети через вентиль 6 при запорных вентилях (5) и (7) происходит сжатие воздуха. При удалении воды из трубы (1) через вентиль (7) при закрытых вентилях (5), (6) происходит расширение сжатого воздуха. Скорость заполнения труб водой или удаление воды позволяет провести процессы различного характера. Так, медленная подача (удаление) воды (в течение 30 минут) позволяет провести процесс, близкий к изотермическому.
При исследовании процессов сжатия перед началом опыта при помощи вентиля (5) выравнивается давление воздуха внутри сосуда с окружающим. Опыт заканчивается при достижении избыточного давления 4 атм.
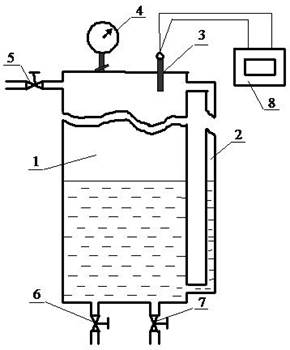
Рис. 2. Схема установки для исследования термодинамических процессов:
1 – вертикальная стальная труба (d = 20 см); 2 – водоуказательное стекло;
3 – термометр сопротивления; 4 – манометр; 5, 6, 7 – вентили;
8 – прибор 2ТРМ1-двухканальный измеритель-регулятор
Вначале опыта, до подачи воды в сосуд, записать показания приборов в графу 1 табл. 2.1. После подачи воды в сосуд показания всех приборов снимают при увеличении давления внутри сосуда на 1 атм и заносят их в соответствующие графы табл. 2.1.
Таблица 2.1
Протокол результатов измерений
| № | Показания
манометра
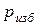 , кПа , кПа
| Показания прибора 2ТРМ1 t, °C | Высота столба воздуха
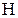 , м , м
|
| а б в |
Обработка результатов исследований
Используя полученные в эксперименте данные, определяют абсолютное давление, температуру и объем воздуха в цилиндрической трубе для каждого измерения.
Из уравнения состояния находят массу воздуха, m, кг, в цилиндре
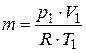 , (2.1)
, (2.1)
где 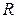 – газовая постоянная воздуха, кДж/(кг·К).
– газовая постоянная воздуха, кДж/(кг·К).
Газовая постоянная воздуха, 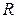 , кДж/(кг·К), определяется по формуле
, кДж/(кг·К), определяется по формуле
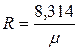 , (2.2)
, (2.2)
где 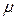 – молярная масса воздуха, равная 28,96 кг/моль.
– молярная масса воздуха, равная 28,96 кг/моль.
Удельный объем воздуха, u, м3/кг, для каждого измерения определяется из соотношения
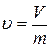 . (2.3)
. (2.3)
Энтропия воздуха, S, кДж/кг  К, определяется по формуле
К, определяется по формуле
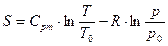 , (2.4)
, (2.4)
где 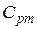 – средняя массовая изобарная теплоемкость воздуха, кДж/(кг·К);
– средняя массовая изобарная теплоемкость воздуха, кДж/(кг·К); 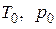 – температура и давление при нормальных физических условиях (
– температура и давление при нормальных физических условиях (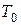 = 273 К;
= 273 К; 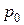 = 101,3 кПа).
= 101,3 кПа).
Средняя массовая изобарная теплоемкость воздуха, 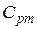 , кДж/(кг·К), определяется по формуле
, кДж/(кг·К), определяется по формуле
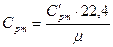 , (2.5)
, (2.5)
где 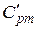 – средняя объемная изобарная теплоемкость воздуха, которая определяется по температуре табл. П.3.1.
– средняя объемная изобарная теплоемкость воздуха, которая определяется по температуре табл. П.3.1.
Уравнение политропного процесса 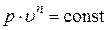 . Показатель политропного процесса n определяют по выражению
. Показатель политропного процесса n определяют по выражению
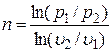 . (2.6)
. (2.6)
Используя экспериментальные данные и найденный показатель политропы, проверяют справедливость соотношений
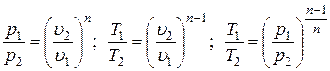 ; (2.7)
; (2.7)
Теплоту, участвующую в процессе, Q, кДж, определяют по уравнению
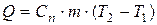 , (2.8)
, (2.8)
где 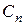 – теплоемкость в политропном процессе, кДж/(кг·К).
– теплоемкость в политропном процессе, кДж/(кг·К).
Теплоемкость в политропном процессе, 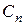 , кДж/(кг·К), определяется по формуле
, кДж/(кг·К), определяется по формуле
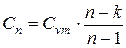 , (2.9)
, (2.9)
где 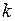 – показатель адиабаты для воздуха, k =1,4.
– показатель адиабаты для воздуха, k =1,4.
Работу в процессе, L, кДж, находят по уравнению
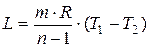 . (2.10)
. (2.10)
Изменение внутренней энергии, ∆U, кДж, определяется по формуле
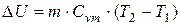 . (2.11)
. (2.11)
По результатам расчетов заполняют табл. 2.2. Проверяют справедливость первого закона термодинамики для условий опыта
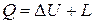 . (2.12)
. (2.12)
В р, u- и Т, s- координатах строят графики процессов.
Таблица 2.2
Результаты расчетов
| № | 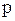 , кПа , кПа
| 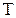 , К , К
| V, м3 | 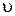 , м3/кг , м3/кг
| 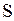 , кДж/(кг×К) , кДж/(кг×К)
|
| а б в |
2.3. Контрольные вопросы и задания к защите лабораторных работ
1. Какие процессы называются политропными?
2. Назовите частные случаи политропных процессов.
3. Связь показателя политропы с частными случаями политропных процессов.
4. Назовите приборы и способы определения основных характеристик состояния рабочего тела.
5. Изобразите графически частные случаи политропных процессов в р, u – и Т, s – координатах.
6. Как рассчитываются энергетические результаты процессов?