Рассмотрим некоторую циклическую машину (рис.).
В качестве теплоприемника может выступать окружающая атмосфера, температуру  которой считаем постоянной. Пусть рабочее тело получает от теплоотдатчика в форме теплоты энергию которой считаем постоянной. Пусть рабочее тело получает от теплоотдатчика в форме теплоты энергию  . .
| 
|
Тепловая машина превратит в работу часть этой энергии, причем
 .
.
Температура теплоотдатчика 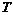 может изменяться, при этом он переходит из некоторого состояния 1 в 2. В этом случае порции теплоты
может изменяться, при этом он переходит из некоторого состояния 1 в 2. В этом случае порции теплоты  сообщаются рабочему телу при различной температуре
сообщаются рабочему телу при различной температуре 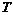 , следовательно
, следовательно
 .
.
Можем записать:  , где
, где  – элементарное количество теплоты, которое теплоотдатчик получает от рабочего тела. Тогда
– элементарное количество теплоты, которое теплоотдатчик получает от рабочего тела. Тогда
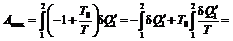
 ,
,
где 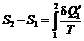 – изменение энтропии теплоотдатчика в случае, если состояния 1 и 2 соединяются с помощью некоторого обратимого процесса.
– изменение энтропии теплоотдатчика в случае, если состояния 1 и 2 соединяются с помощью некоторого обратимого процесса.
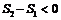 , т.е. энтропия уменьшается.
, т.е. энтропия уменьшается.
Таким образом, в работу превращается лишь часть энергии  , которая сообщается рабочему телу в форме теплоты, причем отличие тем больше, чем больше при этом уменьшилась энтропия системы, выступающей в качестве теплоотдатчика. Т.е. энтропия системы, за счет энергии которой совершается работа, накладывает предел на получение максимальной работы.
, которая сообщается рабочему телу в форме теплоты, причем отличие тем больше, чем больше при этом уменьшилась энтропия системы, выступающей в качестве теплоотдатчика. Т.е. энтропия системы, за счет энергии которой совершается работа, накладывает предел на получение максимальной работы.
Понятие о термодинамических потенциалах
Наряду с энтропией используют ряд других, связанных с ней функций состояния системы. Наиболее важны из них:
1. 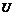 – внутренняя энергия;
– внутренняя энергия;
2. 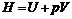 – энтальпия;
– энтальпия;
3.  – свободная энергия (функция Гельмгольца);
– свободная энергия (функция Гельмгольца);
4.  – функция Гиббса.
– функция Гиббса.
Данные функции состояния являются термодинамическими потенциалами. Это следует из того, что при равновесных процессах, в которых остаются постоянными некоторые из параметров системы, убыль термодинамических потенциалов равна совершаемой системой работе.
Покажем это, используя первое начало термодинамики  .
.
1. Внутренняя энергия 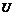 .
.
При адиабатическом процессе  имеем:
имеем:  .
.
2. Энтальпия 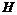 .
.
В самом общем случае совершаемую системой элементарную работу  можно представить в виде:
можно представить в виде:
 ,
,
где  – работа, не связанная с изменением объема системы (например, работа против сил поверхностного натяжения, работа по перемещению зарядов в электрическом поле и т.д.).
– работа, не связанная с изменением объема системы (например, работа против сил поверхностного натяжения, работа по перемещению зарядов в электрическом поле и т.д.).
Тогда первое начало имеет вид:
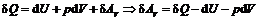 .
.
Отсюда при одновременном выполнении условий  и
и  получим:
получим:
 .
.
3. Свободная энергия  .
.
Для обратимых процессов:  .
.
При  получим:
получим:  .
.
Тогда 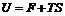 , т.е. внутреннюю энергию системы можно разделить на две части. Одна из них – свободная энергия – может быть превращена в работу при обратимом изотермическом процессе и в этом смысле является «свободной». Вторая, равная
, т.е. внутреннюю энергию системы можно разделить на две части. Одна из них – свободная энергия – может быть превращена в работу при обратимом изотермическом процессе и в этом смысле является «свободной». Вторая, равная  , в том же процессе не может быть превращена в работу и называется связанной энергией.
, в том же процессе не может быть превращена в работу и называется связанной энергией.
Для термодинамической системы, находящейся при постоянных температуре и объеме, 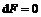 . При необратимом процессе
. При необратимом процессе 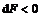 , т.е. свободная энергия может только убывать, поэтому условием равновесия такой системы будет условие минимума свободной энергии.
, т.е. свободная энергия может только убывать, поэтому условием равновесия такой системы будет условие минимума свободной энергии.
4. Функция Гиббса 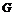 .
.
С учетом работы, не связанной с изменением объема системы:
 .
.
Тогда  .
.
Отсюда при  и
и  имеем:
имеем:
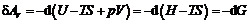 .
.
Зависимость давления насыщенного пара
От температуры
Чтобы проинтегрировать уравнение Клапейрона-Клаузиуса, найдём сначала зависимость теплоты испарения от температуры, т.е. L (T).
К состоянию пара при температуре Т от жидкости при температуре Т 0 можно прийти двумя путями.
1-ый способ: испарить жидкость при температуре Т 0 и нагреть пар при постоянном давлении до температуры Т. Затрачиваемая на 1 моль энергия равна:

2-ой способ: жидкость нагреть до Т, а затем испарить.

Начальные и конечные состояния в обоих способах одинаковы, поэтому 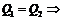

В уравнении Клапейрона-Клаузиуса можно пренебречь молярным объёмом жидкости по сравнению с молярным объёмом газа:
 «
« , где
, где  .
.
Кроме того, для пара предполагаем выполнение уравнения 
Тогда 
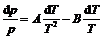 .
.
Таким образом, давление насыщенного пара для фазового перехода жидкость–газ определяется формулой:
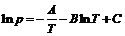 , где А, B, С – постоянные.
, где А, B, С – постоянные.