Тема: Углеводы.
Классификация углеводов
Общая формула: Сх(Н2О)y
I.Моносахариды - углеводы, которые не расщиплятся на более простые углеводы (глюкоза, фруктоза, рибоза,дизоксилибоза)
II.Олигосахариды (дисахариды) – углеводы, которые при гидролизе дают несколько моносахаридов (сахароза).
III.Полисахариды – углеводы, которые дают множество молекул моносахаридов при гидролизе (крахмал, целлюлоза, гликоген)
Глюкоза
Строение молекулы глюкозы
А) Линейное строение
С6Н12О6 – глюкоза

СН2ОН – СНОН – СНОН – СНОН – СНОН - СНО
СН2ОН – (СНОН)4 –СНО
С6Н7О (ОН)5.
Глюкоза – альдегидоспирт т.к обладает свойствами альдегидов (есть альдегидная группа) и свойствами многоатомных спиртов (есть 5ОН).
I. Циклическое строение
а) α- форма глюкозы – гидроксильные группы располагаются по одну сторону кольца молекулы при первом и втором углероде
α – форма
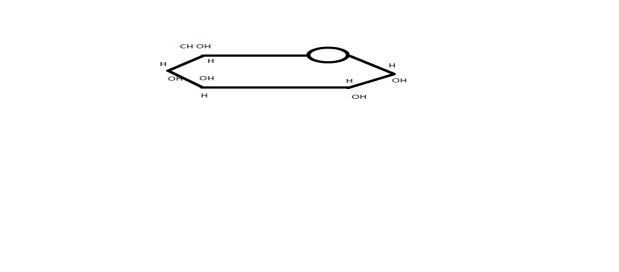
б) β глюкоза – группы ОН располагаются по разные стороны кольца

 2) Нахождение в природе
2) Нахождение в природе
В свободном виде глюкоза находится в зеленых растениях Особенно много в виноградном соке (виноградный сахар) В организме человека содержится в мышцах и в крови и немного во всех клетках организма.
В природе глюкоза образованная в процессе фотосинтеза - процесс образования органических веществ в зеленых листьях на свету в присутствии хлорофилла с выделением кислорода.
6СО2+6Н2О→ С6Н12О6+6О2↑
Физические свойства.
Глюкоза – бесцветное кристаллическое вещество, сладкое на вкус, хорошо растворимо в воде.
Химические свойства.
I.Свойства общие с многоатомными спиртами (так как есть 5ОН):взаимодействие с гидроксидом меди (II).
Опыт: в пробирку прилить Сu(ОН)2 и раствор глюкозы
Наблюдения: ярко – синий раствор
СuSO4+2NaOH→Cu(OH)2↓+Na2SO4
C6H7O (OH)5+ Cu(OH)2↓→C6H7O(OH)3 Cu +2H2O
Глюконат меди(II)
Ярко-синий р-р
II.Свойство общие с альдегидами:
а) взаимодействие с Cu(OH)2 при tº
Опыт: пробирку с Сu(OH)2 и глюкозой нагреть.
Наблюдение: выпадает желтый осадок, переходящий в кирпично – красный осадок.
CH2OH (CHOH)4 – CНО + Cu(OH)2→CH2OH(CHOH)4 – CООН + Cu2O↓+2H2O
Глюконовая кислота
б) Реакция серебряного зеркала.
CH2OH – (CHOH)4 – CНО +Ag2O→CH4OH(CHOH)4 – CООН +2Ag↓
Вывод: глюкоза - альдегидоспирт, так как обладает свойствами многоатомных спиртов (есть 5-ОН) и свойствами альдегидов (альдегидная группа -СНО)
в) Гидрирование: в результате образуется 6-ти атомный спирт – сорбит
CH2OH – (CHOH)4 – CНО +H2→CH2OH(CHOH)4 – CH2OH
III Специфические свойства глюкозы
Глюкоза подвергается брожению:
а) спиртовое
C6H12O6→2C2H5OH+2CO2↑
б) молочно – кислое
C6H12O6→2CH3 – CHOH –COOH
в) масляно – кислое
C6H12O6→C3H7COO+2H4↑+2CO2↑
5) Применение:
Глюкозу используют при интоксикации (например при пищевом отравлении или деятельности инфекции), вводят внутривенно струйно и капельно, так как она является универсальным антитоксическим средством. Также препараты на основе глюкозы и сама глюкоза используется эндокринологами при определении наличия и типа сахарного диабета у человека (в виде стресс теста на вывод повышенного количества глюкозы из организма)
Дисахариды.
Сахароза
Строение молекулы сахарозы
С12Н22О11
В отличии от глюкозы, сахароза имеет гидроксильные группы, но не имеет альдегидную группу это можно доказать опытом:
Пробирку с Cu(OH)2 и раствором сахарозы встряхнуть, образуется ярко-синий раствор (так как есть гидроксильные группы). Пробирку нагреть. Изменений окраски не произошло. Нет альдегидной группы.
Структурная формула сахарозы:

С12Н22О11 + Н2О→ С6Н12О6 + С6Н12О6
Физические свойства
Сахароза – бесцветные кристаллическое вещество. Вкус сладковатый. Растворимость (в граммах на 100 граммов растворителя): в воде 179 (0 °C) и 487 (100 °C), в этаноле 0,9 (20 °C). Малорастворима в метаноле. Не растворима в диэтиловом эфире.
Химические свойства
1. Гидролиз сахарозы
С12Н22О11 + Н2О → С6Н12О6 + С6Н12О6
Вывод: гидролиз происходит при нагревании и в присутствии минеральных кислот (Н2SO4). При этом образуется глюкоза и фруктоза.
Образование глюкозы свидетельствует выделению кирпично–красного осадка в реакции с Cu(OH)2, так как в глюкозе есть альдегидная группа, а в сахарозе нет.
Крахмал
1. Строение молекулы глюкозы
(С6Н10О5)n
Крахмал – природный полимер, то есть высокомолекулярное соединение. Мономером является
α – глюкоза.
Физические свойства
По внешнему виду – белый порошок. В воде не растворим. В горячей воде набухает и образует клейстер.
Химические свойства
1. Качественная реакция на крахмал
Реакция с йодной водой
Наблюдается темно-синее окрашивание
2. Гидролиз крахмала
(С6Н10О5)n + nН2О → nС6Н12О6
Крахмал подвергается гидролизу при нагревании и в присутствии минеральной кислоты с образованием глюкозы
При нанесении йода на продукт реакции синее окрашивание не наблюдается.
Целлюлоза