-Алкенами называются ненасыщенные ациклические углеводороды, молекулы которых содержат одну двойную связь.
-Атомы углерода, связанные двойной связью С=С, находятся в состоянии
sp2-гибридизации, двойная связь - сочетание σ (сигма) и π (пи) - связей.
-Наличие слабой π (пи) - связи делает алкены более активными - способны вступать в реакции присоединения.
Изомерия алкенов (одинаковая молекулярка и состав, разное строение).
-Названия олефинов образуются заменой окончания "ан" в названии алканов на "ен"; входят в состав жидких жиров - масел, отсюда второе название - олефины.
-цифры перед назв. указывают положение двойной связи, например:
СН3 — СН=СН — СН2 — СН3 пент ен-2.
-Для низших членов гомологического ряда сохранились названия с окончанием "илен": этилен (два ат.С), пропилен(три ат.С) и др.
-Углеводородные радикалы (УВ-R), образованные от алкенов имеют суффикс «-енил». Тривиальные названия: CH2=CH— «винил», CH2=CH—CH2— «аллил».
1.Изомерия положения при смене места двойной связи:
СН3 — СН=СН — СН2 — СН3 пент ен-2 и СН3=СН—СН — СН2 — СН3 пентен-1
Задание: постройте структурную формулу 3,4,4-триметилпентен-2
2. Геометрическая цис-, транс - изомерия некоторых алкенов:
Задание. 1. В виде цис - и транс-изомеров может существовать:
1)этилен; 2)пропилен; 3)бутен-1; 4)бутен-2
2. Цис-транс-изомерия возможна для:
1) гексена-2 2) бутина-1 3) 2,3-диметилпентана 4) 2,3-диметилбутена-2
3.Межклассовая изомерия:
Алк ен ы изомерны цикло алк ан ам у них тоже общая формула CnH2n.

Гомологический ряд этилена (одинаковое строение, разный количественный состав, то есть разная молекулярка):
-Неразветвлённые алкены образуют гомологический ряд этена (этилена):
|
|
-Общая формула гомологического ряда алкенов СnН2n.
этен (этилен) C2H4 пропен C3H6 бутен C4H8 пентен C5H10
гексен C6H12 гептен C7H14 октен C8H16 нонен C9H18 децен C10H20
Получение алкенов:
1.Крекинг нефтепродуктов:
-Крекинг - превращение УВ, при высокой температуре (термический) или на катализаторе (каталитический).
- Крекинг алканов - важнейший промышленный способ получения алкенов из высококипящих фракций нефти.
Под действием сильного нагревания (до 700 °С) или каталитический крекинг на оксиде алюминия или кремния в молекулах алканов расщепляются σ -связи С—С, при этом образуется смесь низкомолекулярных алканов и алкенов:

гептан бутан пропен
Каталитический крекинг приводит и к изомеризации.
2.Дегидрирование предельных УВ (отщепление атомов водорода)Элиминирование. Атомы углерода при элиминировании переходят из sр3 - в sp2-гибридное состояние.Это один из промышленных способов получения алкенов. Температура: 350—450 °C, катализатор — Cr2O3. Также используются алюмомолибденовые и алюмоплатиновые катализаторы.

этан этен Чаще дегидрирование осуществляется на Pt или Ni катализаторе:
 3.Дегидратация спиртов (внутримолекулярная) осуществляется в присутствии концентрированной серной кислоты, она играет роль водоотнимателя:
3.Дегидратация спиртов (внутримолекулярная) осуществляется в присутствии концентрированной серной кислоты, она играет роль водоотнимателя:

-Если возможны два направления реакции у вторичных спиртов, то преимущественно идёт первая реакция по правилу Зайцева: Отщепление атома водорода в реакциях дегидрогалогенирования и дегидратации происходит преимущественно от наименее гидрогенизированного атома углерода. (Отнимание водорода идёт у и так бедного водородом атома углерода)
|
|
 4.Дегидрогалогенирование галогеналканов осуществляется также по правилу Зайцева. Уходит однозначно галоген, и уходит водород от углерода и так бедного водородом(бедный становится ещё беднее):
4.Дегидрогалогенирование галогеналканов осуществляется также по правилу Зайцева. Уходит однозначно галоген, и уходит водород от углерода и так бедного водородом(бедный становится ещё беднее):
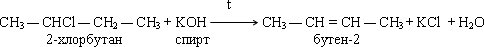

Запомнить: процесс идёт при действии спиртового раствора щёлочи (при действии водного раствора щёлочи получается другой продукт (одноатомный спирт - реакция замещения, а не отщепления).
5. Дегалогенирование. При действии цинка или магния на ди бром (хлор)производное алканов происходит отщепление атомов галогена у соседних атомов углерода и возникает двойная связь:

дибромпропан пропен
Дома: параграф №12 до химических свойств алкенов - учить.