Состав и строение молекул жиров.
Сложные эфиры могут образовываться разнообразными карбоновыми кислотами и спиртами. Наибольшее значение имеют те, которые образованы трёхатомным спиртом глицерином и высшими карбоновыми кислотами. К последним относятся, например, стеариновая кислота состава С17Н35СООН и олеиновая кислота состава С17Н33СООН.
Первая – предельная кислота, вторая – непредельная. В её углеводородном радикале имеется двойная связь между углеродными атомами, поэтому в молекуле олеиновой кислоты на два водородных атома меньше:
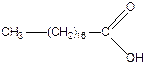
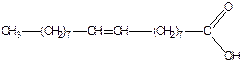
Стеариновая кислота Олеиновая кислота
Сложные эфиры карбоновых кислот и глицерина называются жирами. Если формулу
карбоновой кислоты записать в общем виде  , то образование жира
, то образование жира
можно представить уравнением реакции этерификации:
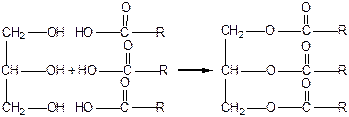
Глицерин Карбоновая кислота Жир
Химическую природу жиров начали изучать в первой половине XIX в. Синтез жира тристеарина впервые осуществил французский химик М. Бертло в 1854 г.
Физические свойства жиров. Состав и строение углеводородных радикалов влияют на свойства жиров. Вот как, например, изменяются их температуры плавления:
| Радикал | Название жира | Тпл, °С |
| ― С17Н35 | Тристеарин | |
| ― С17Н35 | Триолеин | - 4 |
Как видим, жир, образованный предельной кислотой, в обычных условиях твёрдый, непредельной – жидкий. В состав жидких растительных масел (подсолнечного, кукурузного, оливкового и др.) входят остатки преимущественно непредельных кислот, в состав твёрдых животных жиров (говяжьего, бараньего и др.) – остатки предельных кислот.
Жиры легче воды и нерастворимы в ней, но растворяются в органических растворителях.
Жиры наряду с белками и углеводами принадлежат к биологически активным веществам. Они входят в состав клеток растительных и животных организмов и являются для них источником энергии. В результате окисления 1 г жира выделяется
37,7 кДж энергии, вдвое больше, чем при окислении 1 г белка или углевода.
Основное количество жиров, употребляемых человеком, содержится в мясе, рыбе, молочных и зерновых продуктах. В случае когда в организм человека с едой поступает больше энергии, чем используется им, образуются жирообразные вещества, отлагающиеся в тканях организма. Таким образом он аккумулирует энергию.
В соответствии с данными современной медицины чрезмерное употребление жиров, образованных предельными кислотами, то есть животных жиров, может привести к накоплению веществ, затрудняющих ток крови в артериях, в частности тех, которые поставляют кровь в мозг. Более полезными для употребления признаются жиры, образованные непредельными кислотами, то есть растительные масла. В составе, например, подсолнечного масла содержится 91% непредельных карбоновых кислот.
Химические свойства жиров.
В молекулах жидких жиров в отличие от твёрдых имеются двойные углерод – углеродные связи. Как вам уже известно, по месту двойной связи возможна реакция присоединения, в частности водорода. В результате этой реакции непредельное соединение превращается в предельное, а жидкий жир – в твёрдый.

Триолеин Тристеарин
Процесс отвердевания (гидрирования) жиров лежит в основе производства маргарина (от греч. слова, означающего жемчужина). Негидрированные жиры прогоркают, окисляясь по двойным связям, у них появляются неприятные запах и вкус. Гидрирование жиров замедляет эти процессы, кроме того, позволяет из более дешёвых растительных масел получать более ценные твёрдые жиры.
Жиры как сложные эфиры подвергаются гидролизу.
Жиры гидролизируют с образованием трёхатомного спирта глицерина и карбоновых кислот.
Если проводить гидролиз тристеарина в присутствии щёлочи, образуется соль стеариновой кислоты, известная как основа мыла:
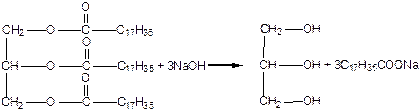
Поскольку в результате щёлочного гидролиза жира образуется мыло, то реакция называется омылением жира.
Натриевые соли высших карбоновых кислот – основная составная часть твёрдого мыла, соли калия – жидкого мыла.
Для получения мыла из жира в промышленности вместо щёлочи используют соду Na2CO3. Мыло, полученное непосредственно в результате этой реакции, называется ядровым и известно как хозяйственное. Туалетное мыло отличается от хозяйственного наличием добавок: красителей, ароматизаторов, антисептиков и др.
Основным компонентом твёрдого мыла является смесь растворимых солей высших жирных кислот. Обычно это натриевые, реже — калиевые и аммониевые соли таких кислот, как стеариновая, пальмитиновая, миристиновая, лауриновая и олеиновая.
Один из вариантов химического состава твёрдого мыла — C17H35COONa (жидкого — C17H35COOK).
Моющее действие мыла – сложный физико-химический процесс. Мыло является посредником между полярными молекулами воды и неполярными частицами загрязнений, нерастворимыми в воде. Если обозначить углеводородный радикал буквой R, то состав мыла можно выразить формулой R – COONa. По химической природе мыло – это соль, ионное соединение. Кроме полярной группы –COONa в его составе имеется неполярный радикал R, в состав которого могут входить 12-17 атомов углерода. Во время мытья молекулы ориентируются на загрязнённой поверхности таким образом, что полярные группы обращены к полярным молекулам воды, а неполярные углеводородные радикалы – к неполярным частицам загрязнения. Последние как бы попадают в окружение молекул мыла и легко смываются с поверхности водой.
В жёсткой воде образуются нерастворимые магниевые и кальциевые соли карбоновых кислот, поэтому мыло теряет своё моющее действие, а соли оседают на поверхности изделия:
2C17H35COONa + MgSO4 → (C17H35COO)2Mg↓ + Na2SO4
Синтетические моющие средства, при всём разнообразии их химического состава, имеют подобное мылу строение молекул, в которых есть растворимая в воде полярная часть и нерастворимый углеводородный радикал. Но они, в отличие от мыла, являются солями другой химической природы и в жёсткой воде не образуют нерастворимых соединений. В этом состоит преимущество синтетических моющих средств перед обыкновенным мылом.
Мыло и синтетические моющие средства принадлежат к так называемым поверхностно-активным веществам (ПАВ). Их широкое применение часто связывают с загрязнением окружающей среды, в частности водоёмов. Дело в том, что к синтетическим моющим средствам добавляют фосфаты, которые в водоёмах превращаются в вещества, питающие микроорганизмы, бурное размножение которых может привести к заболачиванию водоёмов. Поэтому современные ПАВ должны химически или биологически разлагаться после использования на безопасные вещества, не загрязняющие стоки.