Производство нитроаммофоски
«Химическая технология»
Выполнила:
Студентка группы 9651
Полежаева Е.А.
«__» ______ 2012 г.
Преподаватель:
Петухова Е. А.«__» ______ 2012 г.
Содержание.
1.Введение………………………………………………………………………………………………………….3
2.Характеристики нитроаммофоски…………………………………………………………………..4
3.Основные физико-химические свойства…………………………………………………………4
4.Сырьё для производства нитроаммофоски…………………………………………………….6
5. Технологическая схема производства нитроаммофоски………………………………9
6.Материальный расчет………………………………………………………………………………………12
7.Заключение……………………………………………………………………………………………………….19
8.Список литературы……………………………………………………………………………………………20
Введение.
Минеральные удобрения — неорганические соединения, содержащие необходимые для растений элементы питания.
Минеральные удобрения содержат питательные вещества в виде различных минеральных солей. В зависимости от того, какие питательные элементы содержатся в них, удобрения подразделяют на простые и комплексные. Простые (односторонние) удобрения содержат один какой-либо элемент питания. К ним относятся фосфорные, азотные, калийные и микроудобрения. Комплексные, или многосторонние, удобрения содержат одновременно два или более основных питательных элемента.
В почвах обычно имеются все необходимые растению питательные элементы. Но часто отдельных элементов бывает недостаточно для удовлетворительного роста растений. На песчаных почвах растения нередко испытывают недостаток магния, на торфяных почвах – молибдена, на черноземах – марганца и т. п. Применение минеральных удобрений – один из основных приемов интенсивного земледелия. С помощью удобрений можно резко повысить урожаи любых культур на уже освоенных площадях без дополнительных затрат на обработку новых земель.
Для внесения минеральных удобрений используются туковые сеялки.
Минеральные удобрения бывают азотными, фосфорными, калиевыми, сложными и микроудобрениями. Они являются продукцией химического производства и содержат в себе одно или несколько питательных веществ в высокой концентрации.
Характеристика азофоски.
Азофоска- высокоэффективное концентрированное трехкомпонентное удобрение (N:P2O5:K2O =1:1:1); реакция в почвенных водах – слабокислая, применяется на всех почва, под все сельскохозяйственные культуры.
Основные физико-химические свойства.
Насыпная плотность, т/м3 …………………………………………………………………...1,0….1,05
Угол естественного откоса…………………………………………………………………….40
Гигроскопическая точка, % при содержании воды, %:
0,2…………………………………………………………………………………………………………..49,6
0,6……………………………………………………………………………………………………….….52,1
0,9……………………………………………………………………………………………………..……54,0
Температура плавления, С ……………………………………………………………..……170…190
Азофоска не токсична, не взрывоопасна, способна к очаговому терморазложению от источников тепла, имеющих температуру выше 1900С. Так как терморазложение не переходит в горение, азофоска относится к трудногорючим веществам. Ориентировочный состав азофоски, %:
Моно- и диаммонийфосфаты NH4H2PO4, (NH4)2HPO4 -23,2
Дикальцийфосфат CaHPO4 -4,5
Нитрат аммония NH4NO3 -39,0
Хлорид калия KCl -27,5
Фторид кальция CaF2 -5,3
Вода H2O -0,5
Продукт должен удовлетворять следующим техническим требованиям:
Массовая доля питательных веществ в сумме, %....................................≥49
Содержание азота (N), %............................................................................≥16
Содержание фосфора(P2O5), %..................................................................≥16
в том числе водорастворимого P2O5, %.................................................≥13,5
Содержание калия (K2O), % …………………………………………………………………..≥16
Содержание влаги (H2O), %.......................................................................≤0,6
Гранулометрический состав, %:
>4мм……………………………………………………………………………………………………….≤3
От 1 до 4мм…………………………………………………………………………………………….>94
<1мм………………………………………………………………………………………………………..≤3
Прочность гранул на раздавливание, кгс/см3……..≥20
Азофоска гигроскопична. Для уменьшения слёживаемости, гранулы должны обрабатываться 45% раствором диспергатора НФ и опудриваться диатомитом.
Удобрение транспортируется упакованное в полиэтиленовые мешки или навалом.
Сырьё для производства нитроаммофоски.
Сырьем для производства азофоски являются апатитовый концентрат, азотная кислота, жидкий аммиак, хлорид калия, диоксид углерода, карбамид, диспегатор НФ-жидкий, диатомит.
Кольский апатитовый концентрат- лучшее в мире фосфатное сырьё. Он до сих пор является основным сырьём для производства концентрированных фосфорных и сложных удобрений.
Нефелиновый концентрат является лишь побочным продуктом. Коммерческое значение его во много раз ниже, нежели чем апатитового концентрата. Однако во многих случаях нефелиновый концентрат является удобным для использования продуктом. Нефелин (или элеолит) — породообразующий минерал, алюмосиликат калия и натрия ортокремниевой кислоты (Na,K)AlSiO4. Используют в производстве алюминия, соды, в стекольной, кожевенной промышленности. В больших количествах получается в качестве отхода при добыче апатита.
Апатитовый концентрат Ca5F(PO4)3 (ГОСТ 22275-76) должен содержать, %:
P2O5……………………………………………………………………………………………………….≥39,4
H2O………………………………………………………………………………………………….…….≤1,0
Fe2O3, Al2O3………………………………………………………………………………………….…≤3,0
MgO…………………………………………………………………………………………………..……≤0,23
Крупность концентрата не должна превышать 11,5% остатка на сите с сеткой № 016(размер ячеек 0,16мм). Плотность 3,1т/м3. Насыпная плотность 1,5…1,8т/м3.
Молекулярная масса 504,3.
Азотная кислота HNO3 (ГOCТ 6-03-270-76) представляет собой бесцветную или слегка желтоватую жидкость. Она является сильным окислителем. Все металлы, кроме платины, золота и титана, растворяются в азотной кислоте, образуя соответствующие оксиды или нитраты. Азотная кислота сильно дымится на воздухе, выделяя оксиды азота, которые с влагой образуют туман.
Молекулярная масса 63,02. Применятся азотная кислота –не менее 57% (высший сорт) и не менее 56%(1 сорт) с содержанием оксидов азота в пересчете на N2O4- не более 0,07 %, прокаленного остатка- не более 0,004%.
Жидкий аммиак технический NH3 (ГОСТ 6221-82) Молекулярная масса 17,03. Применяется аммиак 99,6% (марка Б) и 99,6%(марка А) с содержанием масла не более 8мл/г, влаги –не более 0,4%; железа- не более 2 мг/л.
Аммиак при нормальной температуре и атмосферном давлении находится в газообразном состоянии. Газообразный аммиак относится к горючим газам. Температура его самовоспламенения 6500С. На производство поступает жидкий аммиак, а в техническом процессе используется газообразный аммиак и его водные растворы.
Хлорид калия KCl (ГОСТ 4568-83)- кристаллический порошок серовато-белого или красно-бурого цвета. Массовая доля хлорида калия – не менее 95%, в пересчете на K2O – не менее 60%, воды- не более 1%. Молекулярная масса 74,55. Применяется в сельском хозяйстве как самостоятельное удобрение и используется в промышленности при производстве сложных удобрений.
Углекислый газ (диоксид углерода) CO2(ГОСТ 8050-76)- бесцветный газ, без запаха, тяжелее воздуха в полтора раза, плохо растворяется в воде. В производстве фзофоски используется газ марки «технический».
Карбамид CO(NH2)2 (ГОСТ 2081-75) представляет собой гранулы белого цвета, хорошо растворимые в воде. Молекулярная масса 60,05. В производстве азофоски карбамид добавляют на стадии разложения апатитового концентрата азотной кислотой для уменьшения выделения оксидов азота в газовую фазу.
Диспергатор НФ технический (ГОСТ 6848-79) марки Б- продукт конденсации сульфокислот нафталина с формальдегидом, нейтрализованный аммиачной водой, представляет собой жидкость коричневого цвета, в которой допускается наличие осадка. Массовая доля активного вещества в пересчете на сухой продукт оставляет не менее 4,5%, воды – не более 57%. Плотность 1,16г/см3.
Диатомит –беловато-серый порошок. Массовая доля SiO2- не менее 90%, влаги- не более 2%. Кроме диоксида кремния содержит оксиды кальция и магния. В мировой практике диатомитовый порошок считается наиболее эффективной опудривающей добавкой.
Кондиционирование азофоски диатомитом, наносимым на гранулы в количестве 2% от их массы, позволяет сохранить её сыпучесть даже после шестимесячного хранения.
Технологическая схема производства нитроаммофоски.
Технологическая схема производства нитроаммофоски с применением аммонизатора-гранулятора приведена на рис. 22.
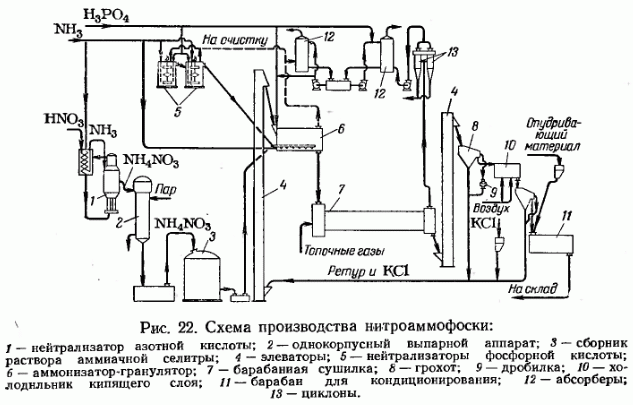
Азотная (47%-ная) и фосфорная (32—54% Р2О5) кислоты из напорных баков через дозаторы подаются соответственно в нейтрализаторы 1 и 5. Газообразный аммиак поступает на нейтрализацию фосфорной кислоты при 8°С и избыточном давлении 0,25—028 Мн/м2 (2.5—2,8 кгс/см2).
Процесс нейтрализации проводят в течение 1,5—2 ч в аппаратах с мешалками при температуре 110—125oС в первой ступени и 105—115 oС во второй до рН раствора 5—5,5 (мольное отношение NH3: Н3РO4 = 1,3—1,4: 1). При этом из раствора испаряется до 40% воды.
В зависимости от концентрации и степени подогрева азотной кислоты процесс ее нейтрализации проводят при 110—135°С и избыточном давлении 15— 20 кН/м2 (0,15—0,2 кгс/см2). Выходящий из нейтрализатора 1 раствор аммиачной селитры подвергают донейтрализации путем добавления NH3 или HNO3. Далее раствор центробежным насосом передают на упаривание в одно- или двухступенчатый выпарной аппарат 2 пленочного типа. Здесь раствор упаривается до концентрации 90—95% NH4NO3, после чего поступает в сборник 3. Отсюда плав аммиачной селитры при 165—175oC. центробежным насосом подается в аммонизатор-гранулятор 6, куда вводятся также раствор моноаммонийфосфата из нейтрализатора 5, хлористый калий, ретур и газообразный аммиак (под сдой гранулируемой смеси). Аммиак подается в количестве 105—110% от стехиометрической нормы, необходимой для полной нейтрализации второго водородного иона фосфорной кислоты.
При температуре 70-85oС и продолжительности пребывания смеси в аппарате примерно 10 мин степень нейтрализации фосфорной кислоты аммиаком в смеси соответствует отношению NH3: H3PO4=1,8—2. В этих условиях процесс гранулирования протекает удовлетворительно при содержании в смеси 4—6% влаги и кратности ретура 3,5—5. Одновременно с нейтрализацией н гранулированием в аммонизаторе-грануляторе происходит частичная подсушка смеси за счет тепла химических реакций, в результате чего в аппарате А-Г удаляется 10—15% воды, вводимой с сырьем, ретуром и растворами.
Из аммонизатора-гранулятора продукт, содержащий 2,5% влаги и более, направляется в барабанную сушилку 7 (диаметр 5 м, длина 40 м, общий объем 785 м3). Для сушки продукта используются топочные газы, температура которых на входе составляет 250—350°С, на выходе 110—130°С. Из сушилки продукт при влажности не более 0,5% и температуре 86—95 °С подастся элеватором на грохота 8 для рассева на три фракции: товарную (размеры гранул 2—4 мм), крупную (более 4 мм) и мелкую (менее 2 мм). Товарная фракция далее поступает па охлаждение, мелкая и крупная фракции после дробилки 9 возвращаются в качестве ретура в процесс.
Товарная фракция охлаждается с 80—95 до 30—35oС в холодильнике барабанного типа или кипящего слоя. Охлажденный продукт после повторного рассева подается на кондиционирование в аппарат 11 барабанного типа. Для кондиционирования применяют опудривающие и омасливающие вещества, добавляемые в количестве 1,5—2% от массы продукта. В качестве опудривающих материалов обычно используют тонко измельченный каолин, кизельгур, доломит, известняк и др. Для омасливания применяют различные нефтепродукты, например парафинистый мазут. После кондиционирования продукт направляется на расфасовку и упаковку в полиэтиленовые или битумированные крафтцеллюлозные мешки.
Удобрения содержат не менее 95% P2O5 в водорастворимой форме, не более 0,5% влаги, выход товарной фракции (размеры гранул 2—4 мм) достигает 95%. Гранулы хорошо окатаны и имеют высокие показатели физико-химических и механических свойств.
Отходящие газы производства нитроаммофоски содержат до 0,1 г/м3 фтора, до 2 г/м3 аммиака и пыль, состав которой аналогичен составу удобрений. Для очистки газов после нейтрализаторов, выпарных аппаратов, аммонизатора-гранулятора предусматриваются абсорбционные аппараты типа полых скоростных скрубберов, работающих в замкнутом цикле с использованием для орошения технологической жидкости. Процессы производства диаммонитрофоса и диаммонитрофоски практически не отличаются от процессов получения нитроаммофоски. В первых двух случаях аммонизацию проводят более глубоко (на 85—95%).
Расчет материального баланса получения азотно- кислотной вытяжки разложения апатитового концентрата 45%-ой азотной кислотой, осаждения кремнефторида натрия из азотнокислотной вытяжки.
1. Определим количество образующихся продуктов с учетом степени извлечения компонентов.
Табл.1
| Согласно реакции 1 | |
| Образуется Ca(NO3)2 | 1000*0.518*0.98*164/56=1487.7кг |
| Образуется H3PO4 | 1000*0.394*0.98*2*98/142=532.8кг |
| Образуется HF | 1000*0.0303*0.95*20/19=30.22кг |
| Согласно реакции 2 | |
| Образуется Fe(NO3)2 | 1000*0.0084*0.7*2*242/160=17.77кг |
| Образуется Ge(NO3)3 | 1000*0.0095*0.98*2*326/328=18.46кг |
| Согласно реакции 3 | |
| Образуется H2SiF6 | 30.3*144/120=36.36кг |
| При этом расходуется SiO2 | 36.36*60/144=15.1кг |
Таким образом, на образование H2SiF6 расходуется все количество SiO2, находящееся в апатите:
1000*0.0151=15.1кг
2. Стадия осаждения Na2SiF6.
Количество HNO3,расходуемое на связывание избытка воды:
Na2CO3+2HNO3=2NaNO3+H2O+Co2
42.8*2*63/106=50.9кг
Табл.2
| При этом образуется NaNO3 | 42.8*2*85/106=68кг | |
| Количество H2O,кг | -образующейся при взаимодействии соды с H2SiF6 | 29.1*18/144=3.64кг |
| -образующейся при взаимодействии соды с HNO3 | 42.8*18/106=7.27кг |
Всего H2O: 3.64+7.27=10.91кг
Общее количество воды в растворе после осаждения кремнефторида натрия (без учета воды в пульпе):
256.92+10.91=267.83кг
Количество углекислого газа,кг:
-выделившегося при образовании кремнефторида натрия
29.09*44/144=8.89кг
-выделившегося при образовании нитрата натрия
42.82*44/106=17.77кг
Всего СО2: 8.89+17.77=26.66кг
Количество оставшейся свободной азотной кислоты:
58.3-50.9=7.4кг
3. Определим количество кремнефторида натрия
Na2CO3+2HNO3=2NaNO3+H2O+Co2
Прореагирует H2SiF6 c содой
36.36*0.8=25кг
Останется H2SiF6 в растворе:36.36-29=7.36кг
Образуется Na2SiF6: 29*188/144=38кг
Количество соды, потребной для осаждения Na2SiF6
29*106/144=21.4 кг
Расход соды с учетом применяемого избытка ее в 200% будет:
21.4+21.4*2=64.2кг
Или в виде 20% раствора Na2CO3
64.2/0.2=321кг
С этим раствором поступает воды:
321-64.2=256.8 кг
4.Количество 100%-ой HNO3
По реакции 1: 1487.7*2*63/164=1143кг
По реакции 2: 17.77*6*63/2*326=10.7кг
Таким образом, всего на реакции расходуется HNO3 :
1143+13.9+10.7=1167.6кг
Учитывая, что разложение ведется при 5%-ом избытке HNO3,необходимо ввести кислоты:
1167*6*1.05=1226кг
Принимая потерю HNO3, в процессе равной 1% от теоретического расхода, находим сколько всего потребуется кислоты:
1167.6*1.06=1237.6кг
Потеря кислоты составляет:
1237.6-1226=11.6кг
Количество 45% кислоты, которое нужно ввести в процесс, будет:
1237.6/0.45=2750.0кг
Остается свободной HNO3 в системе:
1237.6-1167.6-11.6=58.4кг
5.Количество воды, 6находящейся в системе, поступает с азотной кислотой:
2750.0-1237.6=1512кг
Образуется воды согласно реакции 2:
(1000*0.0084*0.7*3*18)/160=2 кг
И (1000*0.0095*0.98*3*18)/328=1.5кг
Образуется воды согласно реакции 3 в результате связывания 30.2 кг HF в H2SiF6
30.22*2*18/6*20=9.1кг
С апатитовым концентратом поступает воды:
1000*0.005=5.0кг
Таким образом, общее количество воды поступает в систему:
1512.4+2.0+1.5+9.1+5.0=1530.0кг
6. В результате разложения апатита азотной кислотой образуется:
Табл.3
| жидкая фаза: | Твердая фаза: |
| HNO3-58.4кг H3PO4-532.8кг Ca(NO3)2-1487.7кг Fe(NO3)2-17.77кг Ge(NO3)2-18.46кг H2SiF6-36.36кг H2O-1530.0кг | CaO 518*0.02=10.36кг P2O5 394*0.02=7.88кг F 30.3*0.05=1.51кг Ge2O3 9.5*0.02=0.19кг Fe2O3 8.4*0.3=2.52кг H2O 1000*0.0197=19.7кг |
| Всего 3681.49кг | Всего 42.16кг |
Потери 100%-ой азотной кислоты составляют 11.6кг, количество теряемой вместе с азотной кислотой воды определяется по разности между общим приходом материалов и вычисленным количеством уходящих продуктов.
Всего поступает в процесс:
1000+2750=3750кг
Всего уходит из системы:
3681.49+42.16+11.6=3735.25кг
В том числе АКВ: 3735.25-11.6=3723.65кг
Таким образом, теряется вода в парах вместе с азотной кислотой:
3750-3735.25=14.75кг
Табл.4
| приход | кг | расход | кг |
| Азотнокислое разложение: -апатитовый концентрат -45%-ая азотная кислота в том числе HNO3 H2O Осаждение Na2SiF6 из АКВ: H2SiF6 100% HNO3 Сода Вода с раствором Na2CO3 Всего | 1237.6 1512.4 3.64 58.3 64.2 256.9 4133.04 | 1.Азотнокислотная вытяжка: Ж.фаза Т.фаза Пары в том числе HNO3 H2O 2.Na2SiO3 NaNO3 H2O CO2 100% HNO3 H2SiF6 Всего | 3681.49 42.16 11.6 14.75 267.83 17.77 10.9 26.66 58.4 3.64 4135.2 |
Неувязка баланса:
((4135.2-4133.04)/4133.04)*100%=0.053%
Заключение:
В ходе курсовой работы мы составили материальный расчет получения азотно- кислотной вытяжки разложения апатитового концентрата 45%-ой азотной кислотой, осаждения кремнефторида натрия из азотнокислотной вытяжки.
Список используемой литературы:
1. Кочетков В.Н «Гранулирование минеральных удобрений»
2. Артюшин А.М., Державин Л.М. Краткий словарь по удобрениям.-М.1984
3. Штефан В.К. Жизнь растений и удобрений,М -1981
4. Основы земледелия и растениеводства. / Под редакцией Никляева В.С. - Москва, 1990.
5. Сельскохозяйственная энциклопедия. В 5 т. Т.1,2,3,4,5 /: Редкол.: Аверьянов С.Ф., Бараев А.И. и др. (Гл. ред. Мацкевич В.В. И Лобанов П. П) - М.: Сов. Энциклопедия. 1969.
6. Дудина Н.Х. и др. Агрохимия и система удобрения. - 3-е изд-е., перераб. и доп. - М.: Агропромиздат, 1991.