АЗОТСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ.
Нитросоединения.
Нитросоединениями называют органические вещества, содержащие одну или несколько нитрогрупп (– NO2).
Получение нитросоединений.
Нитросоединения получают при нитровании органических веществ в присутствии или без участия серной кислоты.
СН4 + HNO3 → CH3NO2 + H2O
Химические свойства.
При восстановлении нитросоединений образуются первичные амины.
CH3NO2 + 3H2 → CH3NH2 + 2H2O
АМИНЫ•
Аминами называет органические производные аммиака, в котором один, два или все три атома водорода замещены на углеводородный радикал.
Классификация и номенклатура аминов.
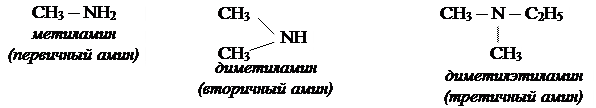
Физические свойства аминов.
Метиламин, диметиламин, триметиламин и этиламин - газообразные вещества. Следующие представители гомологического ряда - жидкости, а высшие амины - твердые вещества. Газообразные и жидкие амины обладают запахом, напоминающим запах аммиака.
Химические свойства аминов.
1. Основные свойства аминов.
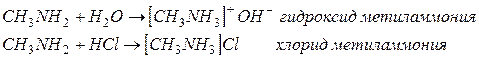
2. Горение.
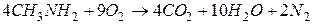
Получение аминов.
1. Восстановление нитросоединений.
C2H5NO2 + 3H2 → C2H5NH2 + 2H2O
2. Взаимодействие галогенпроизводных с аммиаком.
C2H5Cl + NH3 → C2H5NH2 + HCl
Применение аминов.
Амины широко применяются в органическом синтезе. Они служат промежуточными продуктами синтеза лекарственных средств, синтетических волокон, пластмасс, стимуляторов роста растений.
Нахождение в природе. Природные амины животного происхождения: адреналин, норадреналин, серотонин, гистамин, тирамин - участвуют в регуляции центральной нервной, пищеварительной, эндокринной, сердечно-сосудистой и других систем.
Амины растительного происхождения - алкалоиды, характеризующиеся высокой физиологической активностью.
Упражнение.
Составьте уравнения реакций по схеме:
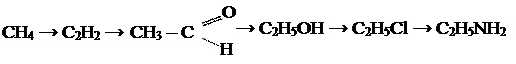
АНИЛИН.
Строение молекулы.

Физические свойства.
Маслянистая жидкость, бесцветная, но быстро темнеющая на воздухе, в воде малорастворим, ядовит.
Химические свойства.
1. Основные свойства.
C6H5NH2 + H2O → [C6H5NH3]OH
гидроксид фениламмония
C6H5NH2 + HCl → [C6H5NH3]Cl
хлорид фениламмония
2. Реакция замещения.
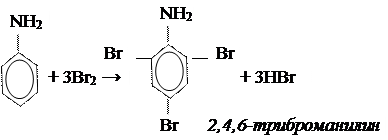
3. Горение.
4C6H5NH2 + 31О2 → 24СО2 + 14H2O + 2N2
Получение анилина.
1. Реакция Зинина.
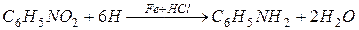
2. Реакция Зайцева.
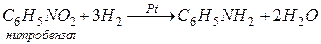
Анилин используется для получения лекарств, красителей, взрывчатых веществ.
АМИНОКИСЛОТЫ.
Аминокислотами называют органические соединения, а молекулах которых содержатся карбоксильная группа (– СООH) и аминогруппа (– NH2). По взаимному расположению функциональных групп выделяют α-, ß-, γ- и т.д. аминокислоты. Наибольшее значение среди аминокислот имеют α-аминокислоты, которые широко распространены в природе и, будучи составными частями белков, участвуют в процессах жизнедеятельности организмов. Из природных объектов выделено около 200 аминокислот
Строение и номенклатура аминокислот.
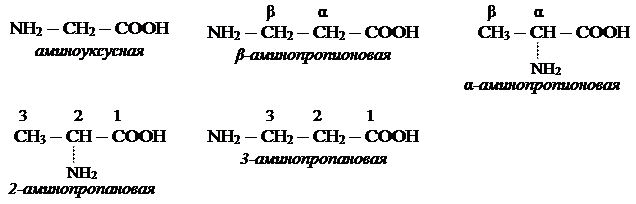
Физические свойства.
Аминокислоты представляет собой белые, кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом.
Химические свойства.
1. Амфотерные свойства аминокислот.
NH2 – CH2 – COOH + NaOH → NH2 – CH2 – COONa + H2O
NH2 – CH2 – COOH + HCl → [NH2 – CH2 – COOH]+Cl-
1. Образование сложных эфиров.
NH2 – CH2 – COOH + C2H5OH → NH2 – CH2 – CO – O – C2H5 + H2O
2.  Реакция конденсации
Реакция конденсации
|

Получение аминокислот.
1. Взаимодействие галогенпроизводных карбоновых кислот с аммиаком.
Cl – CH2 – COOH + NH3 → NH2 – CH2 – COOH + HCl
2. Гидролиз белков.
Применение аминокислот.
Аминокислоты и их производные используют в качестве лекарств. Синтетические аминокислоты - сырье для производства полиамидных синтетических волокон и изделий из этих полимеров. В организме человека многие из аминокислот синтезируются в печени. Однако некоторые из них не могут быть синтезированы в организме, поэтому человек обязательно должен получать их с пищей. К таким незаменимым аминокислотам относятся: гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, треонин, триптофан, валин. Аминокислоты, которые синтезируются в печени (заменимые): аланин, аргинин, аспарагин, аспарагиновую кислоту, цитруллин, цистеин, гамма-аминомасляную кислоту, глютамовую кислоту, глютамин, глицин, орнитин, пролин, серин, таурин, тирозин.
(*сделать сообщение о любой аминокислоте на доп. оценку: формула, значение, содержание в продуктах питания)
БЕЛКИ.
Белками называют природные полимеры, состоящие из большого числа остатков α-аминокислот, связанных между собой пептидными связями.
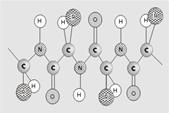
Строение белка.
| Первичная структура белка – последовательность чередования аминокислотных остатков (все связи ковалентные, прочные) | |||
| Вторичная структура – форма полипептидной цепи в пространстве. Белковая цепь закручена в спираль (за счет множества водородных связей) | |||
| Третичная структура – реальная трехмерная конфигурация, которую принимает в пространстве закрученная спираль (за счет гидрофобных связей), у некоторых белков – S–S-связи (бисульфидные связи) | |||
| Четвертичная структура – соединенные друг с другом макромолекулы белков образуют комплекс | |||
 1 1
| 
| 
| 
|
Физические свойства белков.
Молекулы фибриллярных белков вытянуты в длину, это основной строительный материал сухожилий, мускульных и покровных тканей. Такие белки в воде не растворимы.
Глобулярные белки свернуты в клубочки. Глобулярные белки растворимы в воде либо в растворах кислот или оснований.