Газовые законы.
Из уравнения Менделеева-Клапейрона можно вывести ряд законов, справедливых для идеальных газов и полученных экспериментально.
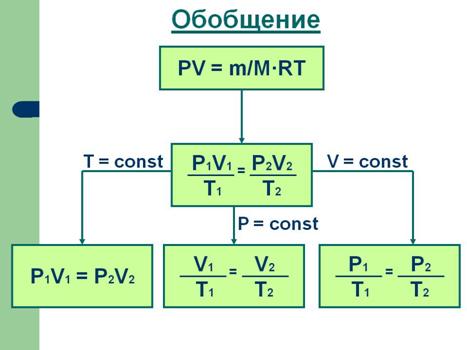
Закон Бойля – Мариотта: произведение численных значений давления р и объема V идеального газа постоянно, если температура Т и масса газа m не изменяются, т. е. при Т = const и m = const
pV = const.
Закон Бойля – Мариотта характеризует связь между давлением и объемом идеального газа в изотермическом процессе изменения его состояния.
Закон Гей–Люссака: при постоянном давлении объем V данной массы m идеального газа прямо пропорционален его абсолютной температуре Т, т. е. при р = const и m = const
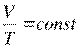 .
.
Закон Гей–Люссака характеризует связь между объемом и температурой идеального газа в изобарическом процессе изменения его состояния.
Закон Шарля: при постоянных объеме V и массе m идеального газа давление газа р прямо пропорционально его абсолютной температуре Т, т. е. при V = const и m = const
 .
.
Закон Шарля характеризует связь между давлением и температурой идеального газа в изохорическом процессе изменения его состояния.
Скорости теплового движения газовых молекул.
Все молекулы газа движутся с разными скоростями. Встречаются медленные молекулы, скорости которых близки к нулю. Встречаются очень быстрые молекулы, скорости которых во много раз превосходят средние скорости молекулярного движения. Между этими пределами скорости молекул с различной степенью вероятности принимают всевозможные значения. Закон распределения скоростей газовых молекул носит название распределения Максвелла, т. к. Максвелл теоретически решил задачу о распределении молекул идеального газа по скоростям поступательного движения.
Распределение Максвелла позволяет определить, какое число молекул DN из общего количества N молекул идеального газа обладает при данной температуре скоростями, лежащими в интервале от v до v + Dv. При этом Максвелл предполагал, что газ химически однороден и находится в состоянии термодинамического равновесия.
Закон распределения молекул по скоростям представлен на рисунке. По оси ординат отложена функция распределения молекул по скоростям

 ,
,
определяющая относительное число молекул 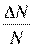 из общего числа N молекул, скорости которых лежат в интервале от v до v + Dv.
из общего числа N молекул, скорости которых лежат в интервале от v до v + Dv.
Эта функция имеет максимум при значении
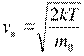 ,
,
называемом наиболее вероятной скоростью. Большинство молекул газа движется с наиболее вероятной скоростью, тогда как число молекул, имеющих очень малые и очень большие скорости, мало.
Площадь, ограниченная графиком функции и осью v, дает полное число молекул.
Закон распределения молекул по скоростям позволяет также подсчитать величину средней (средней арифметической) скорости  поступательного движения молекул идеального газа. Ее можно найти, поделив сумму скоростей молекул на их число:
поступательного движения молекул идеального газа. Ее можно найти, поделив сумму скоростей молекул на их число:
 .
.
Наконец, с помощью данного распределения можно найти среднюю квадратичную скорость. Так называется величина
 ,
,
т. е. квадратный корень из среднего значения квадрата скорости поступательного движения молекулы. Для вычисления 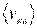 надо скорость каждой молекулы возвести в квадрат, сложить полученные значения и сумму разделить на общее число молекул:
надо скорость каждой молекулы возвести в квадрат, сложить полученные значения и сумму разделить на общее число молекул:
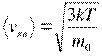 .
.
Таким образом, существуют три скорости, характеризующие состояние газа – наиболее вероятная, средняя арифметическая и средняя квадратичная.
Отметим, что закон распределения Максвелла представляет собой статистический закон, полученный с помощью методов теории вероятностей, а потому тем более точный, чем большее число молекул N рассматривается. Важно подчеркнуть, что данный закон справедлив только для хаотического теплового движения молекул идеального газа.
Задание: 1)Конспект
2) Ответить на вопросы: 20-25

3) решить задачи

Определить плотность гелия при температуре 15 градусов цельсия и давлении 98 кПа.