После окончания опытов первого варианта строят график зависимости удельной электропроводности от концентрации 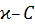 и объясняют полученную зависимость. Во втором варианте дают объяснение причин отклонения k от аддитивности. Данные опытов третьего варианта выражают графически
и объясняют полученную зависимость. Во втором варианте дают объяснение причин отклонения k от аддитивности. Данные опытов третьего варианта выражают графически 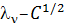 . Затем, экстраполируя полученные прямые на
. Затем, экстраполируя полученные прямые на  , находят предельные электропроводимости
, находят предельные электропроводимости 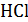 ,
,  и
и  . Величину
. Величину  можно найти, используя опытные данные, по закону независимого движения ионов.
можно найти, используя опытные данные, по закону независимого движения ионов.
Отчет включает в себя следующие разделы: теоретическую часть, цель работы, схему установки, описание методики измерения, таблицу результатов измерений, графики зависимостей 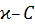 , расчет эквивалентной электропроводности, график зависимости
, расчет эквивалентной электропроводности, график зависимости 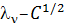 и определение электропроводности в бесконечно разбавленном растворе (при
и определение электропроводности в бесконечно разбавленном растворе (при  ), расчет
), расчет  по закону независимого движения ионов.
по закону независимого движения ионов.
Лабораторная работа 7.
Определение растворимости труднорастворимых солей
Концентрация растворов труднорастворимых солей обычно столь мала, что можно считать эквивалентную электропроводность таких растворов равной электропроводности при бесконечном разведении. В этом случае коэффициент активности  .
.
Так как удельная электропроводность таких растворов  весьма мала, то при ее определении приходится учитывать электропроводность воды
весьма мала, то при ее определении приходится учитывать электропроводность воды  . Таким образом:
. Таким образом:
 . (3.16)
. (3.16)
Эквивалентная электропроводность соли равна
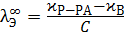 . (3.17)
. (3.17)
В соответствии с законом независимого движения ионов в бесконечно разбавленных растворах выполняется равенство  . Значения предельных подвижностей отдельных ионов представлены в справочниках. Тогда растворимость соли определяется по следующему уравнению
. Значения предельных подвижностей отдельных ионов представлены в справочниках. Тогда растворимость соли определяется по следующему уравнению
 . (3.18)
. (3.18)
Иными словами, измерив удельную электропроводность раствора и чистой воды и воспользовавшись табличными данными для ионных электропроводностей, можно определить растворимость труднорастворимой соли.
Цель работы – определение растворимости труднорастворимых солей.
Экспериментальная часть
Первоначально определяют постоянную сосуда, измеряя сопротивление раствора хлорида калия известной концентрации, как описано в работе 6. Затем сосуд тщательно отмывают от хлорида калия и измеряют электропроводность воды. Это определение проводят 3-4 раза (каждый раз с новой порцией воды), пока не получится хорошая воспроизводимость результатов. Особое внимание следует обратить на чистоту воды: ее удельная электропроводность должна быть близка к  Ом-1. см-1.
Ом-1. см-1.
Для приготовления насыщенного раствора исследуемую соль ( ,
,  ,
, 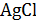 и др.), тщательно очищенную от примесей перекристаллизацией, растирают в фарфоровой ступке. Затем порошок соли всыпают в колбу, туда же приливают дистиллированную воду и в течение 15-20 мин взбалтывают суспензию при небольшом нагревании. Взвеси дают отстояться и раствор вливают в сосуд для измерений. С помощью моста переменного тока измеряют сопротивление исследуемого раствора.
и др.), тщательно очищенную от примесей перекристаллизацией, растирают в фарфоровой ступке. Затем порошок соли всыпают в колбу, туда же приливают дистиллированную воду и в течение 15-20 мин взбалтывают суспензию при небольшом нагревании. Взвеси дают отстояться и раствор вливают в сосуд для измерений. С помощью моста переменного тока измеряют сопротивление исследуемого раствора.