Метод кондуктометрического титрования основан на изменении электропроводности раствора в зависимости от прибавления к нему раствора другого электролита известной концентрации. Он может быть применен к изучению процессов, сопровождающихся изменением числа и природы ионов в растворе.
Если, например, к раствору кислоты постепенно добавлять щелочь, то электропроводность смеси сначала будет уменьшаться, потому что ион водорода ( См·см2/моль-экв) замещается менее подвижным катионом (
См·см2/моль-экв) замещается менее подвижным катионом (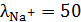 См·см2/моль-экв):
См·см2/моль-экв):
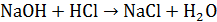 . (5.2)
. (5.2)
После нейтрализации дальнейшее прибавление щелочи вызывает увеличение электропроводности из-за избытка ионов гидроксила, имеющих большую электропроводность ( См·см2/моль-экв).
См·см2/моль-экв).
В общем случае при смешении растворов, содержащих ионы 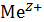 и
и 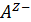 ,которые дают, соединяясь, нерастворимые (например,
,которые дают, соединяясь, нерастворимые (например, 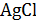 ) или плохо диссоциирующие (например,
) или плохо диссоциирующие (например, 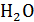 ) соединения, точка эквивалентности при титровании должна быть определена по перегибу кривой электропроводности (рис. 5.1). При этом возможны три варианта изменений электропроводности до достижения эквивалентной точки:
) соединения, точка эквивалентности при титровании должна быть определена по перегибу кривой электропроводности (рис. 5.1). При этом возможны три варианта изменений электропроводности до достижения эквивалентной точки:
1) она уменьшается;
2) остаётся постоянной;
3) увеличивается.
Помимо титрования чистых растворов (рис. 5.1), кондуктометрический метод может быть использован для титрования смеси сильных и слабых кислот (рис. 5.2) (или оснований). В этом случае кривая титрования имеет две точки перегиба: первая из них (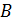 на рис. 5.2) соответствует эквивалентной точке сильной кислоты, вторая (
на рис. 5.2) соответствует эквивалентной точке сильной кислоты, вторая (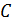 ) – слабой. Когда искривление линии нейтрализации сильной кислоты (
) – слабой. Когда искривление линии нейтрализации сильной кислоты (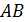 на рис. 5.2) очень велико, рекомендуется вести титрование в присутствии этилового спирта, подавляющего диссоциацию слабой кислоты.
на рис. 5.2) очень велико, рекомендуется вести титрование в присутствии этилового спирта, подавляющего диссоциацию слабой кислоты.
Титрование слабых двухосновных кислот, если их константы диссоциации достаточно сильно отличаются одна от другой, ведут аналогично титрованию смеси сильной и слабой кислот.

Рис. 5.1. Кривая кондуктометрического титрования
сильной кислоты сильной щелочью

Рис. 5.2. Кривая кондуктометрического титрования
смеси сильной и слабой кислот
Аналогично проходит титрование смеси серной кислоты и сульфата меди щелочью. В этом случае сначала происходит нейтрализация кислоты (электропроводность раствора сильно понижается). Затем свободная щелочь реагирует с сульфатом меди с образованием осадка гидрооксида 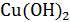 :
:
 . (5.3)
. (5.3)
При этом электропроводность изменяется незначительно. После осаждения меди избыточная щелочь обусловливает резкое возрастание электропроводности раствора.
Наиболее часто кондуктометрический метод применяют при титровании мутных и окрашенных растворов, которые анализировать обычным способом невозможно из-за подавления окраски индикатора. Следует иметь в виду, что накопление в титруемом растворе электролитов, принятых для титрования, снижает точность этого метода.
Цель работы – кондуктометрическое титрование сильной кислоты, смеси сильной и слабой кислот, смеси серной кислоты и сульфата меди, нитрата серебра.
Экспериментальная часть
Схема кондуктометрического титрования состоит из моста переменного тока типа Р-577 и гальванометра. Сосуд для измерения электропроводимости заменяется парой платиновых электродов, прочно скрепленных между собой и погруженных в стакан для титрования. Стакан устанавливается на титровальном столике с мешалкой. Бюретку емкостью 50 мл укрепляют на штативе, на том же штативе крепят электроды с таким расчетом, чтобы их можно было опускать в стакан и поднимать.
Схема питается переменным током постоянного напряжения. Бюретку емкостью 50 мл помещают на штативе; на нем же крепят электроды с таким расчетом, чтобы их можно было опускать в стакан и поднимать.
Определенное количество испытуемого раствора (10 мл) вливают пипеткой в стакан для титрования и разбавляют дистиллированной водой до 100 мл. Кислоту, щелочь или другой реагент известной концентрации прибавляют из бюретки по 1 мл, записывая при этом показания гальванометра. Во избежание изменения электропроводности вследствие разбавления раствора реагентом концентрация его должна быть выше концентрации титруемого раствора в 5-10 раз. Так как при титровании нет необходимости знать величину удельной электропроводности и постоянной сосуда, то достаточно определить общее сопротивление раствора между электродами либо пропорциональную ему силу тока в цепи гальванометра.
Опустив электроды в исследуемый раствор, с помощью реостата находят положение минимума, т. е. устанавливают стрелку гальванометра на минимальное отклонение. Дальнейшая настройка схемы зависит от природы титруемого раствора. Если, например, титруют сильную кислоту или щелочь, то величина электропроводности сначала уменьшается вплоть до эквивалентной точки, а затем вновь возрастает. Поэтому необходимо установить стрелку гальванометра у конца шкалы (на 80 – 90 делений).
При титровании слабых кислот или оснований, когда величина электропроводности непрерывно увеличивается, стрелку устанавливают у начала шкалы (на 25 – 30 делений).
Положение движка и величина сопротивления R, установленные в начале титрования, остаются без изменения до конца. Титрование начинают после выравнивания температуры в сосуде. Точность титрования в этих условиях не превышает 0,5 – 1,0%.