В зависимости от природы нуклеофильного атома, несущего избыток электронной плотности, различают: Н-, С-, N-, О- нуклеофилы в реакциях присоединения–отщепления.
1) Реакции восстановления H -нуклеофилами:
а) LiAlH4 восстанавливает монокарбоновые к-ты (через карбоксилат-анионы, т.к. в карбоксиле имеется «активный H», например Li Å [AlH4] Ө + R–СOОН ® R–СOОAl Ө H3Li Å(комплексная соль) + Н2).
В жестких условиях в избытке LiAlH4 восстановление идет до первичных спиртов с выделением Н2 путем последовательных переходов гидрид-ионов Н :Ө к атому С карбоксилата.
 4 R–СOОН + 3LiAlH4 ® 4 Н2 + 2 LiAlО2 +[(RСН2О)4Al ]Ө Li Å Н3ОÅ 4 RСН2ОН + AlСl3 + LiСl
4 R–СOОН + 3LiAlH4 ® 4 Н2 + 2 LiAlО2 +[(RСН2О)4Al ]Ө Li Å Н3ОÅ 4 RСН2ОН + AlСl3 + LiСl
б) Производные монокарбоновых к-т R–СOZ восстанавливаются до спиртов без выделения Н2


 Оd- 1) LiAlH4 здесь Z = {Hal, ОR, ОСОR - чаще карбэтоксилная группа},
Оd- 1) LiAlH4 здесь Z = {Hal, ОR, ОСОR - чаще карбэтоксилная группа},
 R1-Сd+-Z 2) Н3О Å NаВH4 можно использовать вместо LiAlH4 только для Z = Hal
R1-Сd+-Z 2) Н3О Å NаВH4 можно использовать вместо LiAlH4 только для Z = Hal
в) Амиды восстанавливаются без выделения Н2 до первичных, вторичных или третичных аминов


 Оd- 1) LiAlH4 здесь Z = {NН2; NНR; N(R)2}, выход 60-90%,
Оd- 1) LiAlH4 здесь Z = {NН2; NНR; N(R)2}, выход 60-90%,
 R1-Сd+- Z 2) Н3О Å NаВH4 не используют.
R1-Сd+- Z 2) Н3О Å NаВH4 не используют.
2) С -нуклеофилы:
В качестве С -нуклеофилов в органическом синтезе чрезвычайно часто используются металлорганические соединения карбанионной природы со связью CӨ - Me Å. Типичным примером реакции по карбонильному атому углерода является взаимодействие в эфире или ТГФ производных карбоксильной группы с реактивом Гриньяра - R Ө (MgХ) Å (алкилмагнийгалогенид).

 Оd- О - MgХ - MgХZ О + 1) R2MgХ ОН
Оd- О - MgХ - MgХZ О + 1) R2MgХ ОН
 R1-Сd+-Z + R Ө (MgHal) Å ® R1-С-Z R1-С-R + 2) Н2О R1-С-R2 + Mg(ОН)Х
R1-Сd+-Z + R Ө (MgHal) Å ® R1-С-Z R1-С-R + 2) Н2О R1-С-R2 + Mg(ОН)Х
С -нуклеофил R (где Z = Hal, ОR, ОСОR, N(R)2) R третичный спирт
3) О -нуклеофилы: А) В органической химии одними из наиболее изученных механизмов реакцией является синтез сложных эфиров (этерификация[5]), а также реакций гидролиза и переэтерификации в присутствии кислого катализатора. Эти реакции обратимы, поэтому их механизмы легко представить как постадийный процесс в каждом из обоих направлениях (см. “алканолы” ацилирование спиртов).
4) N -нуклеофилы
Для карбоксильной группы характерна поляризация С=О связи в силу большой электроотрицательности кислорода. В результате на карбонильном атоме углерода возникает d+, а на атоме кислорода d- заряды (>С d+ =О d-). Данные реакции могут протекать в отсутствии или присутствии кислотных катализаторов. Большинство из них протекает как нуклеофильное присоединение - AdN
 Реакции конденсации с участием соединений, содержащих аминогруппу общей формулы - NН2 -А, где А = Н, R, ОН, NН2, NН-С6Н5, NН-С(О)-NН2 и др. (аммиак, амины, гидроксиламин, гидразин, фенилгидразин, семикабозид и др.) по схеме напоминает образование сложных эфиров,
Реакции конденсации с участием соединений, содержащих аминогруппу общей формулы - NН2 -А, где А = Н, R, ОН, NН2, NН-С6Н5, NН-С(О)-NН2 и др. (аммиак, амины, гидроксиламин, гидразин, фенилгидразин, семикабозид и др.) по схеме напоминает образование сложных эфиров,
 Формализованная схема р-ций образования амидной группы:
Формализованная схема р-ций образования амидной группы:

 R-С-ОН + :NН2 -А ® R-С-NН-А + Н2О
R-С-ОН + :NН2 -А ® R-С-NН-А + Н2О
О О
VI. Синтез ангидридов кислот, сложных эфиров и кетенов
а) при нагревании кислот с водоотнимающими веществами
2 RСООН (tº) ® R- СО-О-СО -R + Н2О
б) из ацилгалогенидов и карбоновых к-т в присутствии пиридина (С5Н5N)
R1СОО Н + Cl -СО-R ® R1- СО-О-СО -R + НСl
в) из кетенов и карбоновых к-т
СН2=С=О (кетен) + R1СООН ® СН3- СО-О-СО -R1
г) реакция ацилгалогенидов со спиртами
СН3-СО- Cl + (СН3)3С-О Н ® СН3- СО-ОС (СН3)3 ( трет-бутилацетат - 68%) + НCl
д) реакция ангидридов кислот со спиртами
R1-СО-О-СО-R + R2-ОН ® R1- СО-О -R2 + R-СООН
ж) реакция переэтерификации (катализируется к-тами и основаниями)
R1-СО-О-R + R2-ОН ↔ R1- СО-О -R2 + R-ОН
VII. Жиры и входящие в их состав кислоты
К липидам относятся жиры и жироподобные вещества растительного и животного происхождения. Природные жиры и растительные жиры состоят главным образом из глицеридов (к-ты С10 - С18). Кислоты, содержащиеся в жирах, можно разделить на две категории: главные и второстепенные. Главные – к-ты, содержание которых в жирах более 10%.
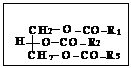 Глицерид, где R1, R2, R3 - радикалы кислот. Большинство жиров содержит две или три главных кислоты и некоторые другие кислоты в меньшем количестве, например, в масле какао содержатся в качестве основных кислот пальмитиновая СН3(СН2)14СООН, стеариновая СН3(СН2)16СООН и непредельные олеиновая СН3(СН2)7СН=СН(СН2)7СООН и СН3(СН2)4СН=СНСН2СН=СН(СН2)7–СООН линолевая к-ты.
Глицерид, где R1, R2, R3 - радикалы кислот. Большинство жиров содержит две или три главных кислоты и некоторые другие кислоты в меньшем количестве, например, в масле какао содержатся в качестве основных кислот пальмитиновая СН3(СН2)14СООН, стеариновая СН3(СН2)16СООН и непредельные олеиновая СН3(СН2)7СН=СН(СН2)7СООН и СН3(СН2)4СН=СНСН2СН=СН(СН2)7–СООН линолевая к-ты.
В зависимости от содержания соответствующих остатков к-т жиры различаются по физическим свойствам. По температурам плавления различают твердые жиры (к-ты – стеариновая, пальмитиновая) и густые жидкие (к-ты – олеиновая, линолевая, линоленовая). Для жиров используется понятие «температура затвердевания » (интервал температур). Жиры растворяются в эфире, сероуглероде, бензоле, толуоле и в бензине. В воде нерастворимы, но дают эмульсии.