Регуляция фосфорно-кальциевого обмена
План:
1. Введение
2. Роль фосфорно-кальциевого обмена в детстве
3. Три узловых момента фосфорно-кальциевого обмена
4. Основные регуляторы ФКО
5. Роль паратгормона и кальцитонина
6. Роль кальцитриола
7. Другие гормоны влияющие на обмен кальция
8. Нарушения фосфорно-кальциевого обмена
9. Литература
Фосфорно-кальциевый обмен
В раннем детском возрасте (особенно на первом году жизни) заболевания (или состояния), связанные с нарушением фосфорно-кальциевого обмена, занимают ведущее место.
Такое интенсивное увеличение размеров тела очень часто сопровождается абсолютным или относительным дефицитом кальция и фосфора в организме.
К развитию кальций- и фосфопенических состояний приводят разнообразные факторы: дефицит витаминов (главным образом витамина D), нарушения метаболизма витамина D в связи с незрелостью ряда ферментных систем, снижение абсорбции фосфора и кальция в кишечнике, а также реабсорбции их в почках, нарушения эндокринной системы, регулирующей фосфорно-кальциевый обмен, отклонения в микроэлементном статусе и многое другое.
Существенно реже встречаются гиперкальциемические состояния. Они носят, как правило, ятрогенный характер, но представляют не меньшую угрозу организму, чем гипокальциемии.
Три узловых момента определяют фосфорно-кальциевый метаболизм в организме:
1. всасывание фосфора и кальция в кишечнике;
2. взаимообмен их между кровью и костной тканью;
3. выделение Ca и P из организма – реабсорбция в почечных канальцах.
Основным показателем, характеризующим метаболизм Ca, является его уровень в крови, который в норме составляет 2,3–2,8 ммоль/л (содержание P в крови – 1,3–2,3 ммоль/л).
|
|
Все факторы, ухудшающие всасывание кальция в кишечнике и снижающие реабсорбцию его в почках, вызывают гипокальциемию, которая может частично компенсироваться вымыванием Ca из костей в кровь, что приводит к развитию остеомаляции или остеопорозов.
Избыточное всасывание Ca в кишечнике приводит к гиперкальциемии, которая компенсируется за счет усиленного отложения его в кости (зоны роста) и выведения с мочой.
Неспособность организма удержать нормальный уровень Ca крови вызывает либо тяжелые гипокальциемические состояния с проявлениями тетании, либо приводит к гиперкальциемии с картиной токсикоза, отложением Ca в различных тканях и органах.
Суточная потребность в кальции детей грудного возраста равна 50 мг на 1 кг массы, т.е. ребенок во втором полугодии жизни должен получать около 500 мг.
Важнейшим источником его являются молочные продукты: в 100 мл женского молока содержится 30 мг Ca, в таком же количестве коровьего – 120 мг.
Важное значение имеет состояние слизистой оболочки тонкой кишки: синдромы мальабсорбции, энтериты сопровождаются ухудшением всасывания. Главным регулятором всасывания Ca является витамин D.
Основная масса (более 90%) кальция и 70% фосфора находится в костях в виде неорганических солей. В течение всей жизни костная ткань находится в постоянном процессе созидания и разрушения, обусловленном взаимодействием трех типов клеток: остеобластов, остеоцитов и остеокластов. Кости активно участвуют в регуляции метаболизма Ca и P, поддерживая их стабильный уровень в крови. При снижении уровня кальция и фосфора крови (произведение Ca x P является постоянной величиной и равно 4,5-5,0) развивается резорбция кости за счет активации действия остеокластов, что увеличивает поступление в кровь этих ионов; при повышении данного коэффициента происходит избыточное отложение солей в кости.
|
|
Половина содержащегося в крови Ca связана с белками плазмы (главным образом с альбумином), из оставшейся части более 80% это ионизированный кальций, способный проходить через стенку капилляра в интерстициальную жидкость. Именно он является регулятором разнообразных внутриклеточных процессов, в том числе проведение специфического трансмембранного сигнала в клетку, поддержание определенного уровня нервно-мышечной возбудимости. Связанный с белками плазмы Ca является резервом для сохранения необходимого уровня ионизированного кальция.
Регуляция
Основными регуляторами фосфорно-кальциевого обмена наряду с витамином D являются паратиреоидный гормон (ПГ) и кальцитонин (КТ) – гормон щитовидной железы.
Парагормон и кальцитонин
Гормоны секретируются клетками паращитовидной железы. Местом синтеза кальцитонина является также щитовидная железа.
Парагормон был получен в частично очищенном состоянии в 1925 году из паращитовидной железы быка. Он представляет собой простую полипептидную цепь состоящую из 84 аминокислотных остатков с молекулярной массой 9500 Да; период полураспада около 2 мин. Ген кодирующий биосинтез парагормона локализуется на 11-й хромосоме (11р15).
Парагормон образуется на рибосомах в виде препропарагормона – полипептида состоящего из 115 аминокислотных остатков. В результате локального протеолиза отщепляется 31 аминокислотный остаток с N-конца и образуется активный гормон который запасается в секреторных гранулах.
|
|
Регуляция секреции парагормона осуществляется несколькими механизмами. В течение короткого времени биосинтез парагормона регулируется ионизированным кальцием а в течение длительного времени – 1 25(ОН)2D3 - совместно с кальцием. Скорость секреции обратно пропорциональна концентрации в плазме крови.
Метаболизм и деградация парагормона осуществляется в основном в печени (около 62-70%) а также в почках (30-38%).
Парагормон оказывает многообразное действие в зависимости от ткани-мишени. Все это позволило L. Mallette (1991) высказать мнение что парагормон является прогормоном а его фрагменты обладают биологическим действием. Считается что его аминотерминальный домен (аминокислотные остатки 1-34) ответствен за регуляцию минерального обмена посредством взаимодействия с соответствующими рецепторами в костях и почках; карбокситерминальный домен (аминокислотные остатки 53-84) – за регуляцию функции остеокластов а средний домен (аминокислотные остатки 28-48) возможно за транспорт кальция и фосфора
Парагормон взаимодействует с плазматическими рецепторами которые являются гликопротеинами с молекулярной массой около 800 кДа и состоят из 585-594 аминокислотных остатков. Рецептор парагормона как и все другие рецепторы относящиеся к семейству рецепторов оперирующих через G-белок имеет 3 цепи внеклеточного фрагмента 7 трансмембранных фрагментов и внутриклеточную часть рецептора также представленную 3 петлями полипептидной цепочки.
Такое взаимодействие приводит к активации аденилатциклазы и повышению синтеза цАМФ который активирует протеинкиназу фосфолипазу С диацилглицерин инозитолтрифосфат и участвует в регуляции транспорта ионов кальция натрия и калия через клеточные мембраны.
Парагормон оказывает множественное действие на костную ткань. Он опосредованно активирует ферменты коллагенозу и глюкуронидазу что вызывает деструкцию органических компонентов кости в частности коллагена и гликозамингликанов. В минеральных компонентах костной ткани под действием парагормона происходит солюбилизация гидроксиапатита и высвобождение в кровь кальция и фосфора.
Было установлено что парагормон активирует процессы транскрипции в остеокластах – клетках резорбирующих кости. Влияние парагормона на резорбцию костной ткани на пострецепторном уровне осуществляется в основном через инозитолтрифосфат и диацилглицерин но не через цАМФ которые образуются посредством активации фосфолипазы С и ионов Са.

Кальций всасывается в верхнем отделе тонкого кишечника. Это активный процесс осуществляемый транспортным кальцийсвязывающим белком который активизируется 1 25-дигидроксивитамином D. Всасывание кальция в кишечнике усиливается при увеличении поступления кислот с пищей диете с высоким содержанием белка саркоидозе беременности тогда как щелочи глюкокортикоиды избыток фосфатов и оксалатов снижают его всасывание в кишечнике.
Свое влияние парагормон на натрий-фосфатный котранспорт оказывает путем повышения образования цАМФ и путем активизации фосфолипазы С и образования диацилглицерина и инозитолтрифосфата.
Кальцитонин был впервые получен С. Н. Коопом и соавторами в 1962 году. Кальцитонин человека представляет собой полипептид состоящий из 32 аминокислот с мол. м. 3000 Да с периодом полураспада около 5 мин. Гормон может образовывать путем ковалентной связи димерные и не исключено полимерные формы однако биологически активной является только мономерная форма гормона. Было показано что в процессе трансляции образуется препрокальцитонин и прокальцитонин с мол. м. около 13 кДа.
Специфическим стимулятором секреции кальцитонина является повышение концентрации кальция в крови более 2 25 ммоль/л (9 мг/100 мл). Кроме того стимуляторами секреции кальцитонина являются катехоламины осуществляющие свое действие через β-адренергические рецепторы холецистокинин глюкагон гастрин. Глюкагон и катехоламины взаимодействуя с рецепторами увеличивают содержание цАМФ который стимулирует секрецию кальцитонина так же как и парагормона т.е. цАМФ является внутриклеточным медиатором секреции кальцитонина. Кальцитонин метаболизируется в почках печени и возможно в костной ткани.
Биологический эффект кальцитонина проявляется снижением уровня кальция и фосфора в крови что является следствием влияния кальцитонина на костную ткань и почки. В кости кальцитонин угнетает процессы резорбции кальция. Это проявляется снижением экскреции гидроксипролина и содержания кальция в крови. Одновременное уменьшение фосфора в сыворотке крови является результатом снижения мобилизации фосфора из кости и непосредственной стимуляции поглощения фосфора костной тканью. Кальцитонин ингибирует активность и количество остеокластов. Уже через 1 ч после введения кальцитонина уменьшается образование остеокластов из клеток-предшественников. Механизм действия кальцитонина опосредуется цАМФ и активацией протеинкиназ что сопровождается изменением активности щелочной фосфатазы пирофосфатазной активности и активности ферментов.
Кальцитриол
Наряду с парагормоном и кальцитонином в поддержании фосфорно-кальциевого гомеостаза большое участие принимает витамин D (D-гормон холекальциферол или витамин D3) который при гидроксилировании в печени и почках образует гормон кальцитриол (1α 25-дигидроксихолекальциферол)
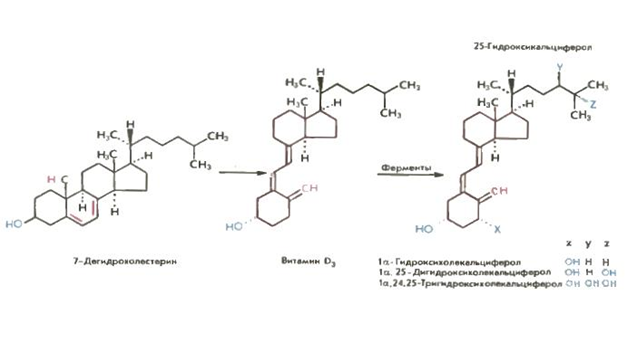
Витамин D3 образуется в коже из 7-дегидрохолестерина под влиянием ультрафиолетового облучения (рис.3). Однако витамин D3 является неактивным. Некоторые авторы рассматривают его как прогормон который путем гидроксилирования (25-гидроксилаза) сначала в печени превращается в 25-гидроксихолекальциферол (25-ОНD2) а затем в почках также путем гидроксилирования (1-гидроксилаза) в 1 25-дигидроксихолекальциферол (1 25-(ОН)2D3. Гидроксилирование в почках может осуществляться и другим путем (24-гидроксилаза) с образованием 24-25-(ОН)2D3. Гидроксилирование витамина D происходит в митохондриях. Необходимо отметить что витамин D2 (эргокальциферол) содержащийся в растениях в организме гидроксилируется тем же путем с образованием 1 25-(ОН)2D2 который по биологической активности эквивалентен 1 25-(ОН)2D3.