
|
Число Авогадро
pV = NRT
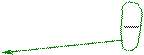 N A
N A
постоянная Больцмана
N
Число молекул газа Число молекул в 1 моль
разделим обе части на V:
p = kT V
pV = m RT
M
Масса газа
|
число молекул в 1 м3.
разделим обе части на V:
Масса 1 моль газа — молярная масса

2. Закон Дальтона
 p смеси= p 1 + p 2 + …
p смеси= p 1 + p 2 + …
p = mRT
VM
— плотность газа.

|
|
15,9994 О
Кислород
Парциальное давление первого из газов, входящих в смесь, — т. е. давление, которое создавал бы этот
Давление смеси
|
p =n 1 RT смеси
газ, если бы он один занимал весь объем смеси.
газов.
|
3.  Основное уравнение МКТ
Основное уравнение МКТ
 2
2
M
 m 0 =
m 0 =
NA
Масса 1 моль
Число молекул в 1 моль


|
k
= m 0 v кв
= 3 kT
 Плотность газа r
Плотность газа r
Масса одной молекулы
 Средняя кинетическая энергия поступательного движения молекул
Средняя кинетическая энергия поступательного движения молекул
|
|
0 10 2
|
v кв =
+ +K+
2 2 2
2 2 Средняя квадратичная скорость
E пост = 2 2 2 = m 0 ⎛ v 1
+ v 2 +K+ v N ⎞= m 0 v
= m 0 v кв,

 ⎜
⎜
 k N 2 ⎝ N
k N 2 ⎝ N
⎟
 ⎠ 2 2
⎠ 2 2
4.  Газовые законы Из
Газовые законы Из
pV = n RT следует, что если n = const, то
pV = const
 T
T




|


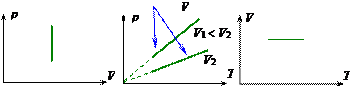
Изотермический процесс,
график - изотерма.
 V (T) = n R × T
V (T) = n R × T


|
процесс,
график - изобара

|
 И
И
процесс,
график - изохора.
|
|
5. Первый закон термодинамики
Количество теплоты, полученное (Q > 0)
или отданное (Q < 0) системой.
Q = D U + A газа
Работа газа
 |
V = const
(Энергия, полученная или отданная системой в процессе
теплопередачи, т. е. при обмене энергиями между молекулами — на микроскопическом уровне.)
Изменение внутренней энергии системы
А газа = 0
C = Q
Þ Q = C D T
U = E k тепл + E p взаим
p = const
D T
Теплоемкость тела (системы)
Внутренняя энергия
Кинетическая энергия
Потенциальная энергия
А газа
= p D V = n R D T
c = Q m D T
Þ Q = cm D T
хаотического
(теплового)
движения
взаимодействия молекул друг с
другом.
численно
n = const
молекул.
А газа = ± S под граф. р (V)
C = Q Þ Q = C nD T
В идеальном газе E k тепл >> E p взаим, поэтому
" + " — если газ расширяется
M nD T
M
U = E
= ii
"-" — если газ сжимается
Молярная теплоемкость вещества
k тепл
pV = n RT
2 2 р
C =D U
i = 3 для одноатомных газов (Не, Ne, Ar, …)
При V = const:
При p = const:
V D T
i = 5 для двухатомных газов (Н2, N2, О2, воздух,)
|
C = D U + A > C
D U =
i (p V
- p V) = i n R D T
p D T V
2 2 2
1 1 2
6. Адиабатический процесс
Для идеального газа
Q подв
Q = 0 Þ A газа = - D U
D U = CV D T
= cV m D T
= CM V nD T
В теплоизолированной системе или при быстрых процессах
Для идеального газа в любом процессе
р При адиабатическом расширении (А газа > 0) газ охлаждается (D U < 0)
При адиабатическом сжатии (А газа < 0) газ нагревается (D U > 0)
Адиабата — гипербола, идущая более "круто" чем изотермы (с ростом V убывает T).
|
|
Рабочее А
Вещество
(газ)
Изотермы
V
7. КПД циклического процесса
(теплового двигателя)
Q отв
hцикла =
A газа в цикле
= Q подв -
Q отв
= 1 -
Q отв
Холодильник
|
Q подв
Q подв
T хол
Q полн. за цикл = Q подв + Q отв = D U в цикле + Aгаза в цикле
Q отв <0 Þ Q отв = -⏐ Q отв⏐ D U в цикле = U кон - U нач = 0
|
|
"-" - если цикл идет "против часовой
h = T наг - T хол
|
наг
КПД идеальной тепловой машины, работающей по
численно
стрелки"
циклу Карно — максимальный
6. Насыщенный пар — газ, дальнейшее изотермическое сжатие или изохорное
теоретически возможный КПД
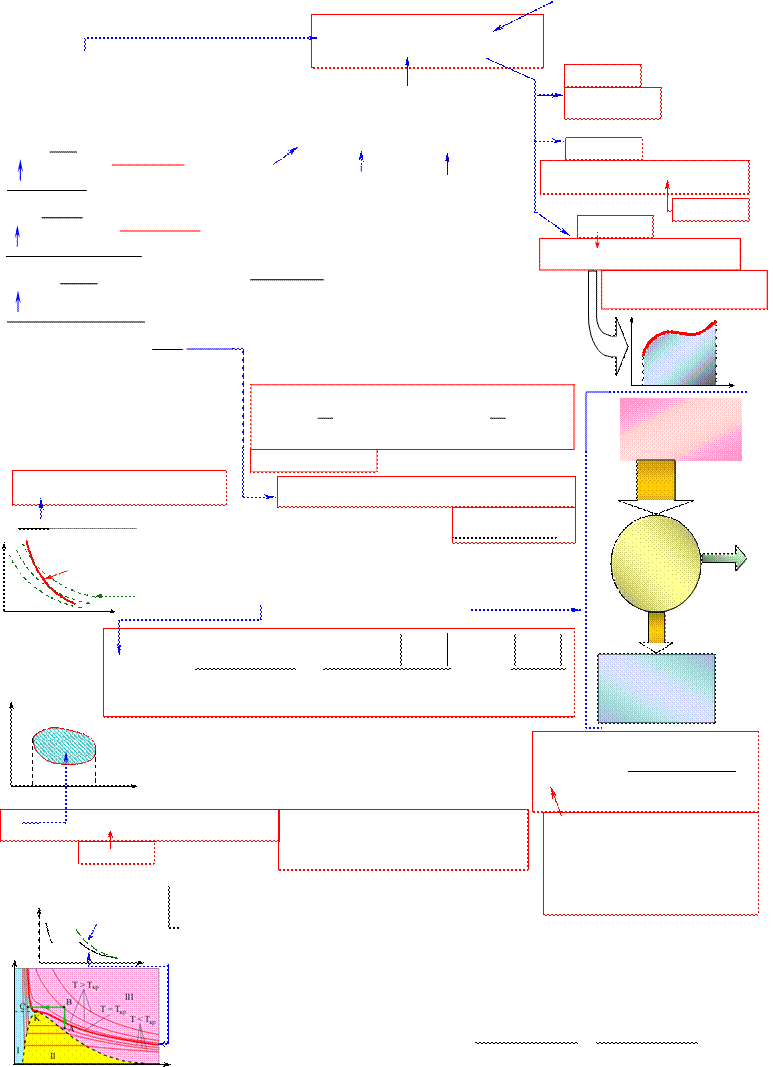
р Идеальная изотерма
охлаждение которого приводит к превращению части этого газа в жидкость (при наличии центров конденсации).
при данных Т нагр и Т хол.
р нас
р V
газ, находящийся в динамическом равновесии со своей жидкостью, т. е. в состоянии, когда число
молекул, переходящих из газа в жидкость равно числу молекул, переходящих обратно за то же время.
|
область II - вода в равновесии с насыщенным область III - газ паром
|
|
T кр - критическая температура, при Т > T кр газ никаким сжатием нельзя перевести в жидкость.
|
 V Для воды p нас (100 оС) » 105 Па
V Для воды p нас (100 оС) » 105 Па
VI.  Электростатика
Электростатика
k = 1
» 9 ×109
Н ×м2
1. Закон Кулона
Сила
F = k
q 1 × q 2


-12
электростатического эл
e r 2
e0 » 8,85×10
Ф/м — электрическая постоянная
взаимодействия
 точечных зарядов q 1 и q 2
точечных зарядов q 1 и q 2
Точечными считаются заряженные тела, размеры которых пренебрежимо малы по сравнению с расстоянием между ними.
r — расстояние между зарядами q 1 и q 2
e — диэлектрическая проницаемость среды, в которой находятся заряды q 1 и q 2
(полагается, что среда — безграничный, однородный диэлектрик)
|
|
|
2. Принцип суперпозиции
 Если на заряд q действуют несколько зарядов Q 1, Q 2, …, то:
Если на заряд q действуют несколько зарядов Q 1, Q 2, …, то:
q 1 F 21
r q 2
r
F на q
r
= F на q
(Q 1) +
r
F на q
(Q 2
) +K
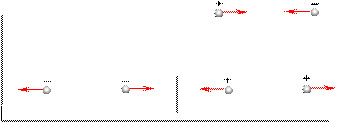
Заряды одинаковых знаков ("одноименные") отталкиваются друг от друга:
r r
Сила, действующая на заряд q со
Сила, которая действовала
бы на заряд q со стороны Q 1 r
r
F 21 q 1
q 2 F 12
r
F 21
q 1 q 2
F 12
стороны системы зарядов Q 1, Q 2, …
заряда Q 1, в отсутствие F 2
остальных зарядов Q 2, Q 3, … Q 2
q r
F 1
r r r
3. Электрическое поле
— особая материя,
F = F 1 + F 2
возникающая вокруг любых электрических зарядов и действующая электрической силой на любые электрические заряды, попавшие в это поле.