Решение. Ординаты и абсциссы точек изотермы толуола вычисляются по формулам (1) и (2):
 (1)
(1)
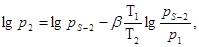 (2)
(2)
где a1 * и a2 * - концентрации адсорбированных бензола и толуола, кг/кг;
V1 и V2 – молярные объемы бензола и толуола в жидком состоянии, м3;
p1 и p2 – парциальное давление паров бензола и толуола, мм рт. ст;
pS-1 и pS-2 – давление насыщенных паров бензола и толуола при 20°С, мм рт. ст.;
T1 и Т2 - абсолютная температура бензола и толуола при адсорбции (в данном случае Т1 — Т2 = 293° К);
β - коэффициент аффинности.
Молярный объем бензола:
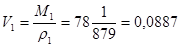 м3/кмоль.
м3/кмоль.
Молярный объем толуола:
 м3/кмоль.
м3/кмоль.
Коэффициент аффинности:
 .
.
На изотерме бензола берем ряд точек

Первая точка: a1 * = 0,25 кг/кг; p1 = 8 мм рт. ст. Вычислим координаты соответствующей точки на изотерме толуола:

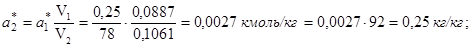
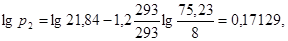
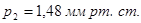
Вторая точка: a1 * = 0,30 кг/кг; p1 = 57 мм рт. ст. Вычислим координаты соответствующей точки на изотерме толуола:




Третья точка: a1 * = 0,15 кг/кг; p1 = 1 мм рт. ст. Вычислим координаты соответствующей точки на изотерме толуола:


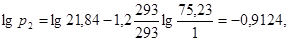

Четвертая точка: a1 * = 0,28 кг/кг; p1 = 20 мм рт. ст. Вычислим координаты соответствующей точки на изотерме толуола:

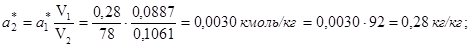
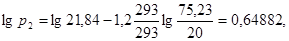
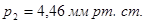
Пятая точка: a1 * = 0,20 кг/кг; p1 = 2,5 мм рт. ст. Вычислим координаты соответствующей точки на изотерме толуола:

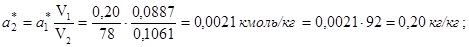
 откуда
откуда

Шестая точка: a1 * = 0,26 кг/кг; p1 = 10 мм рт. ст. Вычислим координаты соответствующей точки на изотерме толуола:

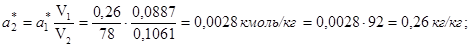
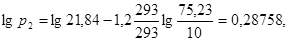 откуда
откуда
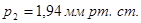
Седьмая точка: a1 * = 0,22 кг/кг; p1 = 3,5 мм рт. ст. Вычислим координаты соответствующей точки на изотерме толуола:


 откуда
откуда
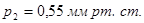
Вычислив ординаты и абсциссы всех точек, полученные данные, сводим в табл. 1.
Таблица 1
| Изотерма бензола | Изотерма толуола | ||
| a1 *, кг/кг | p1, мм рт. ст | a2 *, кг/кг | p2, мм рт. ст |
| 0,15 0,20 0,22 0,25 0,26 0,28 0,30 | 2,5 3,5 | 0,15 0,20 0,22 0,25 0,26 0,28 0,30 | 0,12 0,37 0,55 1,48 1,94 4,46 15,65 |
По найденным точкам строим изотерму толуола для 20 ºС.
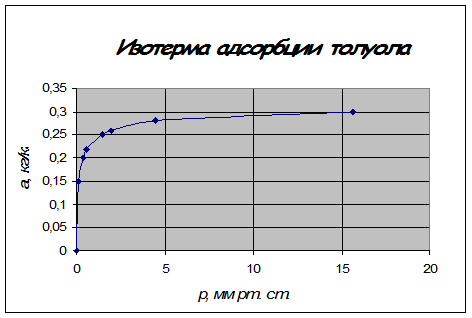
Определим с помощью изотермы статическую активность угля по толуолу при концентрации паро-воздушной смеси 
Предварительно необходимо рассчитать парциальное давление, соответствующее 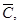 по формуле (3):
по формуле (3):
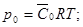 (3)
(3)

По диаграмме абсциссе p0 = 1,4 мм рт. ст. соответствует ордината a0 * = 0,248 кг/кг.
Количество активного угля на одну загрузку составляет:
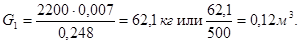
Диаметр адсорбера вычисляется из равенства:

откуда
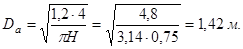
Так как на изотерме точка, соответствующая исходной концентрации паро-воздушной смеси  находится в первой (прямолинейной) области, то продолжительность процесса вычисляется по формуле (4):
находится в первой (прямолинейной) области, то продолжительность процесса вычисляется по формуле (4):
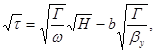 (4)
(4)
где 
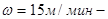 скорость газового потока;
скорость газового потока;
H = 0,75 – высота слоя угля;
b – функция, определяемая по табл. 8-3 (стр. 448, [1]) для

значение b = 1,84;
βу – коэффициент массопередачи, который вычисляется по формуле (5):
 (5)
(5)
Находим кинематический коэффициент вязкости воздуха. Так как по рис. VI (стр. 607, [1]) μ = 0,018 · 10-3 н · сек/м2, то
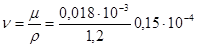 м2/сек.
м2/сек.
Тогда:
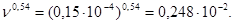
Диаметр частицы угля dз = 0,004 м, и значит
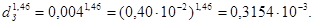
Скорость  следовательно:
следовательно:

Коэффициент диффузии при 0 ºС для системы толуол – воздух:
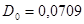 м2/ч = 0,197 · 10-4 м/сек.
м2/ч = 0,197 · 10-4 м/сек.
Для температуры 20 ºС коэффициент диффузии вычисляется по формуле:
 м2/сек.
м2/сек.
После подстановки получим объемный коэффициент массопередачи:
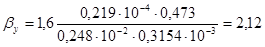 сек -1.
сек -1.
Определяем продолжительность процесса:
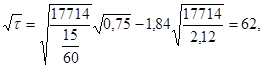
τ = 622 = 3844 сек = 64 мин = 1,07 ч.
Определим количество паро-воздушной смеси, проходящей через адсорбер за 64 мин:
 м3.
м3.
По данным на проектирование, за один период через адсорбер должно пройти 2200 м3. Следовательно, диаметр адсорбера следует увеличить:
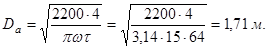
Необходимо также увеличить количество активированного угля на одну загрузку:
 кг.
кг.
Список используемой литературы
1. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии: Учеб. пособие. 6-е изд., доп. и перераб. Л.: Химия, 1964. 634 с.
2. Основные процессы и аппараты химической технологии. Пособие по проектированию/Под ред. Ю.И. Дытнерского 2-ое изд. доп. и перераб.- М/Химия. 1991 г.
3. Касаткин А.Г. Основные процессы и аппараты химической технологии: Учебник, 9-е изд. доп. и перераб. – М.:Химия, 1978. 783 с.
4. Кузнецов А.А. Расчеты основных процессов и аппаратов переработки углеводородных газов. – М.:Химия, 1983. – 233 с.
5. Варгафтик Н.Б. Справочник по теплофизическим свойствам газов и жидкостей. – М.: Государственное изд-во физико-математической литературы «Физматгиз». 1963. 708 с. с ил.