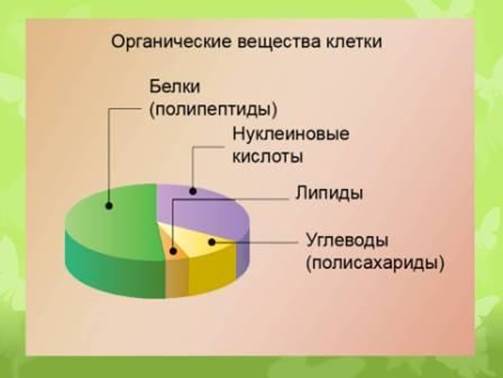
Химические соединения, основой строения которых являются атомы углерода, составляют отличительный признак живого. Эти соединения называются органическими. Органические соединения чрезвычайно разнообразны, но только четыре класса имеют всеобщее биологическое значение: белки, нуклеиновые кислоты, углеводы, липиды.
Белки. Это биополимеры, мономерами которых являются аминокислоты.
Аминокислоты представляют собой низкомолекулярные органические соединения, содержащие карбоксильную (-СООН) и аминную (-NН3) группы, которые связаны с одним и тем же атомом углерода. К атому углерода присоединяется боковая цепь – какой-либо радикал.
У большей части аминокислот имеется одна карбоксильная группа и одна аминогруппа, эти аминокислоты называют нейтральными. Существуют и основные аминокислоты – с более чем одной аминогруппой, а также кислые минокислоты – с более чем одной карбоксильной группой.
Известно около 200 аминокислот, встречающихся в живых организмах, однако только 20 из них входят в состав белков.
В зависимости от радикала основные аминокислоты делят на 3 группы:
1.Неполярные (аланин, метионин, пролин, лейцин, изолейцин, триптофан, фенилаланин);
2.Полярные незаряженные (аспарагин, глутамин, серин, глицин, тирозин, треонин, цистеин);
3.Заряженные (аргинин, гистидин, лизин – положительно; аспарагиновая и глутаминовая кислоты - отрицательно).
Белки представляют собой полипептиды, в молекулу которых входит от 50 до нескольких тысяч аминокислот с молекулярной массой свыше 10000.
Каждому белку свойственна в определенной среде своя особая пространственная структура. При характеристике пространственной структуры выделяют четыре уровня организации молекул белков.
Первичная структура – последовательность аминокислот в полипептидной цепи. Первичная структура специфична для каждого белка и определяется генетической информацией, т.е. зависит от последовательности нуклеотидов в участке молекулы ДНК, кодирующем данный белок. От первичной структуры зависят свойства и функции белков. Замена одной единственной аминокислоты в составе молекул белка или изменение их расположения влечет за собой изменение функций белка.
В живых клетках молекулы белков или отдельные их участки представляют собой не вытянутую цепь, а скручены в спираль, напоминающую вытянутую пружину – α-спираль или сложены в складчатый слой – β-структура. Вторичная структура возникает в результате образования водородных связей между -СО- и -NН2-группами двух пептидных связей в одной полипептидной цепи (спиральная структура) или между двумя полипептидными цепями (складчатый слой).
У большинства белков спиральные и неспиральные участки полипептидной цепи складываются в трехмерное образование шаровидной формы – глобулу – третичная структура. Третичная структура стабилизируется ионными, водородными связями, ковалентными дисульфидными связями, которые образуются между атомами серы, а также гидрофобными взаимодействиями.
Многие белки, обладающие третичной структурой, могут выполнять свою биологическую роль в клетке. Однако для осуществления некоторых функций организма требуется участие белков с еще более высоким уровнем организации.
Такую организацию называют четвертичной структурой. Она представляет собой функциональное объединение нескольких молекул белка, обладающих третичной структурной организацией.
Функции белков:
1. Ферментативная. Практически все ферменты являются белками.
2. Структурная (коллаген соединительных тканей (у млекопитающих составляет около 25% от общей массы белков), эластин, кератин).
3. Гормональная (инсулин, вазопрессин).
4. Транспортная (например, гемоглобин переносит О2, СО, СО2).
5. Защитная (антитела, фибрин).
6. Сократительная (актин-миозиновый комплекс).
7. Опорная (тубулин микротрубочек).
8. Двигательная. Сократимые и опорные комплексы обеспечивают все виды движения.
9. Гомеостатическая. Практически все белки обладают буферными свойствами, поддерживая постоянную величину рН.
10. Запасающая (овальбумин – запасной альбумин яичного белка).
11. Энергетическая. При гидролизе белков образуется аминокислоты, часть которых окисляется с высвобождением энергии.
Липиды. Это сборная группа органических веществ, которые плохо растворимы в воде, но хорошо растворимы в органических (неполярных) растворителях. В молекулах липидов имеются неполярные (углеводородные) и полярные (–СООН, –ОН, –NH2) участки. Неполярные участки не смачиваются водой и называются гидрофобными. Полярные участки смачиваются водой и называются гидрофильными.
К липидам относятся триглицериды, фосфолипиды, стероиды, терпены, воски и некоторые другие вещества.
Липиды могут образовывать соединения с углеводами (гликолипиды) и белками (липопротеиды, или липопротеины).
Функции липидов:
Структурные. Фосфолипиды – основа клеточных мембран.
Энергетическая. 1 г = 38,9 кДж.
Запасающие. Твердые и жидкие жиры (триглицериды).
Регуляторные. Многие гормоны.
Защитная и теплоизоляционная. Жир.
Смазывающая и водоотталкивающая. Воска.
Метаболическая.
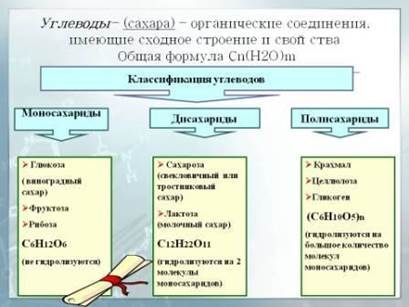
Углеводы, или сахара – это органические вещества, состав которых может быть описан формулой Cn(H2O)m. К углеводам относятся моносахариды, олигосахариды и полисахариды.
Моносахариды – это простейшие углеводы. В их состав входят углерод, водород и кислород в соотношении 1:2:1. Молекула моносахарида состоит из углеродного скелета, в боковых цепях которого содержатся водород и функциональные группы (гидроксильные –ОН, альдегидные –СНО, кетогруппы =С=О).
Функции моносахаридов:
1. Играют роль промежуточных продуктов реакций.
2. Входят в состав нуклеотидов и их производных
3. Входят в состав некоторых коферментов
4. Служат основными источниками энергии при дыхании.
5. Служат исходными веществами для синтеза аминокислот, сложных углеводов и других веществ (например, аскорбиновой кислоты).
Полисахариды – это углеводы, состоящие из остатков множества моносахаридов (тысячи и десятки тысяч), связанных гликозидными связями. Гигантские молекулы (макромолекулы), в состав которых входят сходные, многократно повторяющиеся структуры, называются полимеры, а сами повторяющиеся структуры называются мономеры. Полимеры могут быть линейными и разветвленными. К полисахаридам относятся многие полимеры глюкозы: крахмал, гликоген, целлюлоза (клетчатка).
Функции полисахаридов:
1. Запасающие (гликоген у грибов и животных, крахмал у растений).
2.Структурные, или опорно-защитные (целлюлоза, муреин, мукополисахариды).
ВОПРОСЫДЛЯ СОМОПРОВЕРКИ
1.Какие химические соединения называются углеводами?
2.Какие клетки наиболее богаты углеводами?
3.Что такое моносахариды? Приведите приме-
4.Что такое дисахариды? Приведите примеры.
5.Какой простой углевод служит мономером крахмала» гликогена, целлюлозы?
6.Укажите функции углеводов.
7.Что такое жиры?
8. Опишите их химический состав.
9. Какие функции выполняют жиры?
ЛИТЕРАТУРА
1. Беляев Д. К., Дымшиц Г. М., Кузнецова Л. Н. и др./ Под ред. Беляева Д. К., Дымшица Г. М. Биология, 10 класс, Базовый уровень, 2017 г.(с.9-25)