Задачи по молекулярной физике для студентов факультета
1) (Коз. 2.8) Температура комнаты была t 1 =10оС. После того, как печь натопили. температура в комнате поднялась до t 2 =20оС. Объем комнатs V = 50м3, давление в ней Р =97 кПа. На сколько изменилась масса воздуха, находящегося в комнате? Молярная масса воздуха μ=29 г/моль.
2) (Коз. 2.9) Перед вылетом пули из ствола ружья объем, занимаемый пороховыми газами, в n =100 раз превышает объем твердого пороха. Температура газов в этот момент Т =1000 К. Молярная масса пороховых газов μ=30 г/моль, плотность твердого пороха ρо=1 г/см3.Определить давление пороховых газов при вылете пули.
3) (Коз.2.10) Баллон с гелием при давлении Р 1=6,5·106 Па и температуре t 1 = −3оС имеет массу М 1=21 кг, а при давлении Р 2=2·106 Па и той же температуре массу М 2=20 кг. какую массу гелия содержит баллон при давлении Р =1,5·107 Па и температуре t =27оС?
4) (Коз.2.18) При нагревании газа при постоянном объеме на 1 К давление увеличилось на 0,2%. При какой начальной температуре находился газ?
5) (Коз. 2.24) До какой температуры нужно нагреть запаянный шар, содержащей m =17,5 г воды, чтобы он разорвался? Стенки шара выдерживают давление не более Р=107 Па, объем шара V = 1000 см3.
6) (Коз. 2.26) Стеклянный баллон при постоянной температуре был взвешен трижды: а) откачанный, б) заполненный воздухом при атмосферном давлении Ри=105 па, в) заполненный неизвестным газом при давлении Рг=1,5·105 Па. Оказалось, что m1=200 г, m2=204 г, m3= 210 г. Определить молярную массу μг неизвестного газа. Молярная масса воздуха μ=-29 г/моль.
7) (Коз. 2.30) Найти формулу некоторого соединения углерода с водородом, если известно, что m=0,65 г этого вещества в газообразном состоянии создает в объеме V = 1000 см3 при температуре t =27оС давление Р=105 Па.
8) (Ир. 2.7) В вертикальном закрытом с обоих торцов цилиндре находится массивный поршень, по обе стороны которого − по одному молю воздуха. При Т=300 К отношение верхнего объема к нижнему η=4,0. При какой температуре это отношение станет η1=3,0? Трением пренебречь.
9) (Коз. 2.37) В вертикально расположенном цилиндре сечения S под поршнем массы m находится воздух при температуре Т 1. Когда на поршень положили груз массы М, расстояние от дна цилиндра до поршня уменьшилось в n раз. Насколько повысилась температура воздуха в цилиндре? Атмосферное давление равно Р о.
| 10) (Коз. 2.36) В цилиндре под поршнем с площадью S =100 см2 находится m=28 г азота при температуре t 1 =100оС. К поршню через систему блоков подвешен груз массы М =50 кг. Цилиндр охлаждают до t 2 =0оС. На какую высоту h поднимется груз? Атмосферное давление Р о=105 па. Массой поршня пренебречь. | 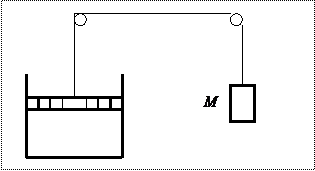
|
11) (Коз.2.42) Сосуды с объемами V 1 =200 см3 и V 2 = 100 см3 соединены короткой трубкой, в которой имеется пористая теплоизолирующая перегородка. С ее помощью в сосудах устанавливается одинаковое давление. Первоначально система находилась при температуре t o =27оС и содержала газ при давлении Р о=105 Па. Затем малый сосуд поместили в тающий лед при температуре t 2= 0оС, а большой − в пар при температуре t 1= 100оС. Какое давление установится в системе? Тепловым расширением сосудов пренебречь.
12) (Коз. 2.55) В закрытом с обоих концов откачанном вертикальном цилиндре подвешен на пружине скользящий без трения поршень, положение равновесия которого находится у дна цилиндра. Под поршень вводят такое количество газа при температуре Т, что поршень поднимается на высоту h. На какой высоте h 1 установится поршень, если этот газ нагреть до температуры Т 1? Сила, действующая на поршень со стороны пружины, пропорциональна смещению поршня.
13) (Пин. 16.18) Газ вращается в центрифугу. Учитывая, что поле центробежных сил инерции эквивалентно полю силы тяжести, написать выражение для распределения концентрации молекул (или давления) газа в радиальном направлении.
14) (Пин. 16.22, Ир. 2.20) Вывести барометрическую формулу для атмосферы, температура которой линейно убывает с высотой. Молярная масса газа М, Р (z=0) = P o, T (z)= T o(1-αz), α>0.
Также попробуйте учесть зависимость ускорения свободного падения от высоты для малых по сравнению с Земным радиусом высот: g(z)=go(1−z/RЗ).
15) (Ир. 2.19) Идеальный газ с молярной массой М находится в очень высоком вертикальном сосуде в однородном поле тяжести, для которого ускорение свободного падения равно g. Считая температуру газа везде одинаковой и равной Т, найти высоту расположения центра тяжести газа.
16) (Ир. 2.18) Идеальный газ с молярной массой М находится в высоком цилиндрическом сосуде, площадь основания которого есть S, а высота h. Температура газа Т, его давление на нижнее основание Р о. Считая, что ускорение свободного падения g и температура газа не зависят от высоты, найти массу газа в сосуде.
17) (Ир. 2.12) Найти максимально возможную температуру идеального газа в следующих процессах: а) 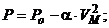 б)
б) 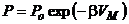 ,
,
где Р о, α и β – положительные постоянные, V M - объем моля газа.
18) На диаграмме РТ представлена зависимость давления от температуры при изохорном нагревании различных масс одного и того же газа в одинаковых по объему сосудах. Что можно сказать о массах этого газа?
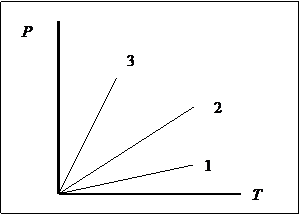
| 1. m1 > m2 > m3 2. m1 < m2 < m3 3. m1 = m2 = m3 4. при различных значениях объема соотношение масс может быть разное 5. для разных газов может быть разная зависимость |
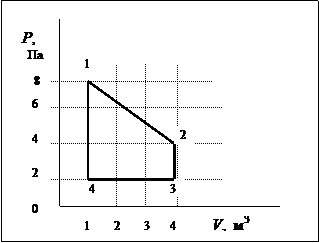
19) Какую работу совершит идеальный газ за один цикл, изображенный на графике?
| 1) 8 Дж 2) 12 Дж 3) 16 Дж 4) 20 Дж 5) 24 Дж |
| 20) (Пин. 17.6) При расширении газа его давление росло линейно, см. рисунок. Какую работу совершил газ? Какое количество теплоты к нему было подведено? Газ одноатомный. | 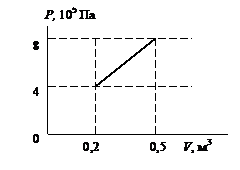
|
21) Идеальная тепловая машина работает по циклу, изображенному на рисунке. Ее КПД равен:
 |
|
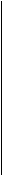

 1) 25%
1) 25%
2) 33,3%
|
3) 75%
 |
4) 50%
 |
|
 определения КПД
определения КПД
|
22) (Ир. 2.122) У тепловой машины, работающей по циклу Карно, температура нагревателя в 1,6 раза больше температуры холодильника. За один цикл машина производит работу А = 12 кДж. Какая работа за цикл затрачивается на изотермическое сжатие рабочего вещества?
23) (Ир. 2.123) В каком случае КПД цикла Карно повысится больше: при увеличении температуры нагревателя на значение Δ Т или при уменьшении температуры холодильника на ту же величину?
24) (Пин. 17.1) В сосуде находится гелий, который изобарно расширяется. При этом к нему подводится количество теплоты, равное 15 кДж. На сколько изменится внутренняя энергия газа? Какова работа расширения?
25) (Пин. 17.5) В цилиндрическом сосуде диаметром 28 см находится 20 г азота, сжатого поршнем, на котором лежит груз массой 75 кг. Температура газа 17оС. Какую работу совершит газ, если его нагреть до 250оС? Какое количество теплоты к нему надо подвести? На сколько поднимется поршень с грузом? Процесс считать изобарным, нагреванием сосуда и внешним давлением пренебречь.
26) (Пин. 17.13) Начальное давление воздуха равно 4,0·105 Па, начальный объем 2,0 м3. Газ адиабатически сжали так, что объем уменьшился в 4 раза. Найти конечное давление. Сравнить с давлением, которое получилось бы, если бы сжатие было изотермическим.
При каком процессе надо совершить бóльшую работу по сжатию газа?
| 27) (Пин. 18.17) На рисунке изображен идеализированный цикл бензинового двигателя внутреннего сгорания. Участок 1−2 соответствует адиабатическому сжатию горючей смеси; участок 2−3 – изохорному сгоранию топлива, когда рабочее тело получает количество теплоты Q; участок 3−4 соответствует адиабатическому расширению рабочего тела; участок 4−1 - изохорному выхлопу отработанных газов. Выразить КПД двигателя через степень сжатия газа ξ= V 2/ V 1. | 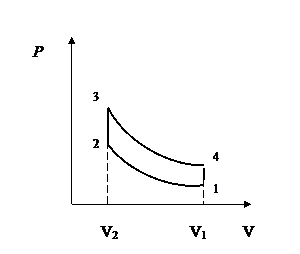
|
28) (Ир.2.137) Найти (в расчете на 1 моль) приращение энтропии углекислого газа при увеличении его термодинамической температуры в 2 раза, если процесс нагревания:
а) изохорический; б) изобарический.
Газ считать идеальным.
29) (Ир. 2.159) Кусок меди массы m 1 =300 г при температуре t 1 =97оС поместили в калориметр, где находится вода массы m 2 =100 г при температуре t 2 =7оС. Найти приращение энтропии системы к моменту выравнивания температур. Теплоемкость калориметра пренебрежимо мала.
30) (Ир. 2.66) Современные вакуумные насосы позволяют получать давления до Р =4·10−10 Па (при комнатной температуре). Найти число молекул газа в 1 см3 и среднее расстояние между ними при этом давлении.
31) (Ир. 2.67) В сосуде объемом m =5,0 л находится азот массы V =1,4 г при температуре Т =1800 К. Найти давление газа, если при этой температуре η =30% молекул диссоциировано на атомы.
33) (Ир. 2.76) Сосуд с газом из жестких двухатомных молекул движется со скоростью v =20м/с. Молярная масса газа М =32 г/моль. найти приращение температуры газа после внезапной остановки сосуда.
34) (Ир. 2.78) Во сколько раз надо адиабатически расширить газ, состоящий из жестких двухатомных молекул, чтобы их средняя квадратичная скорость уменьшилась в η = 1,5 раза?
35) (Ир. 2.79) Азот массы m =15 г находится в закрытом сосуде при температуре Т = 300 К. Какое количество тепла необходимо сообщить азоту, чтобы средняя квадратичная скорость его молекул выросла в η =2,0 раза?
36) (Ир. 2.82) Во сколько раз изменится число ударов жестких двухатомных молекул газа о поверхность стенки в единицу времени, если газ адиабатически расширить в η раз?
37) (Ир. 2.86) Распределение вероятностей значений некоторой величины х описывается функцией f=Ax(a−x) при 0<x<a. Вне этого интервала f =0. Здесь А и а – заданные постоянные. Найти:
а) Наиболее вероятное значение х и соответствующее значение функции f;
б) средние значения х и х 2.
38) (Ир. 2.88) Найти вероятность того, что при Т =300 К молекулы азота имеют компоненты скорости вдоль осей x, y, z соответственно в интервале 300±0,3; 400±0,4 и 500±0,5 м/с.
39) (Ир.2.93) Найти относительное число молекул газа, скорости которых отличаются не более чем на δη =1,0% от значения:
а) Наиболее вероятной скорости;
б) средней квадратичной скорости.
40) (Ир.2.94) Определить температуру газа, для которой:
а) средняя квадратичная скорость молекул водорода больше их наиболее вероятной скорости на Δv =400 м/с;
б) функция распределения молекул кислорода по скоростям f(v) будет иметь максимум при скорости v =420 м/с.
41) (Ир. 2.106) Какая часть одноатомных молекул газа, находящегося в тепловом равновесии, имеет кинетическую энергию, отличающуюся от ее среднего значения на 1,0%?
42) (Ир. 2.114) В очень высоком вертикальном цилиндрическом сосуде находится углекислый газ при некоторой температуре Т. Считая поле тяжести однородным, найти как изменится давление газа на дно сосуда, если температуру газа увеличить в η раз.
43) (Ир. 2.115) Азот находится в очень высоком сосуде в однородном поле тяжести при температуре Т. Температуру увеличили в η раз. На какой высоте h концентрация молекул осталась прежней?