Адиабатический

 Следовательно -
Следовательно -  .
.
Изотермический


Изохорный

 )
)
Первое Начало Термодинамики: 
А для идеального газа 
Таким образом,  где
где  — число степеней свободы частиц газа.
— число степеней свободы частиц газа.
Изобарный


CP=δQ/νΔT=CV+R=((i+2)/2)*R
Уравнение Майера - ур-ние, устанавливающее связь между теплоёмкостями при пост, давлении Cp и пост объёме СV 1 кмоля идеального газа:  где R- газовая постоянная. Впервые было получено Ю. P. Майером в 1842 и ещё до работ Дж. П. Джоуля использовано им для количеств, определения механического эквивалента теплоты. Для произвольной массы m (кг) вещества в состоянии идеального газа уравнение Майера записывается в виде:
где R- газовая постоянная. Впервые было получено Ю. P. Майером в 1842 и ещё до работ Дж. П. Джоуля использовано им для количеств, определения механического эквивалента теплоты. Для произвольной массы m (кг) вещества в состоянии идеального газа уравнение Майера записывается в виде:  , где
, где  - молекулярная масса газа.
- молекулярная масса газа.
5 вопрос. Термодинамика.
Обратимые и необратимые процессы. Второе начало термодинамики.
Ответ:
Процесс называют обратимым, если он допускает возвращение рассматриваемой системы из конечного состояния в исходное через ту же последовательность промежуточных состояний, что и в прямом процессе, но проходимых в обратном порядке. При этом в исходное состояние возвращается не только система, но и среда. Обратимый процесс возможен, если и в системе, и в окружающей среде он протекает равновесно. При этом предполагается, что равновесие существует между отдельными частями рассматриваемой системы и на границе с окружающей средой. Обратимый процесс - идеализированный случай, достижимый лишь при бесконечно медленном изменении термодинамических параметров. Скорость установления равновесия должна быть больше, чем скорость рассматриваемого процесса. Если невозможно найти способ вернуть и систему, и тела в окружающей среде в исходное состояние, процесс изменения состояния системы называют необратимым.
Необратимые процессы могут протекать самопроизвольно только в одном направлении; таковы диффузия, теплопроводность, вязкое течение и другое.
Второе начало термодинамики — физический принцип, накладывающий ограничение на направление процессов передачи тепла между телами.
Второе начало термодинамики гласит, что невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому.
Второе начало термодинамики запрещает так называемые вечные двигатели второго рода, показывая что коэффициент полезного действия не может равняться единице, поскольку для кругового процесса температура холодильника не может равняться абсолютному нулю.
Второе начало термодинамики является постулатом, не доказываемым в рамках термодинамики. Оно было создано на основе обобщения опытных фактов и получило многочисленные экспериментальные подтверждения.
6 вопрос. Физика атомного ядра.
Радиоактивность. Закон радиоактивного распада. Активность нуклида.
Ответ:
Радиоактивный распад — спонтанное изменение состава нестабильных атомных ядер путём испускания элементарных частиц или ядерных фрагментов. Процесс радиоактивного распада также называют радиоактивностью, а соответствующие элементы радиоактивными. Радиоактивными называют также вещества, содержащие радиоактивные ядра.
Закон радиоактивного распада. Пусть за малый промежуток времени Δt количество нераспавшихся ядер N (t) изменилось на ΔN < 0. Так как вероятность распада каждого ядра неизменна во времени, что число распадов будет пропорционально количеству ядер N(t) и промежутку времени Δt: ΔN = –λN(t) Δt
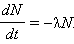
 Коэффициент пропорциональности λ – это вероятность распада ядра за время Δt = 1 с. Эта формула означает, что скорость изменения функции N(t) прямо пропорциональна самой функции.
Коэффициент пропорциональности λ – это вероятность распада ядра за время Δt = 1 с. Эта формула означает, что скорость изменения функции N(t) прямо пропорциональна самой функции.
Решение этого уравнения приводит к экспоненциальному закону: N (t) = N0 e–λt,
где N0 – начальное число радиоактивных ядер при t = 0. За время τ = 1 / λ количество нераспавшихся ядер уменьшится в e ≈ 2,7 раза. Величину τ называют средним временем жизни радиоактивного ядра.
Для практического использования закон радиоактивного распада удобно записать в другом виде, используя в качестве основания число 2, а не e: N (t) = N0 · 2–t/T.
Величина T называется периодом полураспада. За время T распадается половина первоначального количества радиоактивных ядер. Величины T и τ связаны соотношением

Активность нуклида в радиоактивном источнике - величина, равная отношению общего числа распадов радиоактивных ядер нуклида в источнике ко времени распада. Единица А.н. (в СИ) - беккерель (Бк). Внесистемная ед. - кюри (Ки); 1 Ки = 3,700*1010 Бк. Применяют также удельную А. н.: 1) массовую А. н., равную отношению А. н. к массе источника (Бк/кг); 2) объёмную А. н., равную отношению А. н. к объёму источника (Бк/м3); 3) молярную А.н., равную отношению А. н. к кол-ву вещества источника (Бк/моль).
7 вопрос. Термодинамика.
Адиабатический процесс. Уравнение Пуассона.
Ответ:
Адиабатическим называется процесс, при котором отсутствует теплообмен (δQ=0) между системой и окружающей средой. Адиабатическим процессами можно считать все быстропротекающие процессы.
Адиабатический процесс для идеального газа описывается уравнением Пуассона.  Линия, изображающая адиабатный процесс на термодинамической диаграмме, называется адиабатой.
Линия, изображающая адиабатный процесс на термодинамической диаграмме, называется адиабатой.

Уравнение Пуассона.
Для идеальных газов, чью теплоёмкость можно считать постоянной, в случае квазистатического процесса адиабата имеет простейший вид и определяется уравнением

где  — его объём,
— его объём,  — показатель адиабаты,
— показатель адиабаты,  и
и  — теплоёмкости газа соответственно при постоянном давлении и постоянном объёме.
— теплоёмкости газа соответственно при постоянном давлении и постоянном объёме.

 Вывод уравнения Пуассона:
Вывод уравнения Пуассона:
8 вопрос. Квантовая природа излучения.
Тепловое излучение. Спектральная излучательность тела. Спектральная поглощательная способность. Закон Кирхгофа. Абсолютно чёрное тело. Серое тело.
Ответ:
Тела, нагретые до достаточно высоких температур, светятся. Свечение тел, обусловленное нагреванием, называется тепловым (температурным) излучением. Тепловое излучение, являясь самым распространенным в природе, совершается за счет энергии теплового движения атомов и молекул вещества (т. е. за счет его внутренней энергии) и свойственно всем телам при температуре выше 0 К.
Закон излучения Кирхгофа - отношение излучательной способности любого тела к его поглощательной способности одинаково для всех тел при данной температуре для данной частоты и не зависит от их формы и химической природы.
Известно, что при падении электромагнитного излучения на некоторое тело часть его отражается, часть поглощается и часть может пропускаться. Доля поглощаемого излучения на данной частоте называется поглощательной способностью тела  .
.

где  — поток энергии, поглощающейся телом.
— поток энергии, поглощающейся телом.
 — поток энергии, падающий на тело в области
— поток энергии, падающий на тело в области 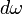 вблизи
вблизи 
С другой стороны, каждое нагретое тело излучает энергию по некоторому закону  , именуемым излучательной способностью тела.
, именуемым излучательной способностью тела.
Согласно закону излучения Кирхгофа:

Тело, способное поглощать полностью при любой температуре все падающее на него излучение любой частоты, называется черным. Следовательно, спектральная поглощательная способность черного тела для всех частот и температур тождественно равна единице.
 — для абсолютно черного тела
— для абсолютно черного тела
Наряду с понятием черного тела используют понятие серого тела — тела, поглощательная способность которого меньше единицы, но одинакова для всех частот и зависит только от температуры, материала и состояния поверхности тела.
 — для серого тела
— для серого тела
9 вопрос. Основы квантовой механики.
Линейный гармонический осциллятор (ЛГО). Квантование энергии ЛГО. Энерния нулевых колебаний
Ответ:
Линейный гармонический осциллятор – это система, совершающая одномерное движение под действием квазиупругой силы. Он является моделью, используемой во многих задачах классической и квантовой теории. Пружинный, физический и математический маятники – примеры классических гармонических осцилляторов. Потенциальная энергия гармонического осциллятора равна:
 , (5.1)
, (5.1)
где  — собственная частота колебаний осциллятора, т — масса частицы. «Потенциальная яма» в данном случае является параболической. Амплитуда малых колебаний классического осциллятора определяется его полной энергией Е. В точках с координатами ±хmax полная энергия Е равна потенциальной энергии. Поэтому с классической точки зрения частица не может выйти за пределы области (– хmax, + хmax).
— собственная частота колебаний осциллятора, т — масса частицы. «Потенциальная яма» в данном случае является параболической. Амплитуда малых колебаний классического осциллятора определяется его полной энергией Е. В точках с координатами ±хmax полная энергия Е равна потенциальной энергии. Поэтому с классической точки зрения частица не может выйти за пределы области (– хmax, + хmax).
Гармонический осциллятор в квантовой механике – квантовый осциллятор – описывается уравнением Шредингера (4.2), учитывающим выражение (5.1) для потенциальной энергии. Тогда стационарные состояния квантового осциллятора определяются уравнением Шредингера вида
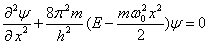 (5.2)
(5.2)
где Е — полная энергия осциллятора. В теории дифференциальных уравнений доказывается, что уравнение (5.2) решается только при собственных значениях энергии
 (5.3)
(5.3)
где 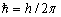 . Формула (5.3)показывает, что энергия квантового осциллятора может иметь лишь дискретные значения, т.е. квантуется. Энергия ограничена снизу отличным от нуля минимальным значением энергии
. Формула (5.3)показывает, что энергия квантового осциллятора может иметь лишь дискретные значения, т.е. квантуется. Энергия ограничена снизу отличным от нуля минимальным значением энергии  . Существование минимальной энергии, называемой энергией нулевых колебаний, представляет собой прямое следствие соотношения неопределенностей.
. Существование минимальной энергии, называемой энергией нулевых колебаний, представляет собой прямое следствие соотношения неопределенностей.
Наличие нулевых колебаний означает, что частица не может находиться на дне «потенциальной ямы», причем этот вывод не зависит от ее формы.
10 вопрос. Физика атомного ядра.
Ядерные реакции. Деление ядра. Ядерные реакторы.
Ответ:
Ядерная реакция – это процесс взаимодействия атомного ядра с другим ядром или элементарной частицей, сопровождающийся изменением состава и структуры ядра и выделением вторичных частиц или γ-квантов.
В результате ядерных реакций могут образовываться новые радиоактивные изотопы, которых нет на Земле в естественных условиях.
Первая ядерная реакция была осуществлена Э. Резерфордом в 1919 году в опытах по обнаружению протонов в продуктах распада ядер. Резерфорд бомбардировал атомы азота α-частицами. При соударении частиц происходила ядерная реакция, протекавшая по следующей схеме: 
Деление ядра — процесс расщепления атомного ядра на два (реже три) ядра с близкими массами, называемых осколками деления. В результате деления могут возникать и другие продукты реакции: лёгкие ядра (в основном альфа-частицы), нейтроны и гамма-кванты. Деление бывает спонтанным (самопроизвольным) и вынужденным (в результате взаимодействия с другими частицами, прежде всего, с нейтронами). Деление тяжёлых ядер — экзотермический процесс, в результате которого высвобождается большое количество энергии в виде кинетической энергии продуктов реакции, а также излучения. Деление ядер служит источником энергии в ядерных реакторах и ядерном оружии.
Ядерный реактор — это устройство, в котором осуществляется управляемая цепная ядерная реакция, сопровождающаяся выделением энергии. Первый ядерный реактор построен и запущен в декабре 1942 года в США под руководством Э. Ферми. Первым реактором, построенным за пределами США, стал ZEEP, запущенный в Канаде в сентябре 1945 года. В Европе первым ядерным реактором стала установка Ф-1, заработавшая 25 декабря 1946 года в Москве под руководством И. В. Курчатова.
К 1978 году в мире работало уже около сотни ядерных реакторов различных типов. Составными частями любого ядерного реактора являются: активная зона с ядерным топливом, обычно окруженная отражателем нейтронов, теплоноситель, система регулирования цепной реакции, радиационная защита, система дистанционного управления. Основной характеристикой ядерного реактора является его мощность. Мощность в 1 МВт соответствует цепной реакции, в которой происходит 3·1016 актов деления в 1 сек.
11 вопрос. Молекулярно-кинетическая теория.
Идеальный газ. Основные законы идеального газа (Бойля-Мариотта, Гей-Люссака, Шарля, Авогадро, Дальтона)
Ответ:
Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.
Уравнение состояния в этой форме называют уравнением Клапейрона–Менделеева.

В случае постоянной массы газа уравнение можно записать в виде:

 (Закон Клапейрона)
(Закон Клапейрона)
Рассмотрим частные газовые законы.
 — Закон Бойля — Мариотта. (Изотермический)
— Закон Бойля — Мариотта. (Изотермический)
 — Закон Гей-Люссака. (Изобарный)
— Закон Гей-Люссака. (Изобарный)
 — Закон Шарля. (Изохорный)
— Закон Шарля. (Изохорный)
Закон Авогадро — при одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится одинаковое число молекул. В одном моле различных веществ содержится NA=6,02·1023молекул (число Авогадро).
Закон Дальтона — давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов: 
Парциальное давление Pn – давление, которое оказывал бы данный газ, если бы он один занимал весь объем.
При  , давление смеси газов:
, давление смеси газов: 
12 вопрос. Молекулярно-кинетическая теория.
Распределение молекул идеального газа по скоростям. Средняя, средне-квадратичная и наиболее вероятная скорости.
Ответ:
При выводе закона распределения молекул по скоростям Максвелл сделал предположение, что газ состоит из огромного числа N тождественных молекул, которые находятся в состоянии беспорядочного теплового движения при одинаковой температуре. Также предполагалось, что силовые поля на газ не действуют.
Закон Максвелла описывается некоторой функцией f(ν), которая называется функцией распределения молекул по скоростям. Если разбить диапазон скоростей молекул на малые интервалы, которые равны dν, то на каждый интервал скорости приходится число молекул dN(ν), имеющих скорость, которая заключена в этом интервале.  Откуда
Откуда 
Применяя методы теории вероятностей, Максвелл получил функцию f(ν) — закон о распределении молекул идеального газа по скоростям:
 (1)
(1)
Скорость, при которой максимальна функция распределения молекул идеального газа по скоростям, называется наиболее вероятной скоростью, значение которой можно найти продифференцировав выражение (1): 

Значения ν =0 и ν =∞ соответствуют минимумам выражения (1), а значение ν, при котором выражение в скобках становится равным нулю, и есть искомая наиболее вероятная скорость ν B: 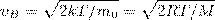 (2)
(2)
Средняя скорость молекулы < ν > (средняя арифметическая скорость) определяется по формуле 
Подставляя сюда f(ν) и интегрируя, получаем  (3)
(3)
Скорости, которые характеризуют состояние газа:
1) наиболее вероятная 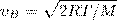
2) средняя 
3) средняя квадратичная 
13 вопрос. Молекулярно-кинетическая теория.
Барометрическая формула. Распределение Больцмана во внешнем потенциальном поле.
Ответ:
При выводе основного уравнения МКТ газов и максвелловского распределения молекул по скоростям предполагалось, что на молекулы газа внешние силы не действуют, поэтому молекулы равномерно распределены по объему. Однако молекулы любого газа находятся в потенциальном поле тяготения Земли. Тяготение и тепловое движение молекул приводят к некоторому стационарному состоянию газа, при котором давление газа с высотой убывает. Больцман обобщил распределение Максвелла на случай поведения частиц в произвольном силовом поле.
Гидростатическое давление столба жидкости или газа:  , где
, где  .
.
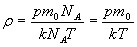 , тогда
, тогда  =>
=>  =>
=>  ;
;
В итоге мы получаем:  − барометрическая формула. Барометрическую формулу можно преобразовать, если воспользоваться выражением
− барометрическая формула. Барометрическую формулу можно преобразовать, если воспользоваться выражением  :
:
 − распределение Больцмана во внешнем потенциальном поле. Из нее следует, что при постоянной температуре плотность газа больше там, где меньше потенциальная энергия его молекул. Если частицы имеют одинаковую массу и находятся в состоянии хаотического теплового движения, то распределение Больцмана справедливо в любом внешнем потенциальном поле, а не только в поле сил тяжести.
− распределение Больцмана во внешнем потенциальном поле. Из нее следует, что при постоянной температуре плотность газа больше там, где меньше потенциальная энергия его молекул. Если частицы имеют одинаковую массу и находятся в состоянии хаотического теплового движения, то распределение Больцмана справедливо в любом внешнем потенциальном поле, а не только в поле сил тяжести.
14 вопрос. Термодинамика.
Теорема Карно.
Ответ:
Сади Карно сформулировал теорему, которая состоит из двух частей.
1. Коэффициент полезного действия любой обратимой тепловой машины, работающей по циклу Карно, не зависит от природы рабочего тела и устройства машины, а является функцией только температуры нагревателя 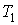 и холодильника
и холодильника  :
:

2. Коэффициент полезного действия любой тепловой машины, работающей по необратимому циклу, меньше коэффициента полезного действия машины с обратимым циклом Карно, при условии равенства температур их нагревателей и холодильников:

Проведем доказательство первой теоремы Карно. Пусть имеются две тепловые машины с общим нагревателем и холодильником, работающие по циклу Карно, но имеющие различные к.п.д. Предположим, что к.п.д. первой тепловой машины больше чем у второй:  . Тогда, запустив первую машину по прямому циклу Карно, а вторую по обратному и соединив их вместе так, чтобы одна машина могла совершать работу над другой, можно будет в такой системе или получать механическую работу за счет отбора теплоты от холодильника, или передавать часть теплоты от холодильника к нагревателю. Как первый, так и второй результат работы такой системы противоречит второму началу термодинамики. Аналогичные рассуждения можно выполнить и в случае, когда
. Тогда, запустив первую машину по прямому циклу Карно, а вторую по обратному и соединив их вместе так, чтобы одна машина могла совершать работу над другой, можно будет в такой системе или получать механическую работу за счет отбора теплоты от холодильника, или передавать часть теплоты от холодильника к нагревателю. Как первый, так и второй результат работы такой системы противоречит второму началу термодинамики. Аналогичные рассуждения можно выполнить и в случае, когда  . Таким образом, для всех тепловых машин, работающих по обратимому циклу Карно, их к.п.д. должен быть одинаков при одинаковых температурах нагревателей и холодильников этих машин.
. Таким образом, для всех тепловых машин, работающих по обратимому циклу Карно, их к.п.д. должен быть одинаков при одинаковых температурах нагревателей и холодильников этих машин.
Вторая теорема Карно может быть обоснована тем, что при протекании необратимого кругового процесса неизбежно произойдет преобразование части работы в теплоту. Это приведет к уменьшению механической работы и, в соответствии с формулой  , к уменьшению к.п.д. тепловой машины в сравнении с идеальной машиной Карно. Следовательно, к.п.д. необратимой тепловой машины всегда будет меньше к.п.д. цикла Карно, если температуры их нагревателей и холодильников одинаковы.
, к уменьшению к.п.д. тепловой машины в сравнении с идеальной машиной Карно. Следовательно, к.п.д. необратимой тепловой машины всегда будет меньше к.п.д. цикла Карно, если температуры их нагревателей и холодильников одинаковы.
15 вопрос. Термодинамика.
Энтропия.
Ответ:
Понятие энтропии впервые было введено в термодинамике для определения меры необратимого рассеяния энергии.


16 вопрос. Молекулярно-кинетическая теория.
Уравнение состояния идеального газа.
Ответ:
Используя зависимость давления идеального газа от его температуры и концентрации молекул
p = nkT,
можно найти связь между основными макроскопическими параметрами газа — объемом V, его давлением p и температурой T.
Концентрация n молекул газа равна
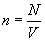 (1)
(1)
где N — число молекул газа в сосуде объемом V. Число N можно выразить как произведение количества вещества 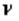 на постоянную Авогадро N A:
на постоянную Авогадро N A:
 (2)
(2)
Из выражений (1) и (2) получаем
 (3)
(3)
Произведение постоянной Авогадро N A на постоянную Больцмана k называется молярной газовой постоянной R. Молярная газовая постоянная равна
 (4)
(4)
Используя молярную газовую постоянную, выражение (3) преобразуем в уравнение
 (5)
(5)
Количество вещества  можно найти, зная массу вещества m и его молярную массу M:
можно найти, зная массу вещества m и его молярную массу M:
 (6)
(6)
поэтому уравнение (5) можно записать в такой форме:
 (7)
(7)
Это уравнение называется уравнением состояния идеального газа.
17 вопрос. Физика атома.
Водородоподобные атомы. Энергетические состояния электронов. Квантовые числа.
Ответ:
Водородоподобный атом — атом, содержащий в электронной оболочке один и только один электрон (водород и его тяжёлые изотопы - дейтерий и тритий).


Квантовые числа — энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
1. Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3,...)
2. Орбитальное квантовое число l определяет форму атомной орбитали. Оно может принимать целочисленные значения от 0 до n -1 (l = 0, 1, 2, 3,..., n -1). Каждому значению l соответствует орбиталь особой формы.
Орбитали с l = 0 называются s-орбиталями,
l = 1 – р-орбиталями (3 типа, отличающихся магнитным квантовым числом m),
l = 2 – d-орбиталями (5 типов),
l = 3 – f-орбиталями (7 типов).
3. Магнитное квантовое число m определяет ориентацию орбитали в пространстве относительно внешнего магнитного или электрического поля. Его значения изменяются от + l до - l, включая 0. Например, при l = 1 число m принимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-АО: рx, рy, рz.
4. Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и -1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона, называемого спином. Для обозначения электронов с различными спинами используются символы:  и
и  .
.
18 вопрос. Физика атомного ядра.
Состав ядра. Изотопы и изобары. Энергия связи атомного ядра. Дефект массы.
Ответ:
Атомное ядро состоит из элементарных частиц — протонов и нейтронов (протонно-нейтронная модель ядра была предложена российским физиком Д. Д. Иваненко, а впоследствии развита В. Гейзенбергом).
Протон (р) имеет положительный заряд, равный заряду электрона. Нейтрон (n) — нейтральная частица. Протоны и нейтроны называются нуклонами.
Ядро обозначается тем же символом, что и нейтральный атом:  , гдеХ — символхимического элемента, Z атомный номер (число протонов в ядре), А — массовоечисло (число нуклонов в ядре).
, гдеХ — символхимического элемента, Z атомный номер (число протонов в ядре), А — массовоечисло (число нуклонов в ядре).
Ядра с одинаковыми Z, но разными А называются изотопами, а ядра с одинаковыми А, но разными Z — изобарами. Например, водород (Z =1) имеет три изотопа:  Н—протий (Z =1, N =0),
Н—протий (Z =1, N =0),  Н—дейтерий (Z =1, N =1),
Н—дейтерий (Z =1, N =1),  Н — тритий (Z =1, N =2). Изотопы одного и того же химического элемента обладают одинаковыми химическими и почти одинаковыми физическими свойствами. Примером ядер-изобар могут служить ядра
Н — тритий (Z =1, N =2). Изотопы одного и того же химического элемента обладают одинаковыми химическими и почти одинаковыми физическими свойствами. Примером ядер-изобар могут служить ядра  Ве,
Ве, 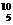 В,
В,  С.
С.
Энергия связи ядра определяется величиной той работы, которую нужно совершить, чтобы расщепить ядро на составляющие его нуклоны без придания им кинетической энергии.
Уменьшение массы ядра при его образовании объясняется выделением энергии связи. Если W св – величина энергии, выделяющейся при образовании ядра, то соответствующая ей масса  называется дефектом массы и характеризует уменьшение суммарной массы при образовании ядра из составляющих его нуклонов.
называется дефектом массы и характеризует уменьшение суммарной массы при образовании ядра из составляющих его нуклонов.
Если ядро массой М яд образовано из Z протонов с массой mp и из (A – Z) нейтронов с массой mn, то: 
Вместо массы ядра М яд величину ∆ m можно выразить через атомную массу М ат:  где mН – масса водородного атома.
где mН – масса водородного атома.
Дефект массы служит мерой энергии связи ядра: 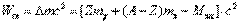
Удельной энергией связи ядра ωсв называется энергия связи, приходящаяся на один нуклон: 
19 вопрос. Молекулярно-кинетическая теория.
Основное уравнение идеальных газов.
Ответ:
Основное уравнение МКТ связывает макроскопические параметры (давление, объём, температура) газовой системы с микроскопическими (масса молекул, средняя скорость их движения).
Пусть имеется кубический сосуд с ребром длиной  и одна частица массой
и одна частица массой  в нём.
в нём.
Обозначим скорость движения 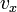 , тогда перед столкновением со стенкой сосуда импульс частицы равен
, тогда перед столкновением со стенкой сосуда импульс частицы равен  , а после
, а после  , поэтому стенке передается импульс
, поэтому стенке передается импульс  . Время, через которое частица сталкивается с одной и той же стенкой, равно
. Время, через которое частица сталкивается с одной и той же стенкой, равно  . Отсюда следует:
. Отсюда следует: 
Так как давление  , следовательно сила
, следовательно сила 
Подставив, получим:  Преобразовав:
Преобразовав: 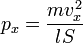
Так как рассматривается кубический сосуд, то 
Отсюда:  . Соответственно,
. Соответственно,  и
и  .
.
Таким образом, для большого числа частиц верно следующее:  , аналогично для осей y и z.
, аналогично для осей y и z.
Поскольку 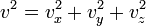 , то
, то  .
.
Отсюда  или
или  .
.
Пусть  — среднее значение кинетической энергии всех молекул, тогда:
— среднее значение кинетической энергии всех молекул, тогда:
 , откуда
, откуда  .
.
 , где k является постоянной Больцмана (отношение универсальной газовой постоянной R к числу Авогадро NA), i — число степеней свободы молекул, а T - абсолютная температура.
, где k является постоянной Больцмана (отношение универсальной газовой постоянной R к числу Авогадро NA), i — число степеней свободы молекул, а T - абсолютная температура.
20 вопрос. Физика атомного ядра.
Ядерные силы и их свойства. Модели атомного ядра.
Ответ:
Между составляющими ядро нуклонами действуют особые, специфические для ядра силы, значительно превышающие кулоновские силы отталкивания между протонами. Они называются ядерными силами.
С помощью экспериментальных данных по рассеянию нуклонов на ядрах, ядерным превращениям и т.д. доказано, что ядерные силы намного превышают гравитационные, электрические и магнитные взаимодействия и не сводятся к ним.
Перечислим основные свойства ядерных сил:
1. ядерные силы являются силами притяжения
2. ядерные силы являются короткодействующими — их действие проявляется только на расстояниях примерно 10–15 м.
3. ядерным силам свойственна зарядовая независимость
4. ядерным силам свойственно насыщение, т. е. каждый нуклон в ядре взаимодействует только с ограниченным числом ближайших к нему нуклонов.
5. ядерные силы зависят от взаимной ориентации спинов взаимодействующих нуклонов.
6. ядерные силы неявляются центральными
Модели ядра:
1. Капельная модель ядра. (1936; Н. Бор и Я. И. Френкель) В этой модели атомное ядро рассматривается как сферическая капля заряженной жидкости. Основанием для такой аналогии послужило то, что плотность ядерного вещества у всех ядер вблизи линии стабильности приблизительно одинакова, что говорит о его несжимаемости. Кроме того, с жидкостью ядерное вещество сближает и свойство насыщения ядерных сил.
2. Оболочечная модель ядра. (1949; М. Гепперт-Майер и X. Иенсен). Предполагает распределение нуклонов в ядре по дискретным энергетическим уровням, заполняемым нуклонами согласно принципу Паули, и связывает устойчивость ядер с заполнением этих уровней.
По мере дальнейшего накопления экспериментальных данных о свойствах атомных ядер появлялись все новые факты, не укладывающиеся в рамки описанных моделей. Так возникли обобщенная модель ядра (синтез капельной и оболочечной моделей), оптическая модель ядра (объясняет взаимодействие ядер с налетающими частицами) и другие модели.
21 вопрос. Квантовая природа излучения.
Основные законы теплового излучения (Стефана-Больцмана, Вина, Рэлея и Джинса, Планка)
Ответ:


Закон Рэлея и Джинса - закон, выражающий распределение энергии в спектре абсолютно чёрного тела в зависимости от температуры.
Закон может быть записан в виде:

где u ν — плотность излучения, соответствующая частоте ν,
с — скорость света,
Т — абсолютная температура,
k — постоянная Больцмана.
22 вопрос. Газ, жидкость, твердое тело.
Фазовые переходы 1-го и 2-го рода. Диаграмма состояния.
Ответ:
Фазовые переходы - переходы вещества из одной фазы в другую, происходящие при изменении температуры, давления или под действием каких-либо других внешних факторов (например, магнитных или электрических полей).
Фазовый переход I рода (например, плавление, кристаллизация и т. д.) сопровождается поглощением или выделением теплоты, называемой теплотой фазового перехода. Фазовые переходы I рода характеризуются постоянством температуры, изменениями энтропии и объема.
Фазовые переходы, не связанные с поглощением или выделением теплоты и изменением объема, называются фазовыми переходами II рода. Эти переходы характеризуются постоянством объема и энтропии, но скачкообразным изменением теплоемкости. Общая трактовка фазовых переходов II рода предложена академиком Л. Д. Ландау (1908—1968). Согласно этой трактовке, фазовые переходы II рода связаны с изменением симметрии: выше точки перехода система, как правило, обладает более высокой симметрией, чем ниже точки перехода. Пример фазовых переходов II рода: переход ферромагнитных веществ (железа, никеля) при определенных давлении в температуре в парамагнитное состояние.
 Для наглядного изображения фазовых превращений используется диаграмма состояния, на которой в координатах р,Т задается зависимость между температурой фазового перехода и давлением в виде кривых испарения (КИ), плавления (КП) и сублимации (КС), разделяющих поле диаграммы на три области, соответствующие условиям существования твердой (ТТ), жидкой (Ж) и газообразной (Г) фаз. Кривые на диаграмме называются кривыми фазового
Для наглядного изображения фазовых превращений используется диаграмма состояния, на которой в координатах р,Т задается зависимость между температурой фазового перехода и давлением в виде кривых испарения (КИ), плавления (КП) и сублимации (КС), разделяющих поле диаграммы на три области, соответствующие условиям существования твердой (ТТ), жидкой (Ж) и газообразной (Г) фаз. Кривые на диаграмме называются кривыми фазового