Вопросы зачетные 1 ЛД 2018
Предмет и задачи курса «ХИМИЯ»
Теоретические основы титриметрического анализа. Закон эквивалентов.
Классификация объемных методов анализа.. Метод кислотно-основного титрования.
Первое начало термодинамики. Энтальпия. Законы Гесса.
Второе начало термодинамики..Энтропия.
Критерии протекания процессов в закрытых системах. Энергия Гиббса..
Кинетические уравнения. Константа скорости реакций. Порядок реакции.
Зависимость скорости реакций от различных факторов.
Химическое равновесие. Константа скорости реакции. Факторы влияющие на химическое равновесие.
Катализ. Ферментативный катализ. Уравнение Мих–Меэнтана.
Протолитическая теория кислот и оснований Бренстеда.
Теория кислот и оснований Льюиса.
Гидролиз солей.Биологическое значение гидролиза.
Термодинамика растворения. Закон распределения.
Растворимость газов. Кесонная и горная болезни.
Свойства растворов слабых и сильных электролитов. Степень диссоциации. Уравнение Оствальда.
Коллигативные свойства растворов.Криоскопия и эбуллиоскопия.
Осмос. Осмотическое давление.Закон Рауля.
Буферные системы крови. Коррекция кислотно-основного состояния организма.
Общая характеристика эссенциальныых элементов. Элементы комплексообразователи в in vivo.
Строение,номенклатура и классификация комплексных соединений.
Окислители и восстановители в in vivo и in vitro.Методы уравнивания ОВР.
Классификация о-в реакций. Эквивалент окислителя и восстановителя.
Классификация,методы получения и очистки дисперсных систем. Диаиз. и гемодиализ.
Электрические свойства дисперсных систем. Строение мицеллы.
Устойчивость коллоидных растворов. Когуляция коллоидных растворов.Правило Шульце-Гарди.
Изоэлектрическая точка аминокислот и полиамфолитов.
Осмотическое давление и мембранное равновесие биополимеров.
Пептизация и коллоидная защита.
Специфические свойства поли - и гетерофункциональных соединений.
Стериоизомерия.Формулы Фишера. R и S, E, Z – номенклатура. D и L-соединения.
Биологически активные соединения, содержащие пиррольное кольцо (пиррол, тетрапиррольные соединения, гем).
Медико-биологическое значение фурана,тиофена и индола.
Пиридин и хинолин и их производные.
Пиримидин, пиридазин и их производные.
Пурин и его производные.
37.Классификация и номенклатура и стериоизомерия α-аминокислот.
38.Кислотно-основные свойства и биполярная структура α-аминокислот.
39.Химические свойства α-аминокислот (реакции этерификации, ацилирование, алкилирование, образование иминов и т.д)
40.Биологически важные реакции α-аминокислот. Пиридоксальный катализ.
Установление первичной структуры пептидов и белков.
Понятие о вторичной, третичной и четвертичной структуре белка.
Классификация и строение моносахаридов.
44.Цикло-оксотаутомерия моносахаридов.
45.Окисление и восстановление моносахаридов.Эпимеризация и изомеризация моноз..
Участие фосфатов моносахаридов в биохимических реакциях.
Классификация дисахаридов. Восстанавливающие и не восстанавливающие дисахариды. Строение и гидролиз.
Гомополисахариды: крахмал (амилоза и амилопектин). Гидролиз.
Строение гликогена и пектовой кислоты. Гидролиз.
Строение гиалуроновой кислоты и хондриатинсульфатов.
Нуклеозиды и нуклеотиды. Гидролиз нуклеотидов.
Строение и функции ДНК и РНК
Нуклеиновые коферменты НАДН, НАДФН,ФАДН2
Строение и функции АТФ. Принцип энергетического сопряжения.
Жиры и масла. Гидролиз.
56.β-окисление жирных кислот.
Фосфатидилсерины, кефалины, лецитины – структурные единицы клеточных мембран.
Сфинголипиды,. Строение церамидов и сфингомиелинов. Биологическая роль.
Холестерин, Эргостерин, превращение его в витамины группы Д.
Примерные задачи к зачету по химии
1.Какое вещество образуется, если к 100 мл раствора H3PO4 с молярной концентрацией 0,4 моль/л добавили гидроксид кальция массой 1.4 г. Вычислим массу образовавшейся соли.
2.Вычислите молярную концентрацию эквивалента раствора H2SO4C(H2SO4)=0,1 моль/г для реакции
 H2SO4+Ca(OH)2
H2SO4+Ca(OH)2
3.Вычислите массу карбоната натрия в растворе объемом 25 мл, если на титрование 10 мл этого раствора израсходовано 15,2 мл HCl с концентрацией 0,101 моль/л.
4.Вычислить стандартную энтальпию реакции, используя значение стандартных энтальпий сгорания:

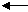 C6H12O6(г) 2C2H5OH(ж)+ 2CO2(г)
C6H12O6(г) 2C2H5OH(ж)+ 2CO2(г)
∆Hcт(C6H12O6)= - 2810 кДж/моль
∆Hcт(C2H5OH)= - 1371 кДж/моль
5.Для обратимой реакции:

 CO(г)+Cl2(г) COCl2(г)
CO(г)+Cl2(г) COCl2(г)
константа равновесия равна 6,386 при 600°С. Установите, в каком направлении будет протекать реакция, если в 1 литре реакционной смеси находиться 1 моль CO и 1 моль Cl2.
6.Сделайте заключение о практическом обратимости реакции в стандартном состоянии, рассчитать константу равновесия при 310 К для реакции:
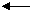
 АТФ+АМФ 2АДФ
АТФ+АМФ 2АДФ
∆G= - 2,10 кДж/моль
7.Вычислите степень ионизации аммиака в растворе с концентрацией 1 .10-1 моль/л.
8.Вычислите температуру замерзания водного раствора рибозы с массовой долей 2%, при K(H2O)=1,8 K.кг/моль.
9.Температура замерзания раствора содержащего 10 г вещества в 150 г бензола, равна 2,07°С. Вычислите молярную массу этого вещества, при K(бензола)=5,07 К .кг/моль.
10.Вычислите осмотическое давление раствора глицерина с массовой долей 1% (ρ=1,0006 г/мл) при температуре 25°С. Будет ли он изотоничен раствору с осмотическим давлением 500 кПа.
11.Для процесса растворения KCl в H2O∆H°=17,2 кДж/моль, ∆S=75,7 Дж (моль.К). Вычислите ∆G растворения.
12.Рассчитайте ионную силу плазмозамещающего раствора, который готовят из NaCl= 0,5г; KCl= 0,1г; NaHCO3=0,4г; H2O=100мл.
13.При отравлении цианидами внутривенно вводят NaNO3c массовой долей 2% с ρ=1,011 г/мл. Вычислите активность ионов в этом растворе.
14.Гидроксид натрия массой 90 г растворили 750 мл H2O, раствор кипит при 102,65°С. Вычислите изотонический коэффициент NaOH в растворе.
15.Скорость ферментативной реакции в 107 раз больше, чем без фермента при 300° К. Какова разность энергий активации этих процессов.
16.К 100 мл крови для изменения Ph от 7,36 до 7,0 надо добавить 36 мл
0,05 М HCl. Рассчитать буферную емкость крови по кислоте.
17.Венозная кровь имеет РH-7,33, а артериальная РH -7,36. Вычислить число ионов водорода в 100 мл той и другой крови.
18.Какой объем 0,1 Н HNO3можно приготовить из 0,7 л HNO3 с массовой долей 30% (ρ=1,18 г/мл)?
19.Вычислить молярность и нормальность:
а) массовая доля(Ba(OH)2)= 6,91, ρ (Ba(OH)2)=1,04 г/мл.
б) массовая доля (КAl(SO4)2)=5,97, ρ(КAl(SO4)2) =1,053 г/мл.
20.Вычислите концентрацию иона цинка в растворе тетрагидроксоцинката натрия с концентрацией 0,3 моль/л при избытке ГИДРОКСИД иона. К нест (1-4)=2,4.10-20.
21.Напишите строение мицелл гидрозоля BaSO4, полученного по реакции BaCl2+Na2SO4.→
22.По одну сторону мембраны находиться раствор белка с концентрацией 0,1 моль/л, по другую раствор NaCl с концентрацией 0,2 моль/л. Вычислите их концентрации после установления равновесия.