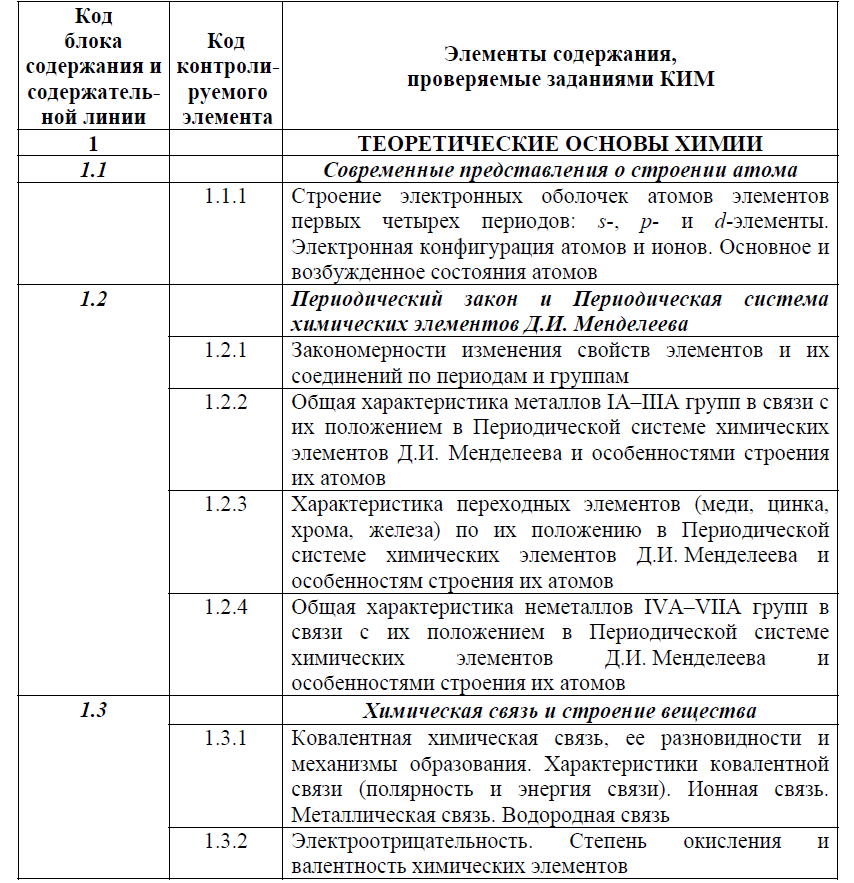
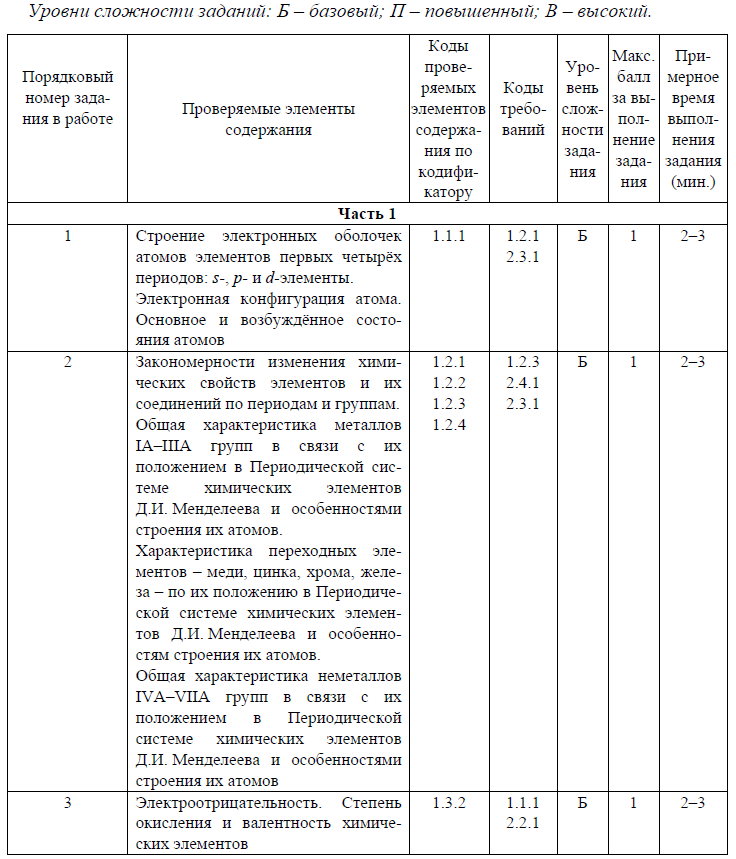
Строение электронных оболочек
Провал электрона у Cr (4s13d5) и Cu (4s13d10), а также у всех d-элементов под ними в таблице.
Для элементов главных подгрупп: Валентные электроны = Внешние электроны
Для элементов побочных подгрупп: Валентные электроны = Внешние электроны (s) + d-электроны предвнешнего уровня.
Пример: N – 5 группа – главная подгруппа – 5 внешних электронов – 5 валентных электронов
Mn – 7 группа – побочная подгр. – 2 внешних электрона (4s2) – 7 валентных электронов (4s2 + 3d5)
Число валентных электронов не может быть больше модуля максимальной/минимальной степени окисления.
Пример: F – 7 группа – 1 валентный электрон, так как F никогда не принимает СО +/- 7
O – 6 группа – 2 валентных электрона, так как принимает СО -2, -1, +2
Zn – 2 группа, побочная подгруппа – 2 валентных, так как постоянная СО +2.
Изменение свойств по ПСХЭ
Стоит запомнить 4 элемента с самой высокой электроотрицательностью, так как по таблице правильно определить невозможно.
Si B H As P Se C S I Br Cl N O F
СО, валентность
Знать постоянные степени окисления идеально. Помнить про SiH4−1.
Степень окисления у инертных газов (VIIIA группа) всегда = 0.
Степени окисления часто встречаемых элементов
| Fe +2, +3, +6 Cr +2, +3, +6 Cu +1, +2 Mn +2, +4, +6, +7 Pb +2, +4 Ag +1, +2 | Cl, Br -1, +1, +3, +5, +7 I -1, +1, +3, +5 S -2, +2, +4, +6 N -3, +1, +2, +3, +4, +5 P -3, +1, +3, +5 C, Si -4, +2, +4 |
Высшая степень окисления не всегда равна номеру группы.
Пример: d-металлы – Fe – 8 группа – высшая СО = +6 (знаем из темы)
О – 6 группа – высшая СО = +2 (знаем из темы)
Низшая степень окисления Металлов = 0.
Валентность – способность атома данного элемента образовывать определенное число химических связей другими атомами.
Некоторые элементы имеют постоянную валентность:
| Водород Н, щелочные металлы, серебро Ag, фтор F | I |
| Щелочно-земельные металлы, цинк Zn, кислород О | II |
| Алюминий Al | III |
В большинстве случаев валентность равна модулю степени окисления, кроме:
- простых веществ:
| Вещество | СО | Структурная формула | Валентность |
| H2, Hal2 | H-H, Hal-Hal | I | |
| O2 | O=O | II | |
| N2 | N≡N | III |
- некоторых других:
валентность N в HNO3 и N2O5 = IV, хотя СО = +5;
валентность N в NH4+ = IV, хотя СО = -3;
валентность О в пероксидах (Na2O2) = II(постоянная), хотя СО = -1 (Na-O-O-Na).
В органических соединениях: СIV, HI, OII, NIII.
Химическая связь. Кристаллические решетки.
Помнить наизусть вещества с Д-А механизмом образования ковалентной связи:
H3O+, NH4+, CO, NO2, HNO3, нитраты, PH4+, BF4-, комплексы
В молекуле может сочетаться несколько типов связей:
CaSO4 – ионная и ковалентная полярная; NH4Cl – ионная и ковалентная полярная
В пероксидах всегда есть ковалентная неполярная связь: H-O-O-H, Na-O-O-Na.
Водородная связь – это связь между молекулами, может образовываться в соединениях, в которых есть фрагмент О-Н, F-H или N-H.
В неорганике: H2O, H2O2, NH3, HF… В органике: спирты, фенол, КК….
Помнить наизусть вещества с атомной КР:
С (алмаз, графит), Si, Ge, B, P (красный, черный), SiO2, H2SiO3, CaC2, SiC, BN, Fe3C, Al2O3
Определяем строение и решетку по таблице:
| Строение | Молекулярное | Немолекулярное | ||
| Кристаллическая решетка | Молекулярная | Ионная | Металлическая | Атомная |
| Химическая связь | Ковалентная | Ионная | Металлическая | Вещества – исключения |
| Состав молекулы | неМеталлы | Металл+неМеталл (Kat+An−) | Металл | Вещества – исключения |
Определяем всегда снизу.
Если в вещества есть ионная связь, вещество 100% с ионной КР.
Пример: CH3COOK – есть ковалентная и ионная связь – решетка ионная.