Джеффризу с соавторами удалось впервые показать, что зонды на основе корпоследовательности ГВР могут быть использованы для одновременного выявления большого количества соответствующих генетических локусов. С помощью зонда, синтезированного путем тандемного лигирования 33 повторяющихся элементов ГВР из гена человеческого миоглобина, они обнаружили на Саузернблотах, несущих гидролизат геномной ДНК человека, картину из большого числа полос. Некоторые из них оказались полиморфными последовательностями. Для выделения этих родственных участков исследователи отобрали из геномной библиотеки соответствующие клоны, используя в качестве зонда при гибридизации в мягких условиях конкатенированные повторы из гена миоглобина. Когда же эти выделенные клоны, в свою очередь, выступили в роли зондов, с помощью некоторых из них в геномной ДНК удалось выявить сложную картину гипервариабельных полос. Клоны содержали последовательности, имеющие области гомологии с тандемными повторами миоглобиновых ГВР, которые и представляли собой общие для этой группы корпоследовательности. Последовательности этого семейства были названы минисателлитами. Для изучения доступны два из них, являющиеся вариантами основной корпоследовательности. Соответствующие зонды, названные 33.6 и 33.15, существуют в виде рекомбинантных форм векторов, полученных на основе бактериофага М13. Каждая из них выявляет около 15 высокополиморфных полос в диапазоне 4–20 т. п.н. Среднее значение гетерозиготности по этим полосам около 90%, при этом вариабельность пропорциональна длине фрагмента и наибольший фрагмент фактически на 100% гетерозиготен в популяции.
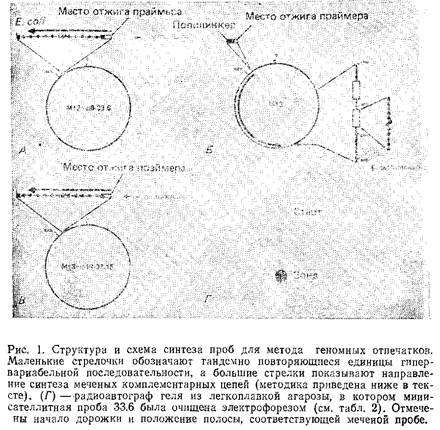
1.1.1 Приготовление минисателлитных зондов
Одноцепочечные матрицы для синтеза зондов можно легко и быстро получить, используя стандартные методики.
Матрицы, приготовленные по методике из табл. 1, обычно получаются в концентрации около 100 мг/мкл, однако лучше оценить концентрацию данной партии путем сравнения со стандартными растворами в геле, окрашенном бромидом этидия.
Учитывая, что молекула матрицы является одноцепочечной и кольцевой, ее нельзя пометить с помощью рассеянных затравок или методами никтрансляции. В этом случае следует воспользоваться техникой достройки праймера.
По этой методике синтетический олигонуклеотид, комплементарный последовательности, находящейся со стороны З-конца минисателлитной вставки, отжигается на матрице в растворе. В результате чего появляются З'-гидроксильные группы, к которым большой фрагмент ДНК-полимеразы I может присоединить меченые дезоксирибонуклеозиды. По истечении времени, необходимого для синтеза комплементарной цепи по всей длине вставки, можно использовать рестриктазу для расщепления новой двухцепочечной молекулы у б'-конца вставки.
Последовательность является частью фагового гена III, кодирующего белок, который участвует в прикреплении к бактериальным F-лилям в ходе инфекции и содержит два участка GC-богатых тандемных повторов. Эти последовательности отжигаются с конкурентной ДНК, содержащейся в большинстве гибридизационных буферов, поэтому для получения картины геномных «отпечатков пальцев» необходимо исключить этот компонент при использовании указанного зонда.
Семейство ГВР, выявляемое тандемным повтором из гена III бактериофага М13, отличается от семейств детектируемых с помощью минисателлитных зондов 33.6 и 33.15, но сходно с ними высокой степенью полиморфизма, а также тем, что частота аллелей уменьшается пропорционально их размерим. Средняя частота совпадения для одной полосы у индивидов европейского происхождения, не находящихся в родстве, составляет около 0,20 для фрагментов больше 2 т. п.н., причем для отдельного индивида таких полос выявляется 15–20. Таким образом, тандемный повтор М13 выявляет картину «отпечатков ДНК», сравнимую по своей сложности с картинами, получаемыми при использовании минисателлитов, и позволяет проанализировать 15 – 20 дополнительных гипервариабельных участков в ДНК человека и других млекопитающих. Так как повтор М13 не содержит сайтов узнавания для рестриктаз Hinll, Mbol, НаеШ и Alul и поскольку распределение детектируемых фрагментов сходно с таковым для отпечатков, полученных с помощью минисателлитов, представляется удобным и эффективным готовить блоты для гибридизации по очереди с каждой из трех, проб.

1.2.1 Приготовление зонда на основе гена 111 фага М13
Тандемные повторы М13 локализуются в положениях 1700–1900 и 2300–2500 фагового генома. Можно использовать эти данные и свойства фагового вектора для синтеза гибридизационного зонда с высокой удельной активностью. После отжига 17-нуклеотидного секвенационного праймера на одноцепочечной ДНК-матрице любого из фагов М13 серии и достройки второй цепи фрагментом Клёнова с участием меченых дезоксинуклеозидтрифосфатов, реакцию останавливают добавлением соли. Если время инкубации выбрано таким образом, что удвоение цепи происходит не далее гена III, то вновь синтезированная цепь длиной до 4,5 т. п.н. содержит меченые нуклеотиды, а проксимальная часть генома фага М13 длиной 2,5 т. п.н., имеющая тандемные повторы, остается одноцепочечной. Это позволяет тандемному повтору гибридизоваться с комплементарными последовательностями ДНК, иммобилизованной на фильтре, и тем самым делает возможным использование меченой ДНК фага в качестве гибридизационной пробы. После освобождения от невключившихся меченых нуклеотидов можно измерить удельную активность ДНК-зонда, которая обычно варьирует в пределах 1–2ХЮ9 имп./мин/мкг ДНК матрицы. Однако, по-видимому, очистка зонда на колонке с сефадексом, снижает его гибридизационную активность, поэтому лучше избегать этого этапа и использовать в качестве зонда полученную реакционную смесь без дальнейшей ее очистки.
2. Гель-электрофорез и перенос ДНК
С обзором методов гель-злектрофореза можно познакомиться в работе. Однако полезно все же вкратце выделить специфические условия, повышающие эффективность анализа методом геномной дактилоскопии.