- Основные положения теории
- Изменение агрегатного состояния вещества
- Молекулярно-кинетическая теория идеальных газов
- Экспериментальные газовые законы
- Температура - мера средней кинетической энергии
| Основные положения теории | |||||||
 Изображение атомов на поверхности кремния, полученное с помощью туннельного микроскопа. Изображение атомов на поверхности кремния, полученное с помощью туннельного микроскопа.
| Начиная с XVIII века, постепенно стала складываться система научных представлений о строении вещества, позднее названная молекулярно-кинетической теорией (МКТ). Молекулярно-кинетическая теория базируется на трёх положениях, обобщающих результаты большого количества экспериментальных данных:
Рассмотрим эти положения несколько подробней. | ||||||

| Молекулярное строение вещества. Моль вещества. Число Авогадро. Количество вещества.
Современная физика не устанавливает пределы структурной делимости материи, однако, однозначно утверждает, что элементами, определяющими основные физические свойства тел, являются атомы, молекулы и ионы.
Атомом называется наименьшая частица данного химического элемента, являющаяся носителем его свойств. Каждому химическому элементу соответствует свой атом.
Молекула – это устойчивая наименьшая частица данного вещества, обладающая его основными химическими свойствами. Молекула состоит из атомов одинаковых или различных химических элементов.
Ион – электрически заряженная частица, которая образуется при потере или приобретении атомами и молекулами одного или нескольких электронов.
Атомное строение имеют инертные газы (гелий, аргон и др.), жидкости (ртуть) и твердые тела (медь, алмаз). Ряд кристаллических веществ, например, хлористый натрий, состоит из разноимённо заряженных ионов. Однако подавляющее большинство веществ образовано из молекул (углекислый газ, вода), поэтому понятие “молекула” часто используется как общий собирательный термин.
Современная экспериментальная техника позволяет наблюдать молекулярную структуру вещества, а также определять размеры атомов и молекул. Эти размеры весьма малы: для атомов они составляют величину порядка 10–10 м, для молекул их диапазон значительно шире - от 10–10 м для простейших молекул до 10–5 м для молекул сложных органических веществ.
Естественно, что при таких размерах масса атомов и молекул также очень мала, к примеру, масса молекулы водорода составляет 3.3·10–27 кг. Понятно, что оперировать такими величинами в практических расчетах не совсем удобно.
Поэтому было введено понятие относительной молекулярной (атомной) массы Mr, которое определяется как отношение массы молекулы (атома) данного вещества m0 к 1/12 массы атома углерода:
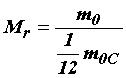 . (1) . (1)
| ||||||


| Число молекул в случае однокомпонентной системы, содержащей молекулы или атомы одного вида, можно найти по формуле:
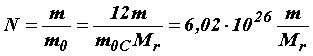 , где m – масса системы, выраженная в килограммах.
Из этой формулы видно, что N имеет очень большие значения, поэтому потребовалось введение некоторого относительного параметра, связанного с числом молекул N в системе, называемого количеством вещества.
В Международной системе единиц (СИ) в качестве такого параметра принят моль – количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в 0.012 кг углерода.
Таким образом, в одном моле любого вещества содержится одно и тоже число молекул или атомов, которое называется числом (постоянной) Авогадро и равно: , где m – масса системы, выраженная в килограммах.
Из этой формулы видно, что N имеет очень большие значения, поэтому потребовалось введение некоторого относительного параметра, связанного с числом молекул N в системе, называемого количеством вещества.
В Международной системе единиц (СИ) в качестве такого параметра принят моль – количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в 0.012 кг углерода.
Таким образом, в одном моле любого вещества содержится одно и тоже число молекул или атомов, которое называется числом (постоянной) Авогадро и равно:
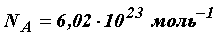 .
Количество вещества n определяется как число молей, равное отношению числа молекул N к числу Авогадро: .
Количество вещества n определяется как число молей, равное отношению числа молекул N к числу Авогадро:
 . (2)
Масса одного моля вещества называется молярной массой. Она равна произведению массы одной молекулы вещества m0 на число Авогадро:
M = m0·NA (3)
и измеряется в килограммах на моль: [ M ] = кг·моль–1.
Из (1), (3) и определения числа Авогадро следует, что между относительной молекулярной массой вещества Mr и его молярной массой M существует соотношение:
M = Mr·10–3 кг·моль–1.
Учитывая равенство
m = N·m0, где m – масса вещества,
по формулам (2) и (3) легко получить ещё одно выражение для количества вещества: . (2)
Масса одного моля вещества называется молярной массой. Она равна произведению массы одной молекулы вещества m0 на число Авогадро:
M = m0·NA (3)
и измеряется в килограммах на моль: [ M ] = кг·моль–1.
Из (1), (3) и определения числа Авогадро следует, что между относительной молекулярной массой вещества Mr и его молярной массой M существует соотношение:
M = Mr·10–3 кг·моль–1.
Учитывая равенство
m = N·m0, где m – масса вещества,
по формулам (2) и (3) легко получить ещё одно выражение для количества вещества:
 , (4)
т. е. количество вещества равно отношению массы этого вещества к его молярной массе.
Тепловое движение молекул.
Беспорядочность, хаотичность движения частиц - важнейшая черта теплового движения. Экспериментальным доказательством непрерывного характера движения молекул является диффузия и броуновское движение.
Диффузия - это явление самопроизвольного проникновения молекул одного вещества в другое.
В результате взаимной диффузии веществ происходит постепенное выравнивание их концентрации во всех областях занимаемого ими объёма.
Установлено, что скорость протекания процесса диффузии зависит от рода диффундирующих веществ и температуры. Одним из наиболее интересных явлений, подтверждающих хаотичность движения молекул, является броуновское движение.Оно представляет собой тепловое движение микроскопических (но состоящих из очень большого числа молекул) частиц вещества, находящихся во взвешенном состоянии в жидкости или в газе, впервые наблюдаемое Р. Броуном. Беспорядочность перемещения таких частиц объясняется тем, что сумма импульсов, полученных ими от молекул с разных сторон, может стать не равной нулю как вследствие разного числа ударов с разных сторон частицы, так и в результате того, что частицу с одной стороны могли ударить молекулы, обладающие большими скоростями, чем молекулы, ударившие ее с другой стороны.
Броуновское движение проявляется тем заметнее, чем меньше частицы и вязкость среды, и чем выше температура системы. Зависимость от температуры свидетельствует о том, что скорость хаотического движения молекул возрастает с увеличением температуры, именно поэтому его и называют тепловым движением.
Взаимодействие молекул.
Межмолекулярные силы имеют электромагнитную природу и сводятся к двум типам - притяжению и отталкиванию. Эти силы являются короткодействующими и проявляются лишь на расстояниях, сравнимых с размерами молекул. Силы притяжения и отталкивания быстро убывают с увеличением расстояния между молекулами, однако скорость их убывания различна. Сила отталкивания преобладает на малых расстояниях и неограниченно растёт по мере приближения расстояния между центрами масс молекул r к некоторой величине d, которую можно рассматривать как эффективный диаметр молекул.
Сила притяжения уменьшается с увеличением r намного медленнее силы отталкивания, поэтому существует некоторое значение межмолекулярного расстояния r = r0, на котором силы отталкивания и притяжения компенсируют друг друга, так что результирующая сила межмолекулярного взаимодействия обращается в нуль. , (4)
т. е. количество вещества равно отношению массы этого вещества к его молярной массе.
Тепловое движение молекул.
Беспорядочность, хаотичность движения частиц - важнейшая черта теплового движения. Экспериментальным доказательством непрерывного характера движения молекул является диффузия и броуновское движение.
Диффузия - это явление самопроизвольного проникновения молекул одного вещества в другое.
В результате взаимной диффузии веществ происходит постепенное выравнивание их концентрации во всех областях занимаемого ими объёма.
Установлено, что скорость протекания процесса диффузии зависит от рода диффундирующих веществ и температуры. Одним из наиболее интересных явлений, подтверждающих хаотичность движения молекул, является броуновское движение.Оно представляет собой тепловое движение микроскопических (но состоящих из очень большого числа молекул) частиц вещества, находящихся во взвешенном состоянии в жидкости или в газе, впервые наблюдаемое Р. Броуном. Беспорядочность перемещения таких частиц объясняется тем, что сумма импульсов, полученных ими от молекул с разных сторон, может стать не равной нулю как вследствие разного числа ударов с разных сторон частицы, так и в результате того, что частицу с одной стороны могли ударить молекулы, обладающие большими скоростями, чем молекулы, ударившие ее с другой стороны.
Броуновское движение проявляется тем заметнее, чем меньше частицы и вязкость среды, и чем выше температура системы. Зависимость от температуры свидетельствует о том, что скорость хаотического движения молекул возрастает с увеличением температуры, именно поэтому его и называют тепловым движением.
Взаимодействие молекул.
Межмолекулярные силы имеют электромагнитную природу и сводятся к двум типам - притяжению и отталкиванию. Эти силы являются короткодействующими и проявляются лишь на расстояниях, сравнимых с размерами молекул. Силы притяжения и отталкивания быстро убывают с увеличением расстояния между молекулами, однако скорость их убывания различна. Сила отталкивания преобладает на малых расстояниях и неограниченно растёт по мере приближения расстояния между центрами масс молекул r к некоторой величине d, которую можно рассматривать как эффективный диаметр молекул.
Сила притяжения уменьшается с увеличением r намного медленнее силы отталкивания, поэтому существует некоторое значение межмолекулярного расстояния r = r0, на котором силы отталкивания и притяжения компенсируют друг друга, так что результирующая сила межмолекулярного взаимодействия обращается в нуль.
| ||||||
| Изменение агрегатного состояния вещества | |||||||
| Агрегатные состояния Всякое вещество может находиться в трёх агрегатных состояниях: в твёрдом, жидком и газообразном. | |||||||

| В газах средняя кинетическая энергия теплового движения молекул значительно превосходит потенциальную энергию их взаимодействия. В этом случае силы взаимодействия между молекулами весьма слабо влияют на характер их относительного движения, поскольку молекулы находятся на достаточно большом расстоянии друг от друга. По мере уменьшения температуры или при сжатии взаимодействие молекул начинает играть настолько существенную роль, что газ в конце концов переходит в конденсированное состояние - жидкость. В жидкости средняя энергия взаимодействия молекул примерно равна средней энергии теплового движения. Тепловое движение нарушает связь между молекулами и приводит к перемещению их относительно друг друга внутри объёма жидкости. В связи с этим жидкость принимает форму сосуда, в который она помещена. | ||||||

| Под твердыми телами обычно подразумеваются кристаллы, характерной особенностью которых является регулярное расположение в них атомов или ионов. О совокупности точек, в которых расположены атомные ядра, говорят как о кристаллической решетке, а сами эти точки называют узлами решетки. Тепловое движение атомов или ионов кристалла носит в основном колебательный характер. Однако, поскольку в кристалле кинетическая энергия колебательного движения атомов значительно меньше абсолютного значения потенциальной энергии их взаимодействия, то тепловое движение не может разрушить связь между атомами. Поэтому твердое тело, в отличие от жидкости, сохраняет свою форму и обладает большой механической прочностью. | ||||||

| Кроме кристаллических тел существуют аморфные тела. Они, хотя и рассматриваются обычно как твердые, представляют собой переохлажденные жидкости. Если рассматривать некоторый атом аморфного тела как центральный, то ближайшие к нему атомы будут располагаться в определенном порядке, но по мере удаления от "центрального" атома этот порядок нарушается и расположение атомов становится случайным. К аморфным телам относятся стекло, пластмассы и т.д. | ||||||

| Переход из одного агрегатного состояния в другое (при постоянном давлении) происходит при строго определённой температуре и всегда связан с выделением или поглощением некоторого количества тепла. Переход вещества из одного состояния в другое происходит не мгновенно, а в течении некоторого времени, когда два состояния вещества существуют одновременно в тепловом равновесии. Плавление и кристаллизация По мере возрастания температуры энергия колебательного движения атомов в твёрдом теле возрастает и, наконец, наступает такой момент, когда связи между атомами начинают разрываться. При этом твердое тело переходит в жидкое состояние. Такой переход называется плавлением.При фиксированном давлении плавление происходит при строго определённой температуре. Количество тепла, необходимое для превращения единицы массы вещества в жидкость при температуре плавления, называют удельной теплотой плавления l. Для плавления вещества массой m необходимо затратить количество теплоты равное: Q = l·m. (5) При охлаждении расплавленного твёрдого тела происходит обратный процесс, называемый кристаллизацией. Образование кристалла также происходит при постоянной температуре, равной температуре плавления. При кристаллизации жидкости выделяется такое же количество теплоты, какое поглощается при плавлении вещества той же массы. Аморфные тела в противоположность кристаллам не имеют определенной температуры плавления. | ||||||

| Испарение и конденсация. Как в жидкостях, так и в твердых телах всегда имеется некоторое число молекул, энергия которых достаточна для преодоления притяжения к другим молекулам и которые способны оторваться от поверхности жидкости или твердого тела и перейти в окружающее их пространство. Этот процесс для жидкости называется испарением (или парообразованием), а для твердых тел - сублимацией (или возгонкой). Количество тепла Q, которое необходимо сообщить жидкости для испарения единицы её массы при постоянной температуре, называется удельной теплотой парообразования r. Количество теплоты, которое надо затратить, чтобы перевести в пар жидкость массой m, Q = r·m. (6) В результате хаотического движения над поверхностью жидкости молекула пара, попадая в сферу действия молекулярных сил, вновь возвращается в жидкость. Этот процесс называется конденсацией. Испарение жидкости происходит при любой температуре и тем быстрее, чем выше температура, больше площадь свободной поверхности испаряющейся жидкости и быстрее удаляются образовавшиеся над жидкостью пары. Следует обратить внимание, что процесс парообразования связан с увеличением внутренней энергии вещества, а процесс конденсации - с уменьшением ее. | ||||||

| Насыщенные и ненасыщенные пары. Влажность. Если за одно и то же время число испаряющихся и конденсирующихся молекул пара одинаково, то число молекул пара над жидкостью будет оставаться постоянным. Такое состояние называют динамическим равновесием пара и жидкости.Пар, находящийся в динамическом равновесии с жидкостью, называют насыщающим (или насыщенным). При неизменной температуре плотность насыщающего пара над жидкостью остается постоянной. Пар, плотность которого меньше плотности насыщающего пара при той же температуре, называют ненасыщающим (или ненасыщенным). Ненасыщенный пар подчиняется законам идеального газа. Частным случаем испарения является кипение.Это процесс интенсивного парообразования не только со свободной поверхности, но и в объеме жидкости. В объеме образуются пузыри, заполненные насыщенным паром. Они поднимаются вверх под действием выталкивающей силы и разрываются на поверхности. Центрами их образования являются мельчайшие пузырьки посторонних газов или частиц различных примесей. | ||||||
Процесс превращения жидкости в пар требует затрат энергии на разрыв связей между молекулами жидкости и на работу против сил внешнего давления. Давление насыщенного пара Pнас внутри пузырька, находящегося у поверхности жидкости, равно сумме внешнего давления на жидкость Рвн и давления под искривленной поверхностью жидкости.
Рнас= Рвн+ 2 s /r, (7)где r - радиус пузырька, s - коэффициент поверхностного натяжения.
Если пузырек имеет размеры порядка нескольких миллиметров и более, то вторым слагаемым можно пренебречь и, следовательно, для больших пузырьков при неизменном внешнем давлении жидкость закипает, когда давление насыщенного пара в пузырьках становится равным внешнему давлению.
Для того чтобы судить, много или мало водяных паров находится в воздухе, вводят понятие влажности. Абсолютная влажность - количество пара, выраженное в килограммах, содержащееся в 1 м3 при данной температуре, т.е. абсолютная влажность равна плотности паров воды. Относительная влажность В - это отношение абсолютной влажности к плотности насыщенного пара при данной температуре.
В =  100%. (8)
Плотность насыщенного водяного пара при данной температуре есть величина табличная. Для определения относительной влажности надо знать абсолютную влажность, которую можно определить по точке росы.
Точке росы соответствует температура, при которой пар, находящийся в воздухе, становится насыщающим. 100%. (8)
Плотность насыщенного водяного пара при данной температуре есть величина табличная. Для определения относительной влажности надо знать абсолютную влажность, которую можно определить по точке росы.
Точке росы соответствует температура, при которой пар, находящийся в воздухе, становится насыщающим.
| |||||||
|
|
|
|
|
|
| Молекулярно-кинетическая теория идеальных газов | ||||||||||||||||||||||
| Тепловое равновесие. Температура. Шкала температур Цельсия. Молекулярная физика и термодинамика изучают свойства и поведение макроскопических систем, т.е. систем, состоящих из огромного числа атомов и молекул. Типичные системы, с которыми мы сталкиваемся в повседневной жизни, содержат около 1025 атомов. При исследовании таких систем важнейшими являются макроскопические величины, непосредственно измеряемые опытным путём и характеризующие свойства всей совокупности молекул в целом. Учитывая необычайную сложность макросистем, следует начать изучение с наиболее простых объектов – систем, состояние которых не меняется со временем. Состояние макроскопической системы, в котором она может находится неопределённо долгое время, называется равновесным (о нём говорят также, как о состоянии теплового равновесия). | ||||||||||||||||||||||

| Равновесное состояние системы в целом может быть описано при помощи величин, называемых макроскопическими параметрами, к числу которых относят давление, объем и т. д. Каждый из параметров характеризует некоторое свойство системы. Так объем V мера свойства системы занимать ту или иную область пространства; давление Р – мера свойства системы сопротивляться внешнему изменению ее объёма. В состоянии теплового равновесия макроскопические параметры не меняются со временем, остаются постоянным. Одним из наиболее важных параметров, характеризующих равновесные свойства макроскопической системы, является температура. Введем этот параметр, для чего рассмотрим два тела, которые могут взаимодействовать и обмениваться энергией. Этот тип взаимодействия, который называется тепловым, приводит к тому, что в результате столкновений молекул в области контакта двух тел происходит передача энергии от быстрых молекул к медленным. Это означает, что энергия движения атомов в одном теле уменьшается, в другом – увеличивается. Тело, которое теряет энергию, называют более нагретым, а тело, к которому энергия переходит – менее нагретым. Такой переход энергии продолжается до тех пор, пока не установится состояние теплового равновесия. В состоянии теплового равновесия степени нагретости тел одинаковы. Для характеристики степени нагретости тела вводят параметр, называемый температурой. Из опыта известно, что при изменении температуры изменяются размеры тел, электрическое сопротивление и другие свойства. Таким образом, температуру можно определить по изменению какого-либо удобного для измерения физического свойства данного вещества. Чаще всего для измерения температур используют свойство жидкости изменять объем при нагревании и охлаждении. Прибор, с помощью которого измеряется температура, называется термометром. | |||||||||||||||||||||
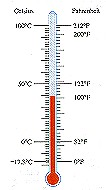
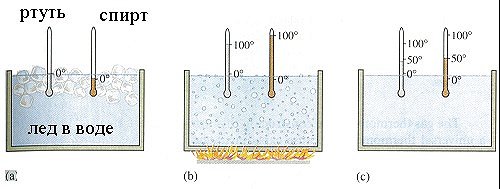
| Обыкновенный жидкостной термометр состоит из небольшого стеклянного резервуара, к которому присоединена стеклянная трубка с узким внутренним каналом. Резервуар и часть трубки наполнены ртутью или другой жидкостью. Температуру среды, в которую погружен термометр, определяют по положению верхнего уровня ртути в трубке. Деления на шкале условились наносить следующим образом. Цифру 0 ставят в том месте шкалы, где устанавливается уровень столбика жидкости, когда термометр опущен в тающий снег, цифру 100 – в том месте, где устанавливается уровень столбика жидкости, когда термометр погружен в пары воды, кипящей при нормальном давлении (105 Па). Расстояние между этими метками делят на 100 равных частей, называемых градусами. Такая температурная шкала создана Цельсием. Градус по шкале Цельсия обозначают °С.
Кроме макроскопических параметров вводят параметры системы, связанные с индивидуальными характеристиками составляющих её частиц, называемые микроскопическими. К их числу относятся в первую очередь масса частиц, их скорость, кинетическая энергия. Идеальный газ. Основное уравнение молекулярно-кинетической теории идеального газа. Теория создана немецким физиком Р. Клаузисом в 1957 году для модели реального газа, которая называется идеальный газ. Основные признаки модели:
Поиск по сайту©2015-2025 poisk-ru.ru
Все права принадлежать их авторам. Данный сайт не претендует на авторства, а предоставляет бесплатное использование. Дата создания страницы: 2017-12-07 Нарушение авторских прав и Нарушение персональных данных |
Поиск по сайту: Читайте также: Деталирование сборочного чертежа Когда производственнику особенно важно наличие гибких производственных мощностей? Собственные движения и пространственные скорости звезд |