g = - 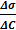 при c → 0
при c → 0
Чем в большей степени уменьшается поверхностное натяжение с увеличением концентрации адсорбируемого вещества, тем больше поверхностная активность этого вещества и наоборот.
Правило Дюкло-Траубе.
В гомологическом ряду жирных кислот с увеличением длины углеводородного радикала на одну -СН2 группу поверхностная активность возрастает в 3 - 3,5 раза
Ориентация молекул ПАВ в поверхностном слое (принцип независимости поверхностного действия Ленгмюра).
Принцип независимости поверхностного действия, заключающийся в том, что при адсорбции полярная группа, обладающая большим сродством к полярной фазе, втягивается в воду, в то время как неполярный радикал выталкивается в неполярную фазу. Образуется мономолекулярный слой:
-малые концентрации ПАВ. При малых концентрациях ПАВ, углеводородные радикалы (R), вытолкнутые в воздух, «плавают» на поверхности воды, затем, по мере роста концентрации ПАВ, они начинают подниматься.
-умеренные концентрации
-насыщенный адсорбционный слой. В насыщенном адсорбционном слое поверхность воды оказывается сплошь покрытой «частоколом Ленгмюра » из вертикально ориентированных молекул ПАВ.
Адсорбция на твёрдых поверхностях. Удельная адсорбция. Факторы определяющие количество поглощённого газа или пара на твёрдом адсорбенте: свободная поверхностная энергия адсорбента, сродство адсорбтива к адсорбенту, концентрация адсорбата и взаимосвязь межмолекулярного взаимодействия в адсорбтиве и величиной адсорбции этого вещества.
Удельная адсорбция Г – это равновесное количество поглощаемого вещества, приходящееся на единицу поверхности или массы твердого адсорбента. Удельная адсорбция для твердых адсорбентов преимущественно выражается в молях поглощенного вещества на единицу массы адсорбента: Г =  где
где
n –количество адсорбата, моль;
m – масса адсорбента, г
Количество поглощенного газа или пара зависит от следующих факторов:
1. От свободной поверхностной энергии адсорбента. Адсорбент тем эффективнее, чем меньше измельчен.
2. От сродства адсобтива к поверхности адсорбента. Полярные вещества лучше адсорбируются на полярных адсорбентах, а неполярные - на неполярных.
3. От природы газа. Лучше адсорбируется тот газ, который легче сжимается.
4. От концентрации адсорбата. Зависимость имеет сложный характер, так как с адсорбцией идет одновременно процесс десорбции. При равенстве скоростей этих процессов наступает равновесие
Теория мономолекулярной адсорбции Ленгмюра. Уравнение Ленгмюра, его анализ.
Теория мономолекулярной адсорбции Ленгмюра:
1)Адсорбция молекул происходит не на всей поверхности адсорбента, а только на адсорбционных центрах, где имеются участки с наиболее нескомпенсированными силовыми полями.
2)Каждый адсорбционный центр может удерживать только одну молекулу адсорбата, при этом адсорбированные молекулы не взаимодействуют со свободными молекулами, что приводит к образованию мономолекулярного слоя поглощаемого вещества;
3)Процесс адсорбции обратим и динамичен, т.к. адсорбированные молекулы удерживаются адсорбционными центрами только в течение определенного промежутка времени, после чего происходит десорбция этих молекул и адсорбция такого же числа новых молекул.
Уравнения Ленгмюра:
Гуд = Г∞ *  где
где
Г∞ - значение предельной адсорбции;
с – равновесная концентрация адсорбента в системе;
К – константа адсорбционного равновесия.
 Г0 – предельная адсорбция
Г0 – предельная адсорбция
1)На 1 участке концентрация маленькая Кс << 1; Гуд = Г∞ * КС
2)На 2 участке концентрация имеет среднее значение Гуд = Г∞ * 
3)На 3 участке концентрация большие Кс >> 1; Гуд = Г∞
Адсорбция на границе твердое тело – жидкость, её особенности. Факторы её определяющие: величина удельной поверхности и сродство адсорбента к адсорбтиву, природа растворителя, природа поглощаемого вещества («подобное взаимодействует с подобным», правило Шилова, правило Ребиндера), влияние концентрации растворённого вещества на процесс адсорбции, влияние температуры. Использование адсорбции из растворов в медицинской практике.
1. При адсорбции из раствора важным фактором является величина удельной поверхности адсорбента и его сродство к поглощаемому веществу. Гидрофильные адсорбенты хорошо поглощают полярные вещества, а гидрофобные - неполярные вещества.
2. Природа растворителя: Чем хуже данный растворитель смачивает поверхность адсорбента и чем хуже растворяет вещество, тем лучше будет происходить адсорбция растворенного вещества.
3. Природа поглощаемого вещества:
а) Выполняется правило «подобное взаимодействует с подобным », т.е. должно быть сродство между адсорбентом и адсорбтивом;
б) правило Шилова: Чем больше растворимость вещества в данном растворителе, тем хуже оно адсорбируется на поверхности твердого адсорбента
в) правило Ребиндера: На поверхности раздела фаз прежде всего адсорбируются те вещества, при адсорбции которых происходит выравнивание полярностей соприкасающихся фаз, причём с увеличением разности полярности фаз способность к адсорбции этих веществ возрастает.
4. Влияние концентрации растворенного вещества на процесс адсорбции при постоянной Т описывается уравнением Ленгмюра
Гуд = Г∞ * 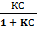
5. Повышение температуры снижает эффективность адсорбции, так как с повышением температуры повышается растворимость.
В медицинской практике. Активированный уголь хорошо адсорбирует газы, алкалоиды, барбитураты, токсины из пищеварительной системы.