Задание
Используя методические рекомендации, решить задачи. Сделать вывод.
Методические рекомендации
Пример 1. Коэффициент молярного поглощения KMnO4 при длине
волны 546 нм равен 2420. Оптическая плотность исследуемого раствора в
кювете толщиной слоя 2 см равна 0.80. Чему равен Т(KMnO4/Mn), г/см3?
Решение. Можно вычислить молярную концентрацию из уравнения:
с(KMnO4) = 0,8 / (2420*2) = 1,65*10–4
T(KMnO4) = с(KMnO4) * M(Mn) / 100 = 1,65*10–4* 55 / 1000 = 9,08*10–6г/см3.
где с (KMnO4) – молярная концентрация раствора, М (Мn) – молярная
масса марганца.
Ответ: 9,08*10–6г/см3.
Пример 2. При фотоколориметрическом определении урана с пероксидом водорода кислотой из стандартного раствора с содержанием урана 10мг/см3 приготовили ряд разведений в мерных колбах вместимостью 100 см3, измерили оптическое поглощение и получили следующие данные:
Vст, см3 1,0 2,0 3,0 4,0 5,0 6,0
А 0,12 0,25 0,37 0,50 0,62 0,75
Определите концентрацию UO22+ в анализируемых растворах, если их оптическое поглощение равно 0,30 и 0,50.
Решение. Строим калибровочный график для стандартного раствора и находим концентрацию при оптическом поглощении 0,30 и 0,50. Она равна 24 и 40 мг/100 см3 соответственно.
Ответ: 24,0 и 40,0 мг/100 см3.
Пример 3. После растворения 0,2500 г стали раствор разбавили до100,0 мл. В три колбы вместимостью 50,0 мл поместили по 25,00 мл этогораствора и добавили: в первую колбу стандартный раствор, содержащий 0,50мг Ti, растворы Н2О2 и Н3РО4, во вторую – растворы Н2О2 и Н3РО4, в третью – раствор Н3РО4 (нулевой раствор). Растворы разбавили до метки и фотометрировали два первых раствора относительно третьего. Получили значения оптической плотности: Ах+ст = 0,650, Ах = 0,250. Рассчитать массовую долю (%) титана в стали.
Решение. Определяем концентрацию титана, добавленного со стандартным раствором: сст = 0,50 / 50,00 = 1,00.10-2 мг/мл,
где 0,50 мг – масса добавленного титана; 50,00 мл – объем раствора.
Вычисляем концентрацию титана по формуле сх = сст Ах / (Ах+ст – Ах);
сх = 1,00·10-2·0,250 / (0,650 – 0,250) = 6,25·10-3 мг/мл.
Определяем массу титана во взятой навеске:
m = (6,25.10-3.50,00.100,0) / 25,00 = 1,25 мг = 1,25. 10 -3 г.
и рассчитываем его массовую долю (%):
wTi = (1,25.10-3.100) / 0,2500 = 0,50%.
Ответ: Массовая доля титана в стали 0,50%.
Пример 4. Вычислите молярную концентрацию и титр раствора рутина (витамина Р), если при 258 нм оптическая плотность анализируемого раствора равна 0,780, а стандартного раствора с концентрацией 6,0·10-5 моль/л – 0,640. М(рутина) = 610 г/моль.
Решение: Молярную концентрацию рутина определяем по формуле для метода одного стандарта:
С(рутина)= 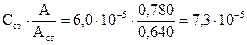 моль/л
моль/л
Определяем титр рутина:
Т(рутина)= 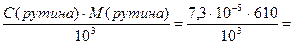 4,46∙10-5 г/мл = 44,6 мкг/мл
4,46∙10-5 г/мл = 44,6 мкг/мл
Ответ: 7,3×10-5 моль/л, 44,6 мкг/мл.
Пример 5. Вычислите молярную концентрацию и титр Cu(II) (в мкг/мл), если оптическая плотность раствора аммиаката меди в кювете с l = 2,00 см составляет 0,282, а молярный коэффициент поглощения 423.
Решение: Определяем молярную концентрацию Cu2+ по значению молярного коэффициента поглощения:
С(Cu2+) = 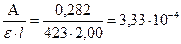 моль/л
моль/л
Определяем титр меди(II):
T(Cu2+) = 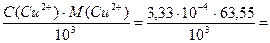 2,12×10-5 г/мл = 21,2 мкг/мл
2,12×10-5 г/мл = 21,2 мкг/мл
Ответ: 3,33×10-4 моль/л, 21,2 мкг/мл.
Пример 6. Чему равна концентрация (в мкг/мл) раствора рибофлавина, если показание флуориметра для исследуемого раствора 0,60, а для стандартного раствора, содержащего 1,0 мкг/мл рибофлавина, - 0,42?
Решение: Определяем концентрацию рибофлавина в анализируемом растворе по формуле для метода одного стандарта:
Т(X) = 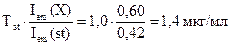
Ответ:1,4 мкг/мл.
Решить задачи:
1. Коэффициент молярного поглощения KMnO4 при длине
волны 546 нм равен 2670. Оптическая плотность исследуемого раствора в
кювете толщиной слоя 1 см равна 0.90. Чему равен Т(KMnO4/Mn), г/см3?
2. При фотоколориметрическом определении урана с пероксидом водорода кислотой из стандартного раствора с содержанием урана 20мг/см3 приготовили ряд разведений в мерных колбах вместимостью 100 см3, измерили оптическое поглощение и получили следующие данные:
Vст, см3 1,0 2,0 3,0 4,0 5,0 6,0
А 0,10 0,20 0,30 0,40 0,60 0,70
Определите концентрацию UO22+ в анализируемых растворах, если их оптическое поглощение равно 0,35 и 0,50.
3. После растворения 0,3600 г стали раствор разбавили до100,0 мл. В три колбы вместимостью 50,0 мл поместили по 25,00 мл этогораствора и добавили: в первую колбу стандартный раствор, содержащий 0,50мг Ti, растворы Н2О2 и Н3РО4, во вторую – растворы Н2О2 и Н3РО4, в третью – раствор Н3РО4 (нулевой раствор). Растворы разбавили до метки и фотометрировали два первых раствора относительно третьего. Получили значения оптической плотности: Ах+ст = 0,750, Ах = 0,350. Рассчитать массовую долю (%) титана в стали.
4. Вычислите молярную концентрацию и титр раствора рутина, если при 258 нм оптическая плотность анализируемого раствора равна 0,880, а стандартного раствора с концентрацией 5,0·10-5 моль/л – 0,540. М(рутина) = 610 г/моль.
5. Вычислите молярную концентрацию и титр Cu(II) (в мкг/мл), если оптическая плотность раствора аммиаката меди в кювете с l = 3,00 см составляет 0,382, а молярный коэффициент поглощения 323.
6. Чему равна концентрация (в мкг/мл) раствора рибофлавина, если показание флуориметра для исследуемого раствора 0,50, а для стандартного раствора, содержащего 1,0 мкг/мл рибофлавина, - 0,52?