ЛИТЕРАТУРА
ВВЕДЕНИЕ
В современных условиях одной из самых актуальных проблем методики преподавания химии в школе становится обеспечение практической ориентированности предметного знания. Это означает необходимость выявления тесной взаимосвязи между изучаемыми теоретическими положениями и практикой жизни, демонстрации прикладного характера химических знаний. Единство теоретического и прикладного материала в процессе преподавания – один из реальных путей реализации специфического требования современной педагогики средней школы о том, чтобы школьник в максимально возможной мере усваивал учебный материал непосредственно в классе.
Актуальность выбранной темы заключается в том, что изучение раздела об электролизе позволяет показать связь теории и практики, дает возможность продемонстрировать применение химической науки, ее законов к практической деятельности человека, рассмотреть проблему охраны окружающей среды, развивать у учащихся интерес к химии, к труду, связанному со знанием химии.
1. ЭТАПЫФОРМИРОВАНИЯ ПОНЯТИЯ «ХИМИЧЕСКАЯ РЕАКЦИЯ»
В силу того, что понятие химическая реакция является достаточно сложным и многогранным, сформировать полное представление обо всех его сторонах, раскрыть всю его философскую сущность невозможно за короткий промежуток времени. Более того, данное понятие формируется на протяжении всего курса обучения химии.
Понятие «химическая реакция» формируется поэтапно [1].
Первый этап (8 класс). На первоначальных этапах изучения химии используется индуктивный подход. В основе изучения, как источник химического познания лежит химический эксперимент. В результате наблюдения за экспериментом учащиеся осознают образования новых веществ в ходе протекания химической реакции. Но в экспериментальном изучении реакций не уделяется внимания ее сущности, акцент делается на внешние проявления (изменение окраски раствора, выделение газа, выпадение осадка).
Понятие о химической реакции начинает формироваться с самых первых уроков. Сначала дают понятие о явлениях, происходящих в природе, повседневной жизни, быту, разграничивая явления на физические и химические. А затем сообщают учащимся о тождественности понятий «химическое явление» и «химическая реакция». На уровне атомно-молекулярного учения разъясняют, как можно по внешним признакам обнаружить протекание химической реакции.
Классификация химических реакций дается на уровне сравнения числа исходных и полученных веществ. При этом учащиеся используют такие мыслительные приемы как сравнение, анализ, синтез, обобщение. Все эти сведения включены в раздел «Первоначальные химические понятия». Далее все стороны системы понятий о химической реакции должны расширяться и дополняться новыми данными, т. е начинается этап накопления. Закономерности протекания химической реакции разбираются на простейших примерах: так влияние температуры рассматривается на реакции образования сульфида железа, реакции окисления рассматриваются как процесс соединения вещества с кислородом, понятие о реакциях обмена на примере взаимодействия кислот с оксидами и т.д.
На втором этапе (8 класс) понятие о химической реакции получает дальнейшее развитие. Начинают формироваться энергетические представления о химических реакциях. Рассматривается понятие об экзо- и эндотермических реакциях, вводится новое понятие о тепловом эффекте химической реакции, термохимических уравнениях и их составлении. При изучении энергетических эффектов появляется возможность показать не только качественную, но и количественную сторону химической реакции. Количественные отношения веществ, вступивших в реакцию, трактуются как молярные отношения реагирующих веществ.
На третьем этапе (8 класс) формирования понятие «химическая реакция» претерпевает качественные изменения в теме «Химическая связь. Строение вещества». В данной теме химическая реакция начинает трактоваться как разрушение одних связей и образование других. Рассматривается это на примере окислительно-восстановительных реакций. Механизм этих реакций объясняют с точки зрения перехода электронов, поднимаясь тем самым на более высокий теоретический уровень.
На основе нового понятия «степень окисления» анализируют известные учащимся реакции разных типов, доказывая тем самым, что среди реакций любого типа можно найти окислительно-восстановительные.
В теме «Подгруппа кислорода» вводится новое понятие аллотропия и соответствующие ей новый тип реакций - аллотропные превращения.
Четвертый этап (9 класс). В разделе «Закономерности химической реакции» вводится понятие о скорости химической реакции и о влияющих на нее факторах (температура, концентрация, поверхность соприкосновения). Здесь же рассматривается вопрос об обратимости химической реакции и о химическом равновесии. Необходимо подчеркнуть динамический характер химического равновесия, факторы, вызывающие смещение химического равновесия. Таким образом, учащиеся знакомятся еще с одним типом химической реакции — обратимыми.
Этап пятый. На данном этапе происходит знакомство учащихся с такой важной темой как «электролиз растворов и расплавов». Она помимо мировоззренческого значения (иллюстрация единства и борьбы противоположностей – моляризации и диссоциации) вносит много нового в объяснение механизма реакций. Далее изучение химической реакции происходит дедуктивно. Знания, сформированные на базе перечисленных теорий, применяются для объяснения фактов и явлений и прогнозирования протекания процессов.
Этап шестой (9 – 10 классы). Дальнейшие развитие понятия о химической реакции осуществляется в курсе органической химии. Дополняются понятия о классификации химических реакций, вводятся новые типы реакций, например реакции изомеризации, полимеризации, этерификации и др. В органике вводится качественно новый материал и в понятие о механизмах реакций. Так, например, рассматривается свободнорадикальный механизм на примере реакций замещения (галогенирование алканов), присоединения (полимеризация), отщепления (крекинг). Расширяется понятие об ионном механизме химической реакции: приводятся примеры присоединения неорганических соединений к алкенам, реакций замещения при гидролизе галогеналканов.
Дополняется также система понятий о закономерностях протекания химических реакций. При развитии понятия «скорость химической реакции» отмечается влияние энергии связи и ее типа. Знания о катализе и катализаторах дополняются в органике знаниями о ферментах.
Этап седьмой (11 класс). На завершающем этапе обучения подводятся итоги, обобщаются знания о химических реакциях. В конце обучения учащиеся должны суметь охарактеризовать предложенную им в качестве примера химическую реакцию в свете компонентов ее содержания.
Формирование знаний о типах химических реакций
Изучение атомно-молекулярного учения и первоначальных химических понятий, а также некоторое накопление фактов позволяет более осмысленно подойти к классификации реакций.
Первое ознакомление с классификацией веществ показывает, что в ее основу положен их состав и свойства: вещества делятся на простые и сложные (по составу), а простые вещества на металлы и неметаллы (по свойствам).
Таким образом, всякая классификация явлений, предметов, веществ связана с выбором каких то существенных признаков, которые можно положить в основу деления предметов или явлений на группы [2].
Можно ли классифицировать химические реакции? Что положить в основу их классификации?
Сущность всякой химической реакции состоит в изменении состава молекул веществ, взятых для реакции. Поэтому характер этих изменений и нужно положить основу классификации химических реакций. После разъяснения поставленной перед учащимися проблемы можно предложить назвать известные им реакции и написать на доске уравнения этих реакций.
| Fe + S= FeS Cu + O2 =CuO | Mg + O2 = MgO H2O= H2 + O2 |
После написания уравнений учитель совместно с учащимися выясняет, какие из них сходны по характеру изменения состава молекул.
В одних случаях из молекул одного вещества получается 2 молекулы других веществ – это реакции разложения, в других, наоборот, из молекул двух веществ образуется одна молекула нового вещества – это реакции соединения. Учитель совместно с учащимися, анализируя данные выводы, выясняет, всегда ли из молекул одного сложного вещества образуются молекулы простого вещества. Для ответа на данный вопрос учитель проводит реакцию разложения, например малахита или перманганата калия.
Таким образом, учащиеся осознают, что в ходе разложения сложных веществ могут образоваться как сложные, так и простые вещества (либо их смесь). В заключении учащиеся зарисовывают схему данного опыта, делают необходимые пометки к чертежу и записывают уравнения реакции.
Далее при формировании у учащихся понятия о типах реакций, учитель вновь выдвигает проблему: могут ли во время протекания химической реакции происходить какие-либо другие перегруппировки атомов кроме тех, которые происходят при химических реакциях присоединения и разложения?
Для ответа на этот вопрос учитель демонстрирует ученикам опыт между раствором CuCl2 и железом (железным гвоздем). В ходе процесса железный гвоздь покрывается налетом меди. Учитель задает вопрос: можно ли данную реакцию отнести к реакциям соединения или разложения? Для ответа на этот вопрос учитель записывает на доске уравнение реакции (связывая тем самым модель процесса с реальным, только что проведенным опытом) и поясняет, что ни к тому, ни к другому типу данную реакцию отнести нельзя, поскольку в ходе процесса из молекул двух веществ образуется также две молекулы новых веществ. А значит, есть основание выделить еще один тип реакции. Это третий тип химической реакции, который называется замещением (вытеснением). Необходимо подчеркнуть, что в реакцию замещения вступает одно простое и одно сложное вещество.
В завершении урока учащиеся выполняют ряд упражнений по данной теме, приобретая и закрепляя тем самым навыки работы с новым материалом. Кроме того, по данной теме учащимся задается задание на дом.
Как видно из вышеперечисленного, в ходе урока учитель при объяснении данного материала использует методы беседы, рассказа, объяснения. Благодаря наводящим вопросам, учащиеся включаются в мыслительный процесс. Здесь рационально использовать наглядность, в качестве которой ведущую роль отводят химическому эксперименту. Важно провести связь типов реакций с процессами, происходящими в жизни (например, процесс выделения меди на железном гвозде свидетельствует о его разрушении, данный процесс разрушения металла присутствует повсеместно). Самой трудной темой в курсе химии средней школя является «Электролиз растворов и расплавов», рассмотрим ее методические особенности.
2. СОСТОЯНИЕ ИЗУЧАЕМОГО ВОПРОСА В СОВРЕМЕННОЙ РОССИЙСКОЙ ШКОЛЕ
2.1 Содержание и последовательность изложения
Тема «Электролиз растворов и расплавов» логически продолжает изучение закономерностей протекания химических реакций, смещения равновесия обратимых процессов и является одним из существенных вопросов теории растворов. Многие вопросы промышленности, металлургии связаны с явлением гидролиза солей, поскольку он является основой их устойчивости и равновесия.
Преподавание темы «Электролиз растворов и расплавов» начинается с 9 класса, первого полугодия. При изучении этой темы пользуются учебником химии под редакцией Г. Е. Рудзитис, Ф.Г. Фельдман, также учебником за 8 - 9 класс под редакцией Н. С. Ахметова. Дидактическим материалом служит книга по химии для 8 - 9 классов под редакцией А. М. Радецкого, В. П. Горшкова; используются задания для самостоятельной роботы по химии за 9 класс под редакцией Р. П. Суровцева, С. В. Софронова; используется сборник задач по химии для средней школы и для поступающих в вузы под редакцией Г. П. Хомченко, И. Г. Хомченко. В 9 классе на изучение данной темы отводится 4 ч [1].
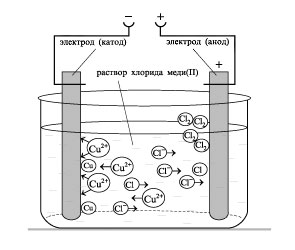
Электролиз растворов
Электролизом называется окислительно-восстановительный процесс, протекающий на электродах при пропускании через электролит электрического тока. При электролизе катод является восстановителем, т. к. отдает электроны, а анод – окислителем, т. к. принимает электроны от анионов.