В предварительно подготовленных горючих смесях скорость распространения пламени во многом определяется скоростью протекания химических реакций, иными словами - кинетикой химических реакций. Такие пламена называются кинетическими.
Процесс окисления топлив происходит через ряд простых химических реакций, включающих в себя реакции разложения топлив, возникновения химически активных радикалов, протекания большого количества прямых и обратных химических реакций с образованием промежуточных продуктов, которые в результате протекания последующих реакций превращаются в конечные продукты горения. На сегодняшний день известно более трехсот химических реакций, сопровождающих процесс горения углеводородных топлив, с их кинетическими характеристиками. Расчет скорости горения на базе всего перечня химических реакций затруднителен и не дает высокой точности результатов.
Возможно описание химических реакций окисления топлив без детализации химического механизма, а представив окисление в виде одной суммарной химической реакции с суммарными (эффективными) кинетическими характеристиками. Такая модель не претендует на высокую точность, но позволяет выявить основные факторы, влияющие на скорость протекания химических реакций. Модель может быть описана формулой Аррениуса в предположении, что скорость химической реакции определяется скоростью образования одного из конечных продуктов горения x и обозначается как Wx c размерностью, например кмоль/м3 с. Выражение имеет вид:
Wx = dcx /dt = K0 c тn c о m exp(- E а /RT), где
Wx – скорость химической реакции, кмоль/м3 с;
K0 – предэкспоненциальный множитель. 1/с;
c т , c о и cx – концентрации топлива, окислителя и конечного продукта, кмоль/м3;
n и m – эффективные показатели порядка реакций;
E а – эффективная энергия активации, МДж/кмоль;
R – газовая постоянная, МДж/кмоль К;
T – температура, К;
t – время, с.
Энергия активации указывает, какой минимальной энергией должны обладать соударяющиеся частицы, для того чтобы произошла химическая реакция. По смыслу множитель exp(- E а /RT) характеризует долю молекул (частиц), обладающей энергией большей, чем E а при температуре T. Произведение K0 exp(- E а /RT) называют константой скорости химической реакции. Кинетические характеристики суммарных реакций определяются экспериментально, они справедливы лишь для диапазона температур, при которых были определены.
Анализ приведенного выше выражения позволяет выявить наиболее значимые факторы, влияющие на скорость химических процессов при горении.
Протекание химических реакций с заметной скоростью и заметным энерговыделением возможно только при температурах, обеспечивающих энергию частиц смеси не ниже эффективной энергии активации E а. Увеличение температуры значительно увеличивает скорость химической реакции, в соответствии с экспонентой.
С ростом концентрации реагирующих веществ скорость химической реакции возрастает, существует такое соотношение концентраций (в условиях ДВС это коэффициент избытка воздуха), при которой скорость реакции в данных условиях максимальна.
Наличие в горючей смеси инертных, не участвующих в химических реакциях компонентов (например, остаточных газов), снижает скорость горения.
Рост давления, при котором протекает химическая реакция, увеличивает ее скорость в связи с ростом концентрации реагирующих веществ, т.е. количества частиц в единице объема.
Совместное влияние температуры и давления при распространении пламени в замкнутом объеме (например, при сгорании в цилиндре) приводит к росту скорости реакции в связи с ростом давления и температуры среды в период сгорания. Рост давления предопределяется тем, что коэффициент молекулярного изменения свежей смеси обычно больше единицы и, в значительной мере, нагревом среды в результате тепловыделения и адиабатического сжатия несгоревшей части смеси.
Процесс горения является самоподдерживающимся процессом Это связано с тем, что при горении протекают не только химические процессы, но и процессы переноса тепла и частиц из сгоревшей части в свежую смесь. В результате переноса горючая смесь, примыкающая к продуктам сгорания, нагревается до температур, при которых начинают протекать реакции окисления, выделяется тепло, которое затрачивается на нагрев продуктов сгорания и передачи тепла последующим слоям свежей смеси. В гомогенных смесях поверхность горения, отделяющая исходную смесь от продуктов сгорания, называют фронтом пламени.

В неподвижной среде в зависимости от способа воспламенения фронт пламени распространяется в виде сферических или плоских поверхностей со скоростью uн, которая называется нормальной скоростью горения. Толщина фронта пламени δфп для условий сходных с условиями в цилиндре ДВС составляет десятые доли миллиметра. Структурно фронт пламени состоит из зоны подогрева толщиной δпод и зоны горения – δг.
В зоне подогрева вследствие переноса тепла и нагретых частиц происходит нагрев исходной смеси и протекает часть предпламенных химических реакций, многие из них являются эндотермическими. В результате возникают химически активные радикалы, способные вступать в реакции окисления с высоким экзотермическим эффектом.
В зоне горения протекает основная часть экзотермических химических реакций.
Т.о. можно констатировать, что скорость распространения фронта пламени зависит от скорости протекания теплофизических и физико-химических процессов в его объеме.
Теплофизические свойства среды с точки зрения процессов переноса определяются коэффициентами теплопроводности, температуропроводности, диффузии, которые не зависят от условий, при которых протекает сгорание. К тому же в условиях ДВС свежая смесь состоит в основном из воздуха и небольшого количества паров топлива, т.е. является средой с неизменными теплофизическими свойствами.
Напротив, физико-химические свойства – скорость протекания химических процессов – существенно зависят от условий осуществления сгорания: давления, температуры, концентраций и т.д. Поэтому можно считать, что влияние на скорость сгорания внешних и начальных условий происходит именно через воздействие на кинетику химических реакций. Рассмотрим влияние различных факторов на скорость распространения пламени.
Температура горения T г в соответствии с формулой Аррениуса сильно влияет на скорость химических реакций и на u н в сторону их увеличения. Кроме того, при неизменной начальной температуре горючей смеси с ростом T г возрастает перепад температур между свежей смесью и продуктами сгорания, что ведет к росту скорости передачи тепла в зону подогрева и ускорению протекания подготовительных процессов и скорости сгорания в целом.
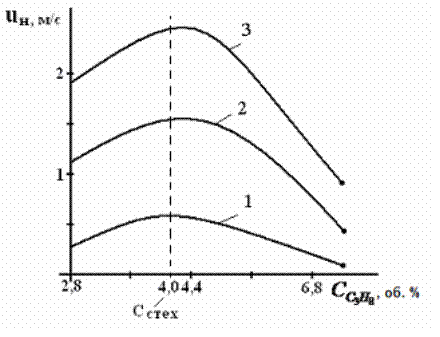
Скорость фронта пламени в зависимости от концентрации пропана в воздухе и начальной температуры 1 – 311К, 2 – 644 К, 3 – 811 К
С ростом начальной температуры T 0 скорость распространения пламени также увеличивается, однако, это влияние существенно слабее.
Концентрация реагирующих веществ
Давление
Соотношение концентраций реагирующих веществ (α, T г)
Остаточные газы
Температура
Рассмотреть гашение в узких каналах
Приведенные выше закономерности характерны для распространения фронта пламени в неподвижной среде – ламинарного пламени. Скорость ламинарного пламени для смесей углеводородных топлив с воздухом составляет в зависимости от различных факторов 5 – 20 см/с. При сжигании топлив в энергетических машинах ламинарный режим горения не реализуется никогда. В среде всегда присутствуют турбулентные пульсации различного происхождения. Фронт пламени, распространяющийся в турбулизированной среде, называется турбулентным пламенем.

Скорость распространения турбулентного пламени значительно выше и составляет 15 – 80 м/с. Ускорение процесса сгорания в турбулентной среде объясняют увеличением площади фронта пламени при его искривлениях при воздействии мелкомасштабной турбулентности. При наличии крупномасштабной турбулентности возможен заброс конечных объемов продуктов сгорания в зону свежего заряда и образование там дополнительных очагов воспламенения, дополнительно увеличивающих скорость горения. При этом линейная скорость перемещения фронта пламени соответствует ламинарному пламени, а массовая скорость выгорания смеси в кмоль/с или кг/с растет за счет увеличения площади фронта. Т.о. при турбулентном сгорании имеется в виду эффективная скорость распространения пламени. Поэтому, влияние рассмотренных выше факторов, влияющих на скорость распространения пламени, сохраняется и для турбулентного пламени, но возникает еще один фактор – уровень турбулизации свежего заряда.
Рассматривают два уровня турбулизации: мелкомасштабная, уровень которой соизмерим с толщиной фронта пламени, и крупномасштабная, возникновение которой связано с вихреобразованием при наполнении цилиндра и сжатии. Крупномасштабная турбулентность в большей мере ускоряет выгорание горючей смеси, чем мелкомасштабная.