I. Эвтектические сплавы
При кристаллизации плохо растворимых друг в друге веществ образуется смесь мелкозернистых кристаллов индивидуальных компонентов которая называется эвтектической смесью или просто эвтектикой (эвтектика – греч. ''легкоплавкий'').
Такое взаимодействие протекает при сплавлении химически индифферентных металлов (размеры атомов которых отличаются более чем на 15%), которые существенно отличаются друг от друга по типу кристаллической решетки.
|
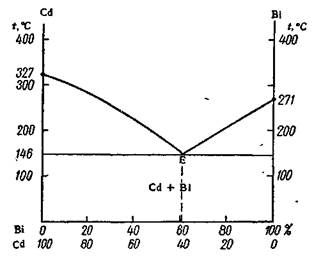
Рисунок 3. Диаграмма плавкости системы с образованием простой эвтектики (кадмий – висмут).
Рассмотрим диаграмму плавкости системы с образованием простой эвтектики (рис.3). Возможные фазовые состояния в системе:
I область: гомогенная система жидкого раствора (Cd + Вi).
Ф = 1, С = 2 + 1 – 1 = 2
II и III области: из общего раствора (Cd + Вi) могут выпадать кристаллы либо Cd, либоBi, в зависимости от состава.
Ф = 2, С = 2 + 1 –2= 1
IV область: из общего раствора одновременно выпадают кристаллы Cd и Bi
Ф = 3, С = 2 + 1 – 3 = 0
Эта система существует при строго определенных значениях температуры и концентрации. При этом создаются условия сплошной кристаллизации, называемой эвтектикой. В
V и VI области: образуется твердый раствор, состоящий из крупных кристаллов чистых металлов (Cd или Вi), спаянных между собой мелкими кристаллами эвтектики.
В данном случае говорят, что твердые сплавы содержат по две структурные составляющие:
1) Первичную (вкрапленную), представляющую собой кристаллы того чистого металла, которого в составе конкретного сплава больше, чем в составе эвтектики;
2) Вторичную (матричную), представляющую собой эвтектическую смесь мелких кристаллов обоих металлов.
Ф = 2, С = 2 + 1 – 2 = 1
Эвтектические сплавы характеризуются малыми размерами и однородностью кристаллов, имеют высокие твердость и механическую прочность. Поэтому, например, сплавы свинца с оловом и сурьмой применяются в качестве типографских шрифтов и решеток аккумуляторов. Вследствие легкоплавкости сплавы свинца с оловом также применяются для припоев и подшипников.
II. Твердые растворы.
Сплав представляет собой однородную фазу переменного состава, в которых различные атомы образуют общую кристаллическую решетку называемую твердым раствором.
Твердый раствор образуется, если атомы смешиваемых металлов могут замещать друг друга в кристаллической решетке, не нарушая ее структуры. Благодаря такой замене получаются совершенно однородные смешанные кристаллы, содержащие одновременно атомы обоих металлов и обуславливающие полную однородность сплава.
Металлы могут образовывать жидкие растворы неограниченной концентрации. При охлаждении из этого раствора выпадают кристаллы чистых компонентов, и их смесь создает затвердевший сплав.
Сплавы такого типа отличаются высокой однородностью (это гомогенные сплавы) и постепенным изменением физических свойств с изменением состава. Прочность и твердость твердых растворов обычно выше, а электрическая проводимость и теплопроводность ниже, чем у каждого из компонентов в отдельности.
Примером могут служить твердые растворы: СuNi; AgAu
Рассмотрим диаграмму плавкости системы с образование непрерывных твердых растворов (рис.4).

|
Вид кривых плавления (нижняя кривая) и кристаллизации (верхняя кривая) обусловлен тем, что выделяющиеся при охлаждении расплава кристаллы содержат оба компонента.
Рисунок 4. Диаграмма плавкости системы с образованием непрерывных твердых растворов (никель – медь).
Возможные фазовые состояния в системе:
I область (выше линии ликвидус): гомогенная система расплава Ni–Cu.
Ф = 1 C = 2 + 1 – 1 = 2
II область (между линиями ликвидус и солидус): расплав и кристаллы твердого раствора
Ф = 2, C = 2 + 1 – 2 = 1
III область (ниже линии солидус): твердый раствор.
Ф = 2, C = 2 + 1 – 2 = 1.
III. Сплавы с образованием интерметаллических соединений
При больших силах взаимодействия между атомами в жидком растворе компонентов возможно образование устойчивых интерметаллидов, которые могут рассматриваться как новые компоненты сплава. Данные сплавы неоднородны, состоят из кристаллов отдельных металлов, смешанных с кристаллами химических соединений металлов. На диаграмме появляются как максимумы, которые отвечают образованию химических соединений, так и минимумы, обусловленные образованием эвтектики.
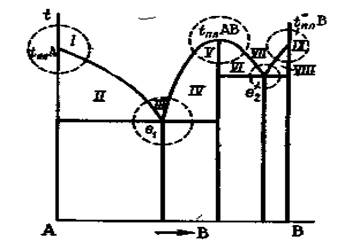
Рассмотрим диаграмму плавкости системы с образованием химического соединения (рис. 5).
|
Рисунок 5. Диаграмма плавкости системы с образованием химического соединения.
Возможные фазовые состояния в системе:
I область: кристаллизации вещества А при температуре плавления.
С = 1 + 1 - 2 = 0
II область: кристаллизация вещества А из жидкого раствора А + АВ
С = 2 + 1 - 2 = 1
III область: эвтектическое состояние: (тв.А; тв.АВ; жидкий раствор А + АВ)
С = 2 + 1 - 3 = 0
IV область: кристаллизации АВ из жидкого раствора А + АВ
С = 2 + 1 - 2 = 1
V область: кристаллизация АВ при температуре плавления АВ:
С = 1 + 1 - 2 = 0
VI область: кристаллизация АВ из жидкого раствора В + АВ:
С = 2 + 1 - 2 = 1
VII область: эвтектическое состояние (тв.В, тв.АВ, жидкий раствор В + АВ):
С = 2 + 1 - 3 = 0
VIII область: кристаллизация вещества В из жидкого раствора В + АВ:
С = 2+ 1 - 2 = 1
IX область: кристаллизация вещества В при температуре плавления.
С = 1 + 1 - 2 = 1
Кристаллические структуры интерметаллидов, как правило, непохожи на структуры индивидуальных компонентов. Свойства химических соединений существенно отличаются от свойств исходных металлов. Они характеризуются меньшими значениями теплопроводности и электрической проводимости, чем образующие их компоненты. Некоторые интерметаллиды являются даже полупроводниками. Интерметаллиды характеризуются хрупкостью, но становятся пластичными при температурах, близких к температурам плавления. Многие из них имеют высокую химическую стойкость.
Реальные диаграммы плавкости, используемые для выбора промышленных сплавов, гораздо сложнее и представляют собой сочетание рассмотренных нами диаграмм плавкости.
Свойства сплавов значительно отличаются от свойств чистых металлов. Например, железо хорошо растворимо, а его сплав с хромом и никелем (нержавеющая сталь) – устойчив в разбавленной серной кислоте.
Температура плавления сплавов очень часто бывает ниже температуры плавления наиболее легкоплавкой составной части сплава. Например, сплав, состоящий из свинца (4части), олова (2части), висмута (6частей) и кадмия (1часть), плавится около 750С, а температура плавления самого легкоплавкого из четырех названных металлов – олова – равна 2320С.
Наоборот, твердость сплавов обычно больше твердости их составных частей, особенно если при сплавлении образуются химические соединения. Очень большой твердостью обладают сплавы, содержащие твердые растворы.
Все эти свойства часто делают сплавы более ценным материалом, чем те металлы, из которых они состоят. Поэтому в промышленности металлы большей частью используются в виде различных сплавов.