Допускает ли первый закон термодинамики самопроизвольный переход тепла от менее нагретого тела к более нагретому? Наблюдаются ли такие процессы в природе? Мы уже отмечали, что первый закон термодинамики — это частный случай закона сохранения энергии. Закон сохранения энергии утверждает, что количество энергии при любых её превращениях остаётся неизменным. Между тем многие процессы, вполне допустимые с точки зрения закона сохранения энергии, никогда не протекают в действительности. Например, с точки зрения первого закона термодинамики в изолированной системе возможен переход тепла от менее нагретого тела к более нагретому, если количество теплоты, полученной горячим телом, точно равно количеству теплоты, отданной холодным телом. В то же время наш опыт подсказывает, что это невозможно. Первый закон термодинамики не указывает направление процессов. Второй закон термодинамики. Второй закон термодинамики указывает направление возможных энергетических превращений, т. е. направление процессов, и тем самым выражает необратимость процессов в природе. Этот закон был установлен путём непосредственного обобщения опытных фактов. Есть несколько формулировок второго закона, которые, несмотря на внешнее различие, выражают, в сущности, одно и то же и поэтому равноценны. Немецкий учёный Р. Клаузиус (1822—1888) сформулировал этот закон так: Невозможно перевести тепло от более холодной системы к более горячей при отсутствии других одновременных изменений в обеих системах или в окружающих телах. Здесь констатируется опытный факт определённой направленности теплопередачи: тепло само собой переходит всегда от горячих тел к холодным. Правда, в холодильных установках осуществляется теплопередача от холодного тела к более тёплому, но эта передача связана с другими изменениями в окружающих телах: охлаждение достигается за счёт работы. Важность этого закона в том, что из него можно вывести заключение о необратимости не только процесса теплопередачи, но и других процессов в природе. Рассмотрим пример. Колебания маятника, выведенного из положения равновесия, затухают (рис. 13.12) 1, 2, 3, 4 — последовательные положения маятника при максимальных отклонениях от положения равновесия).
|
|
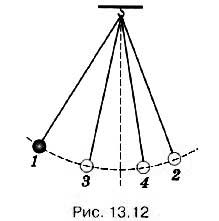
За счёт работы сил трения механическая энергия маятника убывает, а температура маятника и окружающего воздуха (а значит, и их внутренняя энергия) слегка повышается. Можно вновь увеличить размах колебаний маятника, подтолкнув его рукой. Но это увеличение возникает не само собой, а становится возможным в результате более сложного процесса, включающего движение руки. Механическая энергия самопроизвольно переходит во внутреннюю, но не наоборот. При этом энергия упорядоченного движения тела как целого превращается в энергию неупорядоченного теплового движения составляющих его молекул. Ещё один пример — процесс диффузии. Открыв пузырёк с духами, мы быстро почувствуем запах духов. Молекулы ароматического вещества благодаря тепловому движению проникают в пространство между молекулами воздуха. Трудно представить, чтобы все они вновь собрались в пузырьке. Число подобных примеров можно увеличивать практически неограниченно. Все они говорят о том, что процессы в природе имеют определённую направленность, никак не отражённую в первом законе термодинамики. Все макроскопические процессы в природе протекают только в одном определенном направлении. В обратном направлении они самопроизвольно протекать не могут. Все процессы в природе необратимы. Раньше при рассмотрении процессов мы предполагали, что они являются обратимыми. Обратимый процесс — это процесс, который можно провести в прямом и обратном направлениях через одни и те же промежуточные состояния без изменений в окружающих телах. Обратимый процесс должен протекать очень медленно, чтобы каждое промежуточное состояние было равновесным. Равновесное состояние — это состояние, при котором температура и давление во всех точках системы одинаковы. Следовательно, чтобы система пришла в равновесное состояние, необходимо время. При изучении изопроцессов мы предполагали, что переход из начального состояния в конечное проходит через равновесные состояния, и считали изотермический, изобарный и изохорный процессы обратимыми. Идеальных обратимых процессов в природе не существует, однако реальные процессы можно с определённой степенью точности рассматривать как обратимые, что является очень важным для теории. Яркой иллюстрацией необратимости явлений в природе служит просмотр кинофильма в обратном направлении. Например, прыжок в воду будет при этом выглядеть следующим образом. Спокойная вода в бассейне начинает бурлить, появляются ноги, стремительно движущиеся вверх, а затем и весь ныряльщик. Поверхность воды быстро успокаивается. Постепенно скорость ныряльщика уменьшается, и вот уже он спокойно стоит на вышке. Такой процесс, как вознесение ныряльщика на вышку из воды, не противоречит ни закону сохранения энергии, ни законам механики, ни вообще каким-либо законам, кроме второго закона термодинамики.
|
|