Тема урока: «Ионные уравнения»
Цель: сформировать представление учащихся о реакциях, протекающих межу ионами, условий протекания реакций ионного обмена до конца, обратимых реакциях, полных и сокращенных ионных уравнениях.
Задачи:
· способствовать систематизации понятийного аппарата: ион, растворы, электролиты и неэлектролиты, основные типы реакций в неорганической химии, обратимые реакции, условия протекания реакций ионного обмена до конца
o “ 5 ” - обосновать, доказать;
o “ 4 ” - характеризовать, применить;
o “ 3 ” - рассказать;
· способствовать совершенствованию специальных предметных умений: составлять полные и сокращенные ионные уравнения;
· способствовать формированию общеучебных умений:
o а) учебно-интеллектуальных (анализировать факты, устанавливать причинно-следственные связи; выдвигать гипотезу; сравнивать соли и химические реакции, классифицировать, делать выводы);
o б) учебно-информационных (работать с текстом);
o в) учебно–организационных (понимать смысл задания, распределять время для выполнения заданий планировать работу по организации работы, осуществлять самоконтроль);
· способствовать формированию критического мышления учащихся (критически оценивать собственные знания по теме и сопоставлять их с научными);
Изучение нового материала
Реакции обмена протекают между ионами, поэтому называются реакции ионного обмена.
Реакции ионного обмена идут до конца в трех случаях:
· если образуется осадок – нерастворимое вещество после реакции)
· если выделяется газ
· если образуется вода
В остальных случаях реакции обмена являются обратимыми
Разберем эти случаи поподробнее
1) Если образуется осадок:
а) CuSO4 + 2NaOH 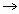 Na2SO4 + Cu(OH)2
Na2SO4 + Cu(OH)2 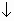
б) 2AgNO3 + CaCl2 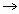 Ca(NO3)2 + 2AgCl
Ca(NO3)2 + 2AgCl 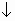
в) Na2CO3 + Ca(NO3)2 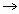 2NaNO3 + CaCO3
2NaNO3 + CaCO3 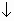
г) BaCl2 + K2SO4 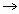 2KCl + BaSO4
2KCl + BaSO4 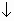
2) Если выделяется газ:
а) CaCO3 + 2HNO3  Ca(NO3)2 + H2CO3 (H2O + CO2
Ca(NO3)2 + H2CO3 (H2O + CO2  )
)
б) Na2SO3 + 2HCl  2NaCl + H2SO3 (H2O + SO2
2NaCl + H2SO3 (H2O + SO2  )
)
в) CuS + 2HCl 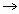 CuCl2 + H2S
CuCl2 + H2S 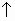
3) Если образуется вода:
а) CuO + H2SO4 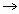 CuSO4 + H2O
CuSO4 + H2O
б) Fe(OH)3 + 3HCl 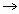 FeCl3 + 3H2O
FeCl3 + 3H2O
в) NaOH + HNO3 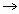 NaNO3 + H2O
NaNO3 + H2O
4) Если НЕ образуются осадок, газ и вода, то реакции являются обратимыми:
Обратимые реакции – это реакции, которые при одних и тех же условиях протекают в двух противоположных направлениях
а) 2NaNO3 + CaCl2  Ca(NO3)2 + 2NaCl
Ca(NO3)2 + 2NaCl
б) K3PO4 + 3NaCl  Na3PO4 + 3KCl
Na3PO4 + 3KCl
в) CuCl2 + Na2SO4  CuSO4 + 2NaCl
CuSO4 + 2NaCl
Ионные уравнения:
Для реакций ионного обмена составляют полные и сокращенные ионные уравнения. При этом на ионы никогда не раскладывают:
· нерастворимые вещества (см. таблицу растворимости);
· оксиды;
· воду;
· газы
1) Запишем молекулярное уравнение и уравняем его:
CuSO4 + 2NaOH 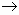 Na2SO4 + Cu(OH)2
Na2SO4 + Cu(OH)2 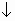
2) Разложим на ионы все, что возможно и затем сократим одинаковые ионы в обоих частях уравнения:
Cu+2 + SO4-2 + 2Na+1 + 2OH-1 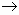 2Na+1 + SO4-2 + Cu(OH)2
2Na+1 + SO4-2 + Cu(OH)2 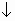 (полное ионное уравнение)
(полное ионное уравнение)
3) Запишем то, что получилось:
Cu+2 + 2OH-1 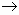 Cu(OH)2
Cu(OH)2 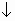 (сокращенное ионное уравнение)
(сокращенное ионное уравнение)
Другие примеры составления ионных уравнений (разбираются с пояснениями):
Пример 2.
CaCO3 + 2HNO3 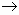 Ca(NO3)2 + H2CO3 (H2O + CO2
Ca(NO3)2 + H2CO3 (H2O + CO2 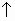 )
)
CaCO3 + 2H+1 + 2NO3-1 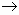 Ca+2 + 2NO3-1 + H2O + CO2
Ca+2 + 2NO3-1 + H2O + CO2 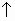
CaCO3 + 2H+1 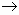 Ca+2 + H2O + CO2
Ca+2 + H2O + CO2 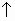
Пример 3.
CuS + 2HCl 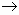 CuCl2 + H2S
CuCl2 + H2S 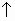
CuS + 2H+1 + 2Cl-1 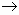 Cu+2 + 2Cl-1 + H2S
Cu+2 + 2Cl-1 + H2S 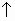
CuS + 2H+1 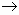 Cu+2 + H2S
Cu+2 + H2S 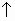
Пример 4.
NaOH + HNO3 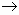 NaNO3 + H2O
NaNO3 + H2O
Na+1 + OH-1 + H+1 + NO3-1 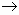 Na+1 + NO3-1 + H2O
Na+1 + NO3-1 + H2O
OH-1 + H+1 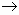 H2O
H2O
Пример 5.
K3PO4 + 3NaCl 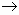 Na3PO4 + 3KCl
Na3PO4 + 3KCl
3K+1 + PO4-3 + 3Na+1 + 3Cl-1 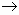 3Na+1 + PO4-3 + 3K+1 + 3Cl-1
3Na+1 + PO4-3 + 3K+1 + 3Cl-1
Вывод: сокращенного ионного уравнения нет, следовательно, у обратимых реакций нет сокращенных ионных уравнений
III. Закрепление изученного материала (20 мин)
Учащимся предлагается выполнить следующие задания.
Задание 1
Саша и Алеша делали домашнее задание. Они составили уравнения реакций, нослучайно на лист бумаги пролили чернила. Помогите ученикам восстановить запись. Составьте к восстановленным
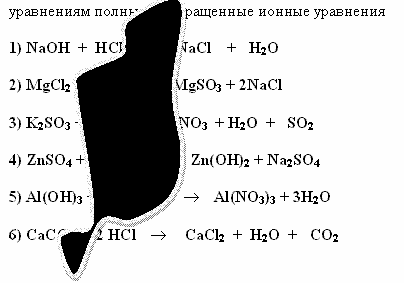
Задание 2.
Вы должны написать полные и сокращенные ионные уравнения к заданиям 2,3
Колдунья с вороном отравили лечебный колодец, в котором был раствор хлористого кальция, который помогал целому городу. Он использовался горожанами при отравлениях, кровотечениях, аллергиях. Они превратили раствор СaCl2 в нерастворимый известняк CaCO3. Помогите жителям «расколдовать» колодец, если в вашем распоряжении есть растворы NaCl, Na2CO3, HCl, H2SO4, Zn(NO3)2.
Задание 3
Олененок спешит к друзьям. Он шел долгих 3 дня. Ему осталось только перейти реку, но река оказалась испорчена – она наполнена раствором серной кислоты. Помогите Олененку воссоединиться с друзьями, если в вашем распоряжении есть растворы NaCl, Ba(OH)2, HCl, CuSO4, Ba(NO3)2.
Далее задания выполняются вами индивидуально. Выполнять их будете завтра на паре (на отдельных листочках). Для этого сохраните их у себя на телефоне или перепишите.
Задание 1 (Ашуров)
1. К неэлектролитам относится:
1) NaCI; 2) MgCI₂; 3) Na₂SiO₃; 4) SiO₂;
2. С выделением газа протекает реакция между:
1) карбонатом натрия и нитратом магния
2) фосфорной кислотой и нитратом бария
3) хлоридом аммония и гидроксидом кальция
4) хлоридом калия и нитратом серебра
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) P₂O₅ + H₂O→ | 1) Na₃PO₄ + H₂↑ |
| Б) H₃PO₄ + Na₂O → | 2) H₃PO₄ + H₂O |
| B) NaOH + P₂O₅→ | 3) H₃PO₄ |
| 4) Na₃PO₄ + H₂O | |
| 5) H₃PO₄ + H₂↑ |
| А | Б | В | |
| Ответ |
Задание 2 (Гаврин)
1. К хорошо растворимым в воде электролитам относится
1) сульфат бария
2) сульфат цинка
3) сульфид меди (11)
4) оксид железа ()
2. Выделение газа происходит в результате взаимодействия ионов
1) H⁺ и CI⁻
2) H⁺ и SO₃²⁻
3) NH₄⁺ и PO₄³⁻
4) NH₄⁺ и S²⁻
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) Na₂O+H₂O → | 1) BaO+NaCI+SO₃ |
| Б) Na₂SO₄+BaCI₂ → | 2) NaOH+H₂↑ |
| В) H₂SO₄+Ba(OH)₂→ | 3) BaSO₄↓+NaCI |
| 4) BaSO₄↓+H₂O | |
| 5) NaOH |
| А | Б | В | |
| Ответ |
Задание 3 (Громов)
1. К хорошо растворимым электролитам в воде относятся
1) гидроксид алюминия
2) гидроксид натрия
3) углекислый газ
4) сахар
2. Выделение газа происходит в результате взаимодействия ионов
1) NH₄⁺ и SO₄²⁻
2) H⁺ и SiO₃²⁻
3) NH₄⁺ и SO₄²⁻
4) H⁺ и S²⁻
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) BaO + SO₂ → | 1) K₂SO₄ + H₂O→ |
| Б) H₂SO₄+H₂O→ | 2) BaSO₃→ |
| B) K₂SO₃+Ba(OH)₂→ | 3) K₂SO₄+H₂↑→ |
| 4) BaSO₄↓ | |
| 5) BaSO₃↓+KOH |
| А | Б | В | |
| Ответ |
Задание 4 (Дьяков)
1. При растворении в воде полностью распадается на ионы
1) гидроксид калия
2) оксид углерода (||)
3) сероводород
4) глюкоза
2. Сокращённое ионное уравнение Cu²⁺+ 2OH⁻= Cu(OH)₂ соответствует взаимодействию
1) нитрата меди (11) и гидроксида железа (11)
2) оксида меди (11) и воды
3) сульфата меди (11) и гидроксида калия
4) карбоната меди (11) и гидроксида бария
3. Выделение газа происходит в результате реакции серной кислоты с
1) гидроксидом калия
2) карбонатом натрия
3) оксидом калия
4) нитратом свинца
Задание 5 (Клопов)
1. К реакциям обмена относят реакцию, уравнение которой
1) CaO + SO₃= CaSO₄
2) 2Na + 2H₂O = 2NaOH +H₂
3) 2Al(OH)₃ = Al₂O₃+H₂O
4) H₂S + 2KOH= K₂S + 2H₂O
2. Электролитом является каждое из двух веществ, формулы которых
1) CaCO₃ CO 3) H₂SO₄Mg(NO₃)₂
2) Ag₂OBaSO₄ 4) PbS C₂H₅OH
3. Выделение газа происходит в результате реакции серной кислоты с
1) SO₃ 2)HNO₃ 3) KCI 4) HBr
Задание 6 (Кузнецова)
1.Вещество, при диссоциации которого образуется сульфид-ион, имеет формулу
1) Na₂S 2) S 3) K₂SO₃ 4) CuSO₄
2. При взаимодействии гидроксида железа (||) с раствором серной кислоты образуются
1) FeSO₄ H₂O 2) Fe₂(SO₄)₃ H₂O 3)) FeSO₄ H₂ 4) Fe₂(SO₄)₃ H₂
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) Fe(OH)₂→ | 1) Fe(OH)₃↓ + NaCI |
| Б) FeCI₃ + NaOH→ | 2) FeO + H₂O |
| B) H₂SO₄p-p + Fe→ | 3) FeSO₄ + H₂↑ |
| 4) FeO + H₂↑ | |
| 5) Fe₂(SO₄)₃ + H₂↑ | |
| 6) Fe₂O₃ + H₂O |
| А | Б | В | |
| Ответ |
Задание 7 (Легенький)
1. К реакциям обмена относится взаимодействие между
1) оксидом натрия и углекислым газом
2) хлоридом железа (||) и хлором
3) соляной кислотой и гидроксидом магния
4) ортофосфорной кислотой и цинком
2. Электролитами являются оба вещества в группе
1) CH₄ NH₄CI 3) CaO BaSO₄
2) C₂H₅OH HNO₃ 4) Fe(OH)₃ HCI
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) H₂S + O₂ → | 1) →H₂SO₃ |
| Б) H₂SO₃ + Na₂O → | 2) → SO₂ + H₂O |
| B) H₂SO₄ + NaOH→ | 3) → Na₂SO₄ + H₂↑ |
| 4) → Na₂SO₄ + H₂O | |
| 5) → Na₂SO₃ + H₂O | |
| 6) → H₂SO₄ |
| А | Б | В | |
| Ответ |
Задание 8 (Маслова)
1. С образованием катионов металла и анионов кислотного остатка диссоциирует
1) сахароза 2) гидроксид натрия 3) хлорид алюминия 4) азотная кислота
2. Какое сокращённое ионное уравнение соответствует реакции между нитратом бария и серной кислотой?
1) Ba²⁺ + SO₄²⁻ = BaSO₄ 3) H⁺ + NO₃⁻ = HNO₃
2) H⁺ + OH⁻ = H₂O 4) Ba²⁺ + 2NO₃⁻ = Ba(NO₃)₂
3. Основанием и кислотой соответственно являются
1) HNO₃ и AI₂O₃ 2) H₂S и NaNO₃ 3) H₂SO₃ и Ca(OH)₂ 4) KOH и H₄P₂O₇
Задание 9 (Машина)
1. К неэлектролитам относится
1) карбонат натрия 3) хлороводород
2) этиловый спирт 4) нитрат цинка
2. Практически необратимо протекает реакция ионного обмена между растворами
1) хлорида калия и нитрата цинка
2) сульфата калия и нитрата бария
3) сульфата натрия и гидроксида калия
4) нитрата натрия и сульфата железа (||)
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) MgO + SO₃ → | 1) →MgSO₃ |
| Б) Mg(OH)₂ + H₂SO₃ → | 2) →MgSO₄ |
| В) Mg(OH)₂ + HCI → | 3) →MgCI₂ + H₂ |
| 4) →MgCI₂ + 2H₂O | |
| 5) →MgSO₃ + 2H₂O | |
| 6) →MgSO₃ + H₂ |
| А | Б | В | |
| Ответ |
Задание 10 (Мелехина)
1. Какое уравнение соответствует реакции обмена
1) CuO + H₂SO₄ = CuSO₄ + H₂O
2) CaO + H₂O = Ca(OH)₂
3) Zn + 2HCI = ZnCI₂ + H₂
4) 2Cr(OH)₃ = Cr₂O₃ + H₂O
2. Вещество, при диссоциации которого образуется сульфат-ион, имеет формулу
1) Na₂S 2) S 3) K₂SO₃ 4) CuSO₄
3. Уравнению реакции Zn(OH)₂ + H₂SO₄ = ZnSO₄ + 2H₂O соответствует сокращённое ионное уравнение
1) H⁺ + OH⁻ = H₂O
2) Zn²⁺ + SO₄²⁻ = ZnSO₄
3) H₂SO₄ + Zn²⁺ = ZnSO₄ + H₂O
4) Zn(OH)₂ + 2H⁺ = Zn²⁺ + 2H₂O
Задание 11 (Некрасов)
1. Сильными электролитами являются
1) HCI AgNO₃ 3) Fe(OH)₃ H₂SO₄
2) Zn(OH)₂ H₂S 4) H₃PO₄ Ag₃PO₄
2. Необратимо протекает реакция ионного обмена между растворами
1) сульфата калия и нитрата алюминия
2) серной кислоты и карбоната натрия
3) гидроксида бария и хлорида натрия
4) нитрата калия и фосфорной кислоты
3. С образованием катионов металла и гидроксид-анионов диссоциирует
1) сахароза 3) гидроксид бария
2) оксид алюминия 4) нитрат алюминия
Задание 12 (Никишина)
1. Ионы СI⁻ образуются при диссоциации
1) KCIO₄ 2) HCIO₃ 3) HCIO 4) KCI
2. Сокращённое ионное уравнение Fe²⁺ + 2OH⁻ = Fe(OH)₂ соответствует взаимодействию веществ:
1) Fe(NO₃)₃ и KOH 3) FeSO₄ и Cu(OH)₂
2) NaOH и FeS 4) Ba(OH)₂ и FeCI₂
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) FeCI₂ + NaOH→ | 1) →FeCI₃ |
| Б) FeCI₃ + KOH→ | 2) → Fe(OH)₂ + 2NaCI |
| В) Fe + HCI→ | 3) → H₂ + FeCI₃ |
| 4) → не взаимодействуют | |
| 5)→ KCI + Fe(OH)₃ | |
| 6) →FeCI₂ + H₂ |
| А | Б | В | |
| Ответ |
Задание 13 (Пронин)
1. Вещество, при диссоциации которого образуется нитрат-анион, имеет формулу
1) NH₄OH 2) Ba(NO₃)₂ 3) NaNO₂ 4) (NH₄)₂SO₄
2. Реакция обмена между растворами соляной кислоты и гидроксида бария проходит до конца за счёт взаимодействия ионов
1) Ba²⁺и CI⁻ 2) Ba²⁺и H⁺ 3) OH⁻ и Ba²⁺ 4) OH⁻ и H⁺
3. С выделением газа протекает реакция между
1) силикатом калия и гидроксидом кальция
2) карбонатом кальция и соляной кислотой
3) нитратом цинка и оксидом бария
4) сульфатом калия и хлоридом магния
Задание 14 (Рогозин)
1. К хорошо растворимым электролитам относится
1) гидроксид бария 2) сульфид меди (||) 3) фосфат железа () 4) карбонат магния
2. При сливании растворов карбоната калия и соляной кислоты в химической реакции участвуют ионы:
1) CO₃²⁻ и CI⁻ 2) K⁺и H⁺ 3) CO₃²⁻ и K⁺ 4) H⁺ и CO₃²⁻
3. К реакциям нейтрализации относится реакция
1) CaO + H₂SO₄ = CaSO₄↓+ H₂O
2) Ba(NO₃)₂ + K₂SO₄ = BaSO₄↓ + 2KNO₃
3) 2NaOH + CuSO₄ = Cu(OH)₂↓ + Na₂SO₄
4) 2H₃PO₄ + 3Ca(OH)₂ = Ca₃(PO₄)₂↓ + 6H₂O
Задание 15 (Сараев)
1. Вещество, при диссоциации которого образуется карбонат-ион, имеет формулу
1) NaHCO₃ 2) CaC₂ 3) Ca(HCO₃)₂ 4) Na₂CO₃
2. К электролитам относится
1) сульфат железа (||) 3) оксид кальция
2) хлор 4) оксид азота (||)
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А) Zn + O₂→ | 1) ZnO + H₂ |
| Б) Zn(OH)₂ + HCI→ | 2) ZnCI₂ + H₂O |
| В) Zn(OH)₂→ | 3) ZnO + H₂O |
| 4) K₂Zn + H₂O | |
| 5) ZnO | |
| 6) Zn + H₂O |
| А | Б | В | |
| Ответ |
Задание 16 (Сараева)
1. К неэлектролитам относится
1) метанол 3) угольная кислота
2) фосфорная кислота 4) соляная кислота
2. Газ выделяется при взаимодействии растворов
1) хлорида калия и серной кислоты
2) карбоната кальция и азотной кислоты
3) серной кислоты и гидроксида бария
4) фосфата натрия и соляной кислоты
3. Установите соответствие между исходными веществами и продуктами реакции.
| Исходные вещества | Продукты реакции |
| А)CaCO₃ + HCI→ | 1. СaCI + NaCO₃ |
| Б) CaCO₃→ | 2. CaCI₂ + H₂CO₃ |
| В) Ca(OH)₂ + HCI→ | 3. CaCI₂ + Na₂CO₃→ |
| 4. не взаимодействуют | |
| 5. CaCI₂ + CO₂ + H₂O | |
| 6. CaO + CO₂ |
| А | Б | В | |
| Ответ |
Задание 17 (Кошкина)
1. К неэлектролитам относится
1) гидроксид магния; 3) оксид углерода (||);
2) гидроксид калия; 4) нитрат меди (||)
2. К реакциям обмена относится взаимодействие между
1) оксидом калия и водой
2) хлором и кислородом
3) азотной кислотой и гидроксидом бария
4) серной кислотой и магнием
3. Молекулярному уравнению реакции Ba(OH)₂ + 2HNO₃ → Ba(NO₃)₂ +2 H₂Oсоответствует сокращённое ионное уравнение
1) Ba(OH)₂ + H⁺→Ba²⁺ + H₂O
2) 2OH⁻ + 2H⁺ → 2H₂O
3) Ba²⁺ + 2NO₃⁻→Ba(NO₃)₂
4) OH + H → H₂O
Задание 18 (Крестьянинов)
1. Электролитом не является
1) гидроксид калия 3) азотная кислота
2) хлорид калия 4) сахароза
2. Сокращённое ионное уравнение H⁺ + OH⁻→H₂O соответствует реакции
1) KOH + H₂SO₄→
2) NH₄OH + H₂SO₄→
3) Fe(OH)₂ + H₂SO₄→
4) Ba(OH)₂ + H₂SO₄→
3. При добавлении раствора карбоната натрия к раствору хлороводородной кислоты
1) выпадает осадок
2) выделяется газ
3) выпадает осадок и выделяется газ
4) видимых изменений не происходит
Задание 19 (Сенченко)
1. Основанием и кислотой соответственно являются
1) HNO₃ и N₂O₅ 3) H₂SO₄ и Ca(OH)₂
2) H₂S и NaNO₃ 4) KOH и Na₃PO₄
2. Уравнением электролитической диссоциации является
1) CaCO₃ →CaO + CO₂
2) NH₄CI→ NH₃ + HCI
3) H₂SO₄→2H⁺ + SO₄²⁻
4) HCI + NaOH→NaCI + H₂O
3. Осадок не образуется при смешивании растворов
1) карбоната натрия и серной кислоты
2) сульфата натрия и нитрата бария
3) карбоната кальция и соляной кислоты
4) сульфита калия и хлорида бария
Задание 20 (Тихонова)
1. С образованием катионов металла в растворах диссоциируют
1) основные оксиды 3) основания
2) кислотные оксиды 4) кислоты
2. К реакциям нейтрализации относится реакция
1) Ca(OH)₂ + H₂CO₃=CaCO₃↓ + 2H₂O
2) Ba(NO₃)₂ + K₂SO₄=BaSO₄↓ + 2KNO₃
3) 2NaOH + CuSO₄ = Cu(OH)₂ + Na₂SO₄
4) CO₂ + Ca(OH)₂= CaCO₃ + H₂O
3. Сульфиту натрия соответствует формула
1) NaHS 2) Na₂SO₄ 3) Na₂SO₃ 4) Na₂S