Распределение Максвелла.
1. Для распределения Максвелла по модулям скоростей молекул для разных газов при одинаковой температуре верны утверждения:
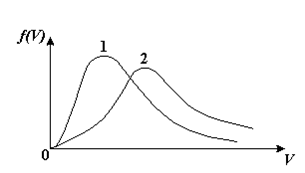 1) График 1 соответствует газу с большей массой молекул
1) График 1 соответствует газу с большей массой молекул
2) График 2 соответствует газу с большей молярной массой.
3) Площадь под этими кривыми тем больше, чем больше молярная масса газа
4) Площади под этими кривыми одинаковы.
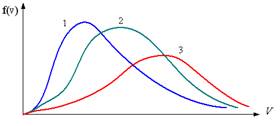 3. В трех одинаковых сосудах находится одинаковое количество одного и того же газа при разных температурах. Функцию распределения молекул по скоростям в сосуде с максимальной температурой будет описывать кривая, обозначенная номером…
3. В трех одинаковых сосудах находится одинаковое количество одного и того же газа при разных температурах. Функцию распределения молекул по скоростям в сосуде с максимальной температурой будет описывать кривая, обозначенная номером…
4. Правильные утверждения о средней квадратичной скорости (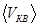 ) частиц системы, подчиняющейся распределению Максвелла:
) частиц системы, подчиняющейся распределению Максвелла:
1) При одинаковой температуре 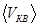 молекул различных идеальных газов одинакова.
молекул различных идеальных газов одинакова.
2) Средняя квадратичная скорость 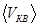 молекул газа при любой температуре меньше наиболее вероятной скорости.
молекул газа при любой температуре меньше наиболее вероятной скорости.
3) Чем больше масса молекулы газа, тем меньше 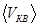 .
.
4) При возрастании температуры системы в четыре раза средняя квадратичная скорость 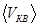 молекул увеличивается в два раза.
молекул увеличивается в два раза.
5. В сосуде находятся одинаковые количества азота N2 (M 1 = 28 г/моль) и водорода H2 (M 2 = 2 г/моль). Функции распределения молекул этих газов по скоростям будут описываться кривыми, изображенными на рисунке под номером
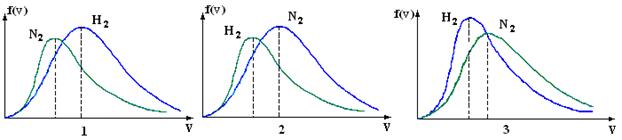
1) 1
2) 2
3) 3
4) правильного рисунка нет
6. Если средняя квадратичная скорость молекул некоторого газа равна 500 м/с, то наиболее вероятная скорость составляет … м/с.
1) 327
2) 250
3) 630
4) 408
7. Если при нагревании некоторого газа наиболее вероятная скорость молекул газа увеличилась в 2 раза, то средняя квадратичная скорость … раз(а).
1) увеличится в 4
2) уменьшится в 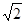
3) уменьшится в 8
4) увеличится в 2
9. Три газа: водород (M 1 = 2 г/моль), гелий (M 2 = 4 г/моль) и кислород (M 3 = 32 г/моль) находятся при одинаковой температуре T. Тогда значение f (Vвер) функции распределения Максвелла, соответствующее наиболее вероятной скорости молекул,..
1)одинаково для всех газов
2) максимально для водорода
3) минимально для гелия
4) максимально для кислорода
10. Три газа: водород (M 1 = 2 г/моль), гелий (M 2 = 4 г/моль) и кислород (M 3 = 32 г/моль) находятся при одинаковой температуре T. Тогда наиболее вероятная скорость Vвер …
1) у всех газов одинакова
2) у кислорода наибольшая
3) у гелия наименьшая
4) у водорода наибольшая
Первое начало термодинамики
1. Для адиабатического процесса в идеальном газе справедливы утверждения:
1) В ходе процесса газ не обменивается энергией с окружающими его телами (ни в форме работы, ни в форме теплопередачи).
2) Если газ расширяется, то его внутренняя энергия уменьшается.
3) Если газ расширяется, то его внутренняя энергия увеличивается.
4) В ходе процесса изменяются параметры состояния газа – объем, давление, температура.
2. Правильные утверждения о внутренней энергии системы:
1) внутренняя энергия системы является функцией ее состояния – зависит от ее термодинамических параметров состояния
2) во внутреннюю энергию системы не входит механическая энергия движения и взаимодействия системы как целого
3) приращение внутренней энергии зависит от пути (способа) перехода системы из начального состояния в конечное
4) внутренние энергии двух тел, находящихся в тепловом равновесии друг с другом, всегда одинаковы
3. Двухатомному идеальному газу в результате изобарического процесса подведено количество теплоты  . На увеличение внутренней энергии газа расходуется часть теплоты
. На увеличение внутренней энергии газа расходуется часть теплоты 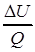 , равная
, равная
1) 0,29
2) 0,71
3) 0,60
4) 0,25