Если экстраплоскость находится в верхней части кристалла, то дислокацию называют положительной, а если в нижней – то отрицательной. Скольжение происходит по плоскости, в которой находится и линия дислокации и вектор Бюргерса. Особенности скольжения КД: 1. Это движение края экстраплоскости по плоскости скольжения под действием напряжений. 2. Не обусловлено диффузией, поэтому может идти при сколь угодно низких температурах. 3. Не связано с переносом массы, поэтому называется консервативным движением. 4. Происходит преимущественно по наиболее плотноупакованным плоскостям – по плоскостям {111} в ГЦК-решетке и по плоскостям {110} в ОЦК-решетке. 5. При низких напряжениях со скоростью порядка 10-7-10-8 см/с. Скорость скольжения не может превышать скорость распространения в данном кристалле упругой деформации, т.е. скорости звука в кристалле. При больших напряжениях в кристалле Fe-3,25%Si зафиксирована скорость скольжения дислокаций порядка 10-2 см/с.
 На рисунке показана краевая дислокация внутри кристалла и ступенька на его правой боковой грани, образовавшаяся в результате сдвига справа налево верхней части кристалла относительно нижней. Если под действием сдвигающей силы дислокация будет скользить справа налево, то сдвиг будет охватывать все большую часть плоскости скольжения. Когда дислокация выйдет на левую боковую грань кристалла, здесь образуется ступенька.
На рисунке показана краевая дислокация внутри кристалла и ступенька на его правой боковой грани, образовавшаяся в результате сдвига справа налево верхней части кристалла относительно нижней. Если под действием сдвигающей силы дислокация будет скользить справа налево, то сдвиг будет охватывать все большую часть плоскости скольжения. Когда дислокация выйдет на левую боковую грань кристалла, здесь образуется ступенька.
33. Решетка совмещенных узлов (РСУ).
Решетка совмещенных узлов соответствует определенной разориентировке зерен и характеризуется величиной Σ, равной обратной доле совпадающих узлов. Значение Σ можно определить как отношение объема элементарной ячейки РСУ к объему элементарной ячейки кристаллической решетки металла. Чем меньше Σ,тем короче период повторяемости в плоскости границы и, следовательно выше ее упорядоченность. Разориентировка, отвечающие малым Σ т.е. с высокой степенью упорядоченности или совпадения называют специальными. Наличие высокой степени порядка таких границ проводит к резкому отличию их свойств от свойств границ низкоупорядоченных, так называемого общего типа. Специальные границы обладают более низкими поверхностным натяжением, низкими активационными параметрами (энергия активации, энтропия активации) и высокими активационными параметрами пограничной диффузии. Из геометрических соображений специальными можно считать границы со сколь угодно большими, но определенного значения Σ. Однако фактически специальными границами можно считать лишь границы, свойства которых отличаются от свойств границ общего типа.
|
|
| На рис. Приведена в качестве примера модель границы наклона с разориентировкой σ=5(36,9 (001)), проходящей по плотно- и неплотноупакованным плоскостям в РСУ. |
|
|

34. Что такое «эффект памяти формы» и каков его механизм?
Эффект памяти формы — явление возврата к первоначальной форме при нагреве, которое наблюдается у некоторых материалов после предварительной деформации.После придания образцу определенной формы при температуре устойчивости высокотемпературной фазы, ему придают новую форму при температуре ниже Мн. Нагрев образца приводит к восстановлению его исходной формы. При нагружении температура начала мартенситного превращения выше чем Мн и обозначается Мд. Исходной фазе придана определенная форма. Затем материал охладили до темп ниже Мн и под действием нагрузки произведено мартенситное превращение при условии сохранение термоупругого равновесия между исходной и новой фазой. Снятие нагрузки в низкотемпературной области устраняет только упругую деформацию, а деформация вызванная превращением сохранятеся. Последующий нагрев приводит к обратному превращению, имеющаяся фаза обратимо и по тем же плоскостям и направлениям переходит в исходную фазу, а образец принимает первоначальную форму. Эффект у NiTi (нитинол).
|
|
35. Кристаллическая структура и область существования модификаций Fe.
Структура решетки: кубическая объемоцентрированная. Период решетки: 2,870 А. Температура Дебая: 460 К. Для Fe характерен полиморфизм, он имеет 4 кристаллические модификации: 1) до 910°С сущ-ет α-Fe (феррит) с ОЦК решеткой; 2) в температурном интервале 768-910°С сущ-ет β-Fe, кот отличается от α-Fe только параметрами кристаллической решетки и магнитными св-вами; 3) в температурном интервале 910-1401°С сущ-ет γ-Fe (аустенит) с ГЦК решеткой; 4) выше 1401°С до температуры плавления устойчив δ-Fe с ОЦК решеткой.
36. Что такое мартенсит? Металлографическая структура мартенсита.
Мартенсит – пересыщенный упорядоченный твердый раствор углерода в α-Fe, имеющий тетрагональную структуру и в котором упорядоченное расположение атомов углерода. Мартенсит в стали не является стабильной фазой и стремится к распаду, особенно при нагреве. Структура представляет собой узкие пластины, по форме приближающиеся к иглам и закономерно ориентированные по высокотемпературной фазе.
37. Твердые растворы. Дальний и ближний порядок.
Твёрдый раствор - твердые фазы, содержание компонентов в которых может изменяться в определенных пределах (в пределах области гомогенности). По протяженности области гомогенности твердые растворы делятся на: растворы с неограниченной растворимостью компонентов, растворы с ограниченной растворимостью компонентов. По типу расположения атомов растворяемого элемента твердые растворы делятся на: растворы замещения; растворы внедрения; растворы вычитания. Дальний порядок – это упорядоченность во взаимном расположении атомов или молекулв веществе (в жидком или твёрдом состоянии), которая (в отличие от ближнего порядка) повторяется на неограниченно больших расстояниях.
Дальним порядком в расположении молекул обладают, например, кристаллы. Ближний порядок — это упорядоченность во взаимном расположении атомов или молекул в веществе, которая (в отличие от дальнего порядка) повторяется лишь на расстояниях, соизмеримых с расстояниями между атомами, то есть ближний порядок есть закономерность в расположении соседних атомов. Ближним порядком в расположении молекул обладают, например, аморфные тела и жидкости.
38. Атомный механизм упорядочения.
 Дислокации, испущенные источниками, накапливаются в кристалле и их число возрастает. Теория дислокаций объясняет упрочнение металла при деформации (наклеп) затруднением движения скользящих дислокаций в присутствии большого числа других дислокаций, принадлежащих той же или другой системе скольжения. Предложено большое число различных механизмов упрочнения. Большинство из них может быть сведено к упругому взаимодействию дислокаций. В связи с этим скалывающее напряжение τсд, вызывающее деформацию сдвига, может быть связано с плотностью дислокаций NД: τсд=Ab√NД. Накопление дислокаций при деформации вызывается задержкой и закреплением у препятствий дислокаций, испущенных источниками. Препятствиями могут служить неподвижные (сидячие) дислокации, скопления дислокаций, границы блоков и зерен, группы вакансий. Группировки дислокаций у препятствий могут иметь разное строение; в качестве модели такой группировки рассмотрим скопления, изображенные на рис. 59, а. Эти группы возникли в результате накопления дислокаций, испущенных источником S, у препятствий Р и Q. Нагромождение дислокаций у препятствий вызывает их упругое взаимодействие. Напряжения, создаваемые таким скоплением, пропорциональны числу дислокаций в нем. Напряжение вокруг скоплений дислокаций в основном определяет упрочнение, так как они препятствуют скольжению в действующей плоскости и в смежных. С ней плоскостях. Когда упругие напряжения в области скопления достигнут величины, сравнимой с приложением скалывающим напряжением т, источник перестанет действовать и деформация прекратится. Для увеличения степени деформации нужно снова вызвать действие источника, для чего следует увеличить скалывающее напряжение т. Таким образом, деформация сопровождается упрочнением металла. Оно затухает и наступает насыщение.
Дислокации, испущенные источниками, накапливаются в кристалле и их число возрастает. Теория дислокаций объясняет упрочнение металла при деформации (наклеп) затруднением движения скользящих дислокаций в присутствии большого числа других дислокаций, принадлежащих той же или другой системе скольжения. Предложено большое число различных механизмов упрочнения. Большинство из них может быть сведено к упругому взаимодействию дислокаций. В связи с этим скалывающее напряжение τсд, вызывающее деформацию сдвига, может быть связано с плотностью дислокаций NД: τсд=Ab√NД. Накопление дислокаций при деформации вызывается задержкой и закреплением у препятствий дислокаций, испущенных источниками. Препятствиями могут служить неподвижные (сидячие) дислокации, скопления дислокаций, границы блоков и зерен, группы вакансий. Группировки дислокаций у препятствий могут иметь разное строение; в качестве модели такой группировки рассмотрим скопления, изображенные на рис. 59, а. Эти группы возникли в результате накопления дислокаций, испущенных источником S, у препятствий Р и Q. Нагромождение дислокаций у препятствий вызывает их упругое взаимодействие. Напряжения, создаваемые таким скоплением, пропорциональны числу дислокаций в нем. Напряжение вокруг скоплений дислокаций в основном определяет упрочнение, так как они препятствуют скольжению в действующей плоскости и в смежных. С ней плоскостях. Когда упругие напряжения в области скопления достигнут величины, сравнимой с приложением скалывающим напряжением т, источник перестанет действовать и деформация прекратится. Для увеличения степени деформации нужно снова вызвать действие источника, для чего следует увеличить скалывающее напряжение т. Таким образом, деформация сопровождается упрочнением металла. Оно затухает и наступает насыщение.


Рис. 59. Скопление дислокаций у препятствия: а — схема; б — скопление дислокаций у границы зерна, при котором упрочнение не возрастает с ростом деформации. Насыщение упрочнения происходит при большом значении т, при котором головные дислокации скоплений прорываются сквозь препятствия Р и Q под действием дислокаций, вновь образуемых источником, но плотность и распределение их в скоплении не изменяются.
39. Сдвиговой механизм пластической деформации.
Механизмы пластической деформации подразделяются на 2 группы – это сдвиговые и диффузионные. В свою очередь сдвиговые(которые нас интересуют) пластическая деформация осуществляется двойникованием и скольжением. Скольжение в кристалл. решетке протекает по плоскостям и направлениям с наиболее плотной упаковкой атомов, где величина сопротивлений сдвигу наименьшая. Это объясняется тем, что расстояние между соседними атомными плоскостями наибольшее, т.е связь между ними наименьшая. Плоскости скольжения и направления скольжения, лежащие в этих плоскостях, образуют систему скольжения. Скольжение осуществляется в результате перемещения в кристалле дислокаций. При действии вдоль плоскости скольжения касательных напряжений атомы вблизи ядра дислокации перемещаюся справо на лево на расстояния, значительно меньше межатомных. Двойникование. Пластическая деформация некоторых металлов, кроме скольжения,может осуществляется двойникованием, которое сводится к переориентировке части кристалла в положение, симметричное по отношению к первой части относительно плоскости, называемой плоскостью двойникования. Двойникование подобно скольжению сопровождается прохождением дислокаций сквозь кристалл. Схемы пластической деформации монокристалла скольжением (а) и двойникованием (б) при растяжении.

40. Механизм спинодального распада пересыщенного твердого раствора.
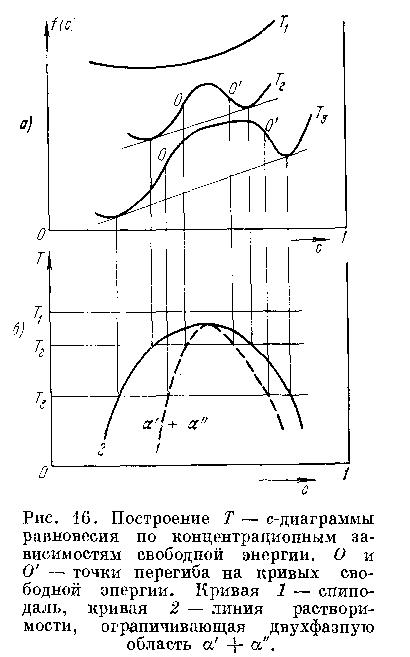
Условия реализации спинодального механизма распада пересыщенного твёрдого раствора: - фазы должны быть изоморфны (одинаковая кристаллическая решётка);- неограниченный твёрдый раствор. Принципиальная схема спинодального распада.
В процессе спинодального распада твердых растворов происходят следующие процессы: 1. Для сплавов, составы которых отвечают вогнутым участкам кривой на графике F(c)-c, образование малых концентрационных неоднородностей приводит к повышению свободной энергии – т.е. сплавы являются метастабильно устойчивыми. Также однородный твердый раствор, будучи переохлажденным, попадает в область метастабильной устойчивости (между спинодалью и границей растворимости). 2. Выход системы из однородного (метастабильного состояния) путем образования флуктуационной критической концентрационной неоднородности. Распад твердого раствора не может сопровождаться постоянным уменьшением свободной энергии – он возможен лишь при флуктуационном преодолении энергетического барьера (образования зародышей новой фазы, связанного с увеличением свободной энергии). Уменьшение свободной энергии происходит за счет последующего роста зародышей. Если же твердый раствор попадает в область, ограниченную спинодалью, то он становится абсолютно неустойчивым, и испытывает распад – с понижением свободной энергии вплоть до равновесного состояния (гетерогенного состояния).

Большое значение имело обнаружение периодического распределения выделяющихся фаз (модулированной структуры) при распаде твердого раствора на две фазы, которые отличаются только концентрацией и параметром решетки. Модулированную структуру впервые наблюдали Дэниел и Липсон в сплаве Си—Ni—Fe. Они обнаружили сателлиты основных рентгеновских рефлексов, соответствующих однофазной структуре. Существование этих сателлитов можно объяснить, если предположить, что параметр решетки (и концентрация Си) периодически изменяется в направлениях кристаллографических осей. Период такой модулированной структуры имеет порядок 100 А. В настоящее, время имеются прямые наблюдения модулированных структур с помощью электронной микроскопии. Привести схему формирования структуры при спинодальном распаде. Начальная стадия спинодального распада состоит в образовании синусоидальных флуктуаций состава с очень малой амплитудой. Границы раздела в процессе незавершенного распада следует считать очень размытыми с непрерывным изменением состава. На начальном этапе концентрационные волны сохроняют когерентную связь, но с увеличениет амплитуды концентрации происходит увеличение разности параметров решеток фаз и происходит разрыв когерентности. Самой важной особенностью спинодального распада следует считать отсутствие необходимости в образовании зародыша новой фазы и, соответственно, увеличение свободной энергии на начальном этапе превращения.
41. Краевая дислокация. Строение. Энергия краевой дислокации. (см вопрос 32)
 Для краевой дислокации вектор Бюргерса b параллелен плоскости сдвига и перпендикулярен экстраплоскости. Энергия краевой дислокации
Для краевой дислокации вектор Бюргерса b параллелен плоскости сдвига и перпендикулярен экстраплоскости. Энергия краевой дислокации
где G – модуль сдвига; m – коэффи-
циент Пуассона (для металлов m»⅓); ro – радиус ядра дислокации (несколько межатомных расстояний); R – расстояние, на которое распространяется упругая деформация от дислокации.
42. Что такое линия Чернова – Людерса и причины их возникновения.
Еще в 1860 г. Людерс, а затем независимо от него Чернов обнаружили, что при растяжении образцов железа и стали на их поверхности образуются специфические фигуры. Чернов связал их возникновение с волнами упругих напряжений. Он обнаружил, что предварительно отполированные образцы становятся матовыми, и пришел к заключению, что мягкая литая сталь обладает драгоценным свойством – способностью фиксировать на своей полированной поверхности рисунок волн упругих напряжений, если усилия превосходят предел упругости. На рис. 7.1 воспроизводятся оригинальные рисунки из сообщения Чернова. Было обращено внимание на то, что одни линии деформации вогнутые, а другие – выпуклые. Чернов показал, что вогнутые линии связаны с локальными впадинами на поверхности, образующимися в результате действия растягивающих волн напряжений, а выпуклые (локальное выпучивание) – с действием сжимающих напряжений. В современной трактовке перемещение полос Чернова-Людерса по поверхности деформируемого образца рассматривается как автоволновой процесс. Ротационные процессы существенно изменяют состояние поверхности деформируемого образца, а следовательно и условия рассеяния света на ней. Подтверждением связи распространения полос Чернова–Людерса с волновой природой пластической деформации является совпадение скоростей распространения этих волн и фронта полосы. Последнюю измеряют путем регистрации распространения полосы на видеопленку.
43. Рост зерна при нагреве металла (см. вопрос 25).
44. Вывести формулу для определения критического размера зародыша при кристаллизации.
Энергетическое состояние системы характеризуется особой термодинамической функцией G, называемой свободной энергией Гиббса. При температуре Т0 свободные энергии двух фаз равнф, эта температура называется равновесной теоритической температурой или т емпературой термодинамического равновесия (рис.1). При T0: GL=GS, где GL и GS – свободные энергии Гиббса жидкой и твердой фаз. Свободная энергия Гиббса может быть определена следующим образом: G=E-TS+PV, где Е – внутренняя энергия, S – энтропия, Т – абсолютная температура (К), V – объем, Е+РV = H, где Н – энтальпия. Тогда свободная энергия может быть выражена в виде: G=H-TS [1] Так как при Т0 GL=GS, то HL – T0SL = HS – T0SS; HL – HS = T0(SL – SS) [2]; HL – HS = L [3], где L – скрытая теплота плавления. SL – SS = ∆S [4]. Тогда L = ∆ST0, то есть ∆S = L/T0 [5]. Для начала процесса кристаллизации необходимо переохлаждение ниже температуры Т0. Величиной или степенью переохлаждения называется разность между температурой термодинамического равновесия (Т0) и фактической температурой (Т): ∆Т = Т0 – Т [6]. Зарождение кристаллитов. При любом фазовом превращении происходит изменение свободной энергии, которое описывается формулой: ∆G = – ∆Gоб + ∆Gгр; ∆G = – (∆Gхим + ∆Gдеф) + (∆Gпов + ∆Gупр)
∆Gдеф = 0; ∆Gупр = 0; ∆G = – ∆Gхим + ∆Gпов [7]
Для зародыша сферической формы радиуса r: ∆Gхим = (∆GL – ∆GS)*(4/3)*πr^3, [8] где (GL – GS) – разница свободных энергий жидкой (L) и твердой (S) фаз – движущая сила превращения; (4/3)πr^3 – объем зародыша сферической формы. Обратимся к формулам [1] и [2], тогда можно записать: (GL – GS) = (HL – HS) – T(SL – SS). Согласно формулам [3], [4] и [5]: GL –GS = L – T(L/T0). Путем несложных математических вычислений, получаем: GL –GS = L*(T0 – T)/T0. Учитывая формулу [6]: GL – GS = (L/T0)∆T. Тогда формула [8] принимает вид: ∆G = – (L/T0)∆T(4/3)πr^3 [9] Для сферического зародыша с радиусом r: ∆Gпов = 4π(r^2)γ, [10] где γ – удельная поверхностная свободная энергия; 4πγr^2 – площадь поверхности зародыша сферической формы. Принимая во внимание ф-лы [9] и [10], ф-лу [7] можно записать: ∆G =  [11]. Для определения критического размера зародыша (rкр) приравняем к нулю первую производную от ∆G по r, т.к. rкр функция проходит через максимум:
[11]. Для определения критического размера зародыша (rкр) приравняем к нулю первую производную от ∆G по r, т.к. rкр функция проходит через максимум:
 . Продифференцировав ф-лу [11], получим:
. Продифференцировав ф-лу [11], получим:
 . Решив это квадратное уравнение найдем:
. Решив это квадратное уравнение найдем:  [12].
[12].
45. Физические свойства железа.
Чистое железо (атомный номер 26; атомная масса 55,85; электронная структура 1s22s22p63s23p63d64s2) –это переходный ферромагнитный металл. Железо существует в 2 аллотропических модификациях. Ниже 910 и выше 1401 0С до температуры плавления (Тs=1539°С) стабильно -железо с ОЦК решеткой, между 910 и 1401 –  - железо с ГЦК решеткой. Температура кипения-3200°С. Чистое железо, содержащее 99.9917 %Fe и только 0.0083% примесей, имеет твердость по Бринелю 490МПа, плотность 7.874 т/м3, намагниченность насыщения 0,1714 Тл, коэффициент линейного расширения 11,7•10-6 К-1, удельное электрическое сопротивление 97 нОм•м, температурный коэффициент электросопротивления 6,5 •10-3 К-1. Чистое железо пластично, имеет серебристо-белый цвет. Технически чисто железо – это сплав железа с углеродом с содержание С менее 0,025%. Примеси (C, Mn, Si, S, P, O, N, H, Cu, Cr, Ni). Твердость технически чистого железа, содержащего 99,9% Fe, значительно выше, чем химически чистого; она равна приблизительно 900МПа. Недостаток – сильно ржавеет. Обладает сильными магнитными свойствами (ферромагнетик), хорошей тепло- и электропроводностью
- железо с ГЦК решеткой. Температура кипения-3200°С. Чистое железо, содержащее 99.9917 %Fe и только 0.0083% примесей, имеет твердость по Бринелю 490МПа, плотность 7.874 т/м3, намагниченность насыщения 0,1714 Тл, коэффициент линейного расширения 11,7•10-6 К-1, удельное электрическое сопротивление 97 нОм•м, температурный коэффициент электросопротивления 6,5 •10-3 К-1. Чистое железо пластично, имеет серебристо-белый цвет. Технически чисто железо – это сплав железа с углеродом с содержание С менее 0,025%. Примеси (C, Mn, Si, S, P, O, N, H, Cu, Cr, Ni). Твердость технически чистого железа, содержащего 99,9% Fe, значительно выше, чем химически чистого; она равна приблизительно 900МПа. Недостаток – сильно ржавеет. Обладает сильными магнитными свойствами (ферромагнетик), хорошей тепло- и электропроводностью
46. Кристаллическая структура модификаций Fe.
Кристаллические модификации а-, g- и d-Fe открыты в 1868 Д. К. Черновым. До f 1042К кристаллическая решётка объёмноцентрированная кубическая, параметр решётки а = 0,2 86645 нм — а-Fe, между t 1173 и 1673К — гранецентрированная, а = 0,3 637 нм — g-Fe, выше f 1673К — объёмноцентрированная, а = 0,2 925 нм — d-Fe, между f 1042 и 1173К – объёмноцентрированная, а = 0,2 895 нм — d-Fe (иногда называется бета — b). Модификации g- и d-Fe парамагнитны.
47. Кристаллическая структура модификаций углерода.
Кристаллические структуры аллотропных модификаций углерода: a — алмаз, b — графит, c — лонсдейлит (гексагональный алмаз), d — карбин, e — фуллерен C60, f — аморфный углерод, g — одностенная углеродная нанотрубка. Углерод обладает свойством полиморфного превращения: имеет гексагональный тип решетки (графит) или решетку с КЧ=4(типа алмаза). Период решетки: 3,570 А. Кристаллические модификации углерода — алмаз и графит. В виде графита углерод находится в сплавах железа типа чугунов. Тпл графита -3500°С, плотность 2,5 г/см3. В сплавах железа с углеродом углерод находится в состоянии твердого раствора с Fe и в виде хим соединения Fe3C – цементита(6,67%С). При норм усл термодинамически устойчив только графит, а алмаз и другие формы метастабильны. При атмосферном давлении и темп-ре выше 1200 K алмаз начинает переходить в графит. Также известны модификации углерода: фуллерены (получают при высоких темп-рах, 64 атома выстраиваются на равных расстояниях в сферу), трубки, карбин.
47. Цементит. Физические свойства и кристаллическая структура.
Цементит — карбид железа, химическое соединение с формулой Fe3C. Концентрация углерода 6,67% по массе — предельная для железоуглеродистых сплавов. Цементит — метастабильная фаза; образование стабильной фазы — графита во многих случаях затруднено. Цементит имеет орторомбическую кристаллическую решётку, очень тверд и хрупок, слабо магнитен до 210 °C. В зависимости от условий кристаллизации и последующей обработки цементит может иметь различную форму — равноосных зёрен, сетки по границам зёрен, пластин, а также видманштеттову структуру. Цементит в разных количествах, в зависимости от концентрации, присутствует в железоуглеродистых сплавах уже при малых содержаниях углерода. Формируется в процессе кристаллизации из расплава чугуна. В сталях выделяется при охлаждении аустенита или при нагреве мартенсита. Цементит является фазовой и структурной составляющей железоуглеродистых сплавов, составной частью ледебурита, перлита, сорбита и троостита. Цементит — представитель так называемых фаз внедрения, соединений переходных металлов с легкими металлоидами. В фазах внедрения велики доля как ковалентной, так и металлической связи. Твёрдость по Брюнеллю больше 800 кг/мм2.
49. Обосновать факт более высокого содержания углерода в фазах метастабильной системы.
Если в равновесии с жидкой фазой, аустенитом и ферритом нах-ся графит, то равновесие является стабильным. В случае, когда равновесие с этими фазами, т.е. растворами на базе Fe, нах-ся цементит, равновесие явл метастабильным. В обоих случаях равновесию любого сплава Fe – С заданного состава соответствует минимум термодинамического потенциала, но его минимальное значение в случае стабильного равновесия меньше, чем в случае метастабильного равновесия. На рис. показано изменение своб энергии в стабильной и метастабильной системе в ф-ции содержания углерода при высокой темп-ре, при кот в равновесии нах-ся аустенит. Видно, что уменьшение своб энергии (ΔF) должно приводить к распаду цементита (графитизации). Видно также, что содержание углерода в аустените в стабильной системе (С’) ниже, чем в метастабильной (С). Сказанное относится и к равновесию феррита с графитом или цементитом.
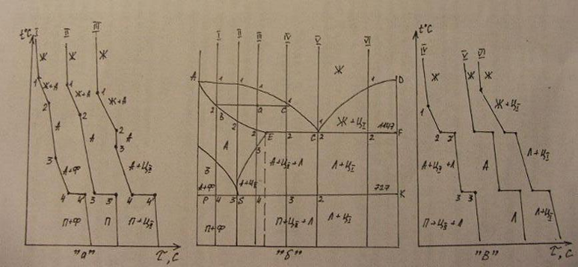
50. Построить кривую охлаждения по метастабильной системе сплава с Х% углерода.
51. Построить кривую охлаждения по стабильной системе сплава с Х% углерода.
52. Перечислить дефекты структуры в сталях.
Для вторичной микроструктуры горячедеформированной углеродистой стали характерны: строчечное расположение неметаллических включений и полосчатое расположение доэвтектоидного феррита и перлита (полосчатая структура). Образование полосчатой структуры обусловлено неоднородностью распределения фосфора в аустените. Полосчатая структура обусловливает анизотропию механических св-в горячедеформированных изделий. Большой размер зерна первичного аустенита приводит к появлению еще одной аномалии во вторичной микро структуре углеродистой стали – образованию видманштеттовой структуры. Эта структура характеризуется пластинчатыми образованиями доэвтектоидного феррита или игольчатыми – вторичного цементита, ориентированно располагающимися на темном фоне перлита. Возникновение такой структуры связано с тем, что, например, в доэвтектоидной стали избыточный феррит выделяется не только на границах, но и внутри крупных зерен аустенита. Помимо большого размера зерна аустенита, образованию видманштеттовой структуры способствует ускоренное охлаждение стали от высоких температур. Сталь с такой структурой обладает повышенной хрупкостью.
53. Принципы маркировки сталей.
Для обозначения марок стали разработана система, принятая в ГОСТах. Обозначения состоят из небольшого числа цифр и букв, указывающих на примерный состав стали. Каждый легирующий элемент обозначается буквой: Н - никель; Х - хром; К - кобальт; М - молибден; Г - марганец; Д - медь; Р - бор; Б - ниобий; Ц - цирконий; С - кремний; П - фосфор, Ч - редкоземельные металлы; В - вольфрам; Т - титан; А - азот (буква А в середине марочного обозначения указывает на наличие азота, специально введенного в сталь); Ф - ванадий; Ю – алюминий. Первые цифры в обозначении показывают среднее содержание углерода в сотых долях процента (у высокоуглеродистых инструментальных сталей в десятых долях процента). Цифры, следующие после буквы, указывают на примерное содержание данного легирующего элемента (при содержании элемента менее 1 % цифра отсутствует; при содержании около 1 % - цифра 1 и около 2 % - цифра 2 и т.д.). Следовательно, сталь состава 0,10-0,15 % С и 1,3-1,7 % Mn будет обозначаться 12Г2; сталь состава 0,28-0,35 % С; 0,8-0,11 % Cr; 0,9-1,2 % Mn; 0,8-1,2 % Si - 30ХГС и т.д. Чтобы показать, что в стали ограничено содержание серы и фосфора (S<0,03 % и P<0,03 %), а также соблюдены все условия металлургического производства высококачественной стали, в конце обозначения марки ставят букву А. (Буква А в середине марочного обозначения указывает на наличие азота, специально введенного в сталь). Особо высококачественная сталь обозначается буквами Ш, ВД, ВИ, ПД и т.д. в конце наименования марки, где ВД обозначает, что сталь или сплав получен вакуумно-дуговым переплавом, Ш - электрошлаковым переплавом, ВИ - методом вакуумно-индукционной выплавки, ПД - плазменно-дуговым и т.д. Наименование марок сплавов состоит только из буквенных обозначений элементов. Исключение составляет никель, после обозначения которого указываются цифры его среднего содержания в процентах. Однако в ряде случаев для сокращения числа знаков в обозначении несколько отступают от точного соблюдения системы ГОСТов (особенно это относится к сложнолегированным сталям). Нестандартные стали обозначают самым различным образом. Так, опытные марки, выплавленные на заводе "Электросталь", обозначаются буквой И (исследовательские) и П (пробные) и порядковым номером, например, ЭИ179, ЭИ276, ЭП398 и т.д. Опытные марки, выплавленные на металлургическом заводе "Днепроспецсталь", обозначают ДИ 80, где Д - завод-изготовитель, И - исследовательская, 80 - порядковый номер, присвоенный марке стали. В инструментальных сталях, имеющих углерода более 1 %, цифры, обозначающие его содержание, полностью опускают. Так, инструментальная сталь с 1,45-1,70 % С; 11-12,5 % Cr и 0,5-0,8 % Mo обозначается Х12М. При маркировке электротехнических сталей (типа 1211, 1313, 2211 и т.д.) в обозначении марки цифры означают: первая - класс по структурному состоянию и виду прокатки; вторая - содержание кремния; третья - группу по основной нормируемой характеристике. Вместе первые три цифры в обозначении марки означают тип стали; четвертая - порядковый номер типа стали. Для изготовления строительных стальных конструкций со сварными и другими соединениями применяются марки стали типа С235, С245, С255, С345, С590К и т.д. Буква С означает сталь строительная, цифры условно обозначают предел текучести проката, буква К - вариант химического состава. По требованию потребителя массовая доля меди в стали С345, С375, С390, С440 должна быть 0,15 - 0,30 %, при этом к обозначению стали добавляется буква Д, например, С345Д. Для изготовления рельсов широкой колеи типов Р75, Р65 и Р50 применяются стали марок М76 и М74, где буква М указывает способ выплавки (мартеновский), цифры - среднее содержание углерода в сотых долях процента. Рельсы узкой колеи типа Р33 изготавливаются из спокойной углеродистой стали. В зависимости от содержания углерода они подразделяются на нормальные (категория Н), твердые (категория Т) и повышенной твердости (категория ПТ). Прокат из стали повышенной прочности изготовляют классов прочности: 265, 295, 315, 325, 345, 355, 375, 390 и 440, где цифры обозначают предел текучести. Для изготовления конструкций, работающих при низких температурах, применяется сталь марок ОН9, ОН9-Ш, ОН6Б, ОН3, ОН6 и т.д. Содержание углерода в них не более 0,1 %, цифра после буквы Н указывает содержание никеля в целых единицах (например, ОН9 содержит около 9 % никеля). Углеродистые литейные стали маркируются числом, обозначающим среднее содержание углерода (в сотых долях процента), и буквой Л. Несмотря на то, что для всех сталей невозможно применить в полном объёме систему маркировки ГОСТов, она все же наиболее удобна, наглядна и значительно превосходит в этом отношении принятую в других странах систему маркировки стали.
54. Условия образования видманштеттовой структуры.
Большой размер зерна первичного аустенита приводит к появлению аномалии во вторичной микроструктуре углеродистой стали – образованию видманштеттовой структуры. Эта структура характеризуется пластинчатыми образованиями доэвтектоидного феррита или игольчатыми – вторичного цементита, ориентированно располающимися на темном фоне перлита. Возникновение видманштеттовой структуры связано с тем, что, например, в доэвтектоидной стали избыточный феррит выделяется не только на границах, но и внутри крупных зерен аустенита. Кристаллы избыточного феррита, возникшие внутри аустенитного зерна, приобретают пластинчатую форму, причем пластины лежат вдоль плоскостей {111} решетки аустенита. Помимо большого размера зерна аустенита, образованию видманштеттовой структуры способствует ускоренное охлаждение стали от высоких температур. Сталь с видманштет структурой обладает повышенной хрупкостью. Для устранения такой структуры применяют термическую обработку. Видманштеттовые структуры наиболее часто образуются при выделении новых фаз из пересыщенных растворов при искусственном старении сплавов. Образование видманштеттовой структуры в стали характеризуется сдвиговым механизмом перестройки решетки у - а. В результате на поверхности шлифов появлялся игольчатый микрорельеф, позволяющий непосредственно изучать кинетику роста кристаллов методом высокотемпературной металлографии. Появление видманштеттовой структуры в околошовной зоне более характерно для газовой сварки и менее для дуговой.
Образованию нежелательной видманштеттовой структуры способствуют значительный рост зерен аустенита и малая скорость его охлаждения. Образованию видманшттетовой структуры способствуют Мп, Сг и Мо.
55. Сфероидизирующий отжиг. Цель использования. Режимы.
Эвтектоидные и заэвтектоидные стали, имеющие стр-ру перлита или перлита с цементитом вторичным, обладают повышенной твердостью. Для ее снижения эти стали подвергают повторному отжигу при 740-780 °С с последующим медленным охл (он называется сфероидизирующим отжигом). Благодаря такому отжигу выделения вторичного цементита и цементит эвтектоида принимают глобулярную (зернистую) форму, а твердость материала снижается. В такой стр-ре отличить цементит вторичный от цементита эвтектоида практически невозможно. Охлаждение при сфероидизации медленное. Оно должно обеспечить распад аустенита на ферритокарбидную структуру, сфероидизацию и коагуляцию образовавшихся карбидов при охл до 620-680 С. Сталь с зернистым перлитом имеет более низкие значения твердости, времени сопротивления и соответственно более высокие относительные удлинения и сужения. После отжига на зернистый перлит эвтектоидные и заэвтектоидные стали, обл хорошей обрабатываемостью резанием – возможно применение больших скоростей резания и достигается высокая чистота поверхности. Кроме того, такая структура при последующей закалки стали, расширяет интервал закалочных температур и уменьшает склонность к образованию трещин. Сфероидизирующий отжиг обеспечивает превращение пластинчатого перлита в зернистый, сфероидизированный. Это улучшает обрабатываемость сталей резанием. Отжиг на зернистый перлит производят по режиму:нагрев стали немного выше точки Ас1, с последующим охлаждением сначала до 700°С, затем до 550-600°С и далее на воздухе. Сфероидизирующий отжиг применяют для сталей, содержащих более 0,65% углерода, например шарикоподшипниковые стали типа ШХ15.
56. Способы закалки. Обоснование режимов.