Цель работы. Изготовление различных химических источников электрической энергии; наблюдение явлений, происходящих при электролизе водных растворов электролитов; изучение процессов, происходящих при электрохимической коррозии различных металлов.
Приборы: гальванический элемент Якоби-Даниэля, электролизер, вольтметр, низковольтный источник постоянного тока.
Реактивы: растворы – сульфата цинка (1 М), раствор сульфата меди (II) (1 М), иодида калия (0,1н.), сульфата меди (II), соляной кислоты (1н.), гексацианоферрата (III) калия, свежеприготовленный крахмальный клейстер, металлы – гранулированный цинк, медная проволока, цинковая пластинка, оцинкованное и луженое железо.
Опыт 1. Гальванический элемент Якоби-Даниэля
В химический стакан налейте 1 М раствор сульфата цинка и опустите цинковый электрод. В другой стакан налейте 1 М раствор сульфата меди и опустите медный электрод. Растворы соедините электролитическим мостиком, заполненным раствором сульфата меди или хлорида калия. Присоедините провода к клеммам электродов и, после замыкания цепи, определите показания вольтметра. Сравните их с расчетным стандартным значением ЭДС для пары цинк-медь. Напишите уравнения химических процессов, протекающих на электродах.
Опыт 2. Электролиз водных растворов электролитов
|
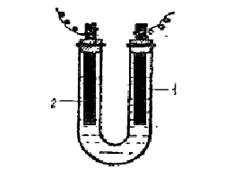
Рис. 9.2. Прибор для электролиза
Растворов солей
Опыт 2.1. Электролиз водного раствора иодида калия
Заполните U-образную трубку 0,5 М раствором KJ, к которому прибавлено 3–4 капли фенолфталеина. В каждое колено U-образной трубки опустите по графитовому электроду и подключите их к низковольтному источнику постоянного тока. Пропускайте в течение 3–5 мин электрический ток. Наблюдайте выделение пузырьков газа и окрашивание раствора у катода. Отключите источник тока. В колено трубки, где находится анод, прилейте 2–3 капли свежеприготовленного крахмального клейстера. Что наблюдается? Составьте схему электролиза. Напишите уравнения реакций, протекающих на электродах.
Опыт 2.2. Электролиз водного раствора сульфата меди (II)
С графитовыми электродами
Налейте в электролизер раствор сульфата меди (II), опустите графитовые электроды и пропускайте в течение 5–10 мин. электрический ток. Наблюдайте выделение пузырьков газа на аноде (какой это газ?). Затем выключите ток. Рассмотрите катод и убедитесь в том, что на нем выделилась медь. Составьте схему электролиза и уравнения реакций, протекающих на электродах.
Опыт 2.3. Электролиз водного раствора сульфата меди (II)
С медным анодом
После окончания электролиза раствора сульфата меди (II) из предыдущего опыта поменяйте полярность электродов. При этом анодом окажется графитовый электрод, покрытый тонким слоем меди. Снова в течение нескольких минут пропускайте электрический ток. Наблюдайте растворение (окисление) меди на аноде (электролиз с активным анодом) и осаждение (восстановление) меди на катоде. Напишите уравнения реакций, происходящих на электродах.
Опыт 3. Коррозия цинка в паре с медью
Опыт 3.1. В пробирку налейте 1 н. раствор соляной кислоты (1/3 объема пробирки) и поместите кусочек цинка. Наблюдается слабое выделение пузырьков водорода. В ту же пробирку опустите зачищенную медную проволоку, так чтобы она не соприкасалась с цинком. Отмечается отсутствие взаимодействия между медью и кислотой. Затем медная проволока приводится в соприкосновение с цинком, при этом на поверхности проволоки появляются пузырьки водорода. Наблюдаемые явления объясняются образованием гальванической пары. Запишите уравнения проходящих электрохимических реакций.
Опыт 3.2. В пробирку с 2-3 мл раствора сульфата меди опустите кусочек цинка на 4-5 мин. Затем омедненный цинк осторожно, но тщательно промойте водой и опустите в 1-2 н. раствор соляной кислоты. В другой такой же раствор поместите цинк, не подвергшийся действию раствора CuSO4. Наблюдайте и объясните различия в интенсивности реакций в разных пробирках.
Запишите уравнения проходящих электрохимических реакций.